
- •Органолептический анализ. Классификация его видов.
- •Основы визуального органолептического анализа.
- •Основы обонятельного анализа.
- •Основы вкусового анализа.
- •Основы осязательного анализа.
- •Подбор дегустаторов. Требования, предъявляемые к ним.
- •Оценка сенсорной чувствительности.
- •10.Метод предпочтения.
- •11.Методы сравнения
- •16.Принцип действия рефрактометров.
- •12 Методы балльной оценки.
- •13.Классификация оптических методов. Их характеристики.
- •21. Оптически активные вещества.
- •Характеристика оав
- •14.Физические основы рефрактометрии.
- •33.Основы теории молекулярных спектров.
- •15. Определение строения вещества с помощью коэффициента преломления.
- •17.Схема прохождения света в рефрактометре Аббе.
- •42.Особенности конструкций ик-спектрометров.
- •18. Схема рефрактометра ран. Принцип работы.
- •19.Практическое применение рефрактометров.
- •20.Поляризованный свет.
- •23.Схема прохождения света при проведении поляриметрического анализа.
- •24.Сущность нефелометрического и турбидиметрического анализов.
- •25. Приборы для нефелометрического анализа.
- •Принцип работы.
- •26. Применение нефелометрического и турбидиметрического анализов.
- •27. Устройство и принцип работы фотонефелометра.(фн-р)
- •28. Основы спектроскопии.
- •29. Классификация спектр.Методов:
- •30. Основы теории оптических атомных спектров. Строение оптических спектров.
- •31.Схема энергетических состояний атомов.
- •32. Спектр поглощения и излучения химических элементов.
- •34. Физические основы фотометрии
- •35. Виды спектров в фотометрии.
- •36. Количественный фотометрический анализ.
- •37. Приборы для фотометрического анализа
- •38. Применение фотометрии.
- •39. Физические основы ик-спектроскопии.
- •40.Основные характеристики ик-спектров.
- •41.Подготовка проб к анализу в ик-спектроскопии.
- •43.Интерпритация ик-спектров.
- •44.Физические основы люминисценции.
- •45.Люминисцентный анализ.
- •46.Возникновение люминисценции.
- •47.Электронные спектры поглощения и спектры люминесценции (излучения)
- •48. Выход и гашение люминесценции
- •49. Качествен.И количествен. Люминесцентный анализ.
- •51.Блок-схема атомно-эмиссионного спектрометра
- •52.Устройство атомизации вещества и возбуждения спектров
- •54Лампа с полым катодом
- •55.Индуктивно-связанная плазма (исп)
- •56.Анализаторы (монохроматоры)
- •57.Способы детектирования излучения.
- •58.Фотоэлектрическое детектирование.
- •59.Расшифровка спектров атомной эмиссии.
- •60.Структура атласа спектров и таблиц спектральных линий. Аналитические линии спектра элемента.
- •62.Фотометрия пламени.
- •79. Разрешающая способность микроскопа.
- •75,Детекторы, газоразрядная трубка, полупроводниковый детектор.
- •76, Качественный и количественный рентгеноспектральный анализ и его применение
- •77.Оптическая микроскопия. Подготовка образцов.
- •78. Устройство и принцип действия оптических микроскопов.
- •80. Количественная металлография. Точечный, линейный и плоскостной анализы структуры материала
- •81. Устройство и принцип действия электронного микроскопа
- •82. Получение изображения в электронном микроскопе
- •83. Подготовка образцов для просвечивающей микроскопии
- •84. Схема растрового электронного микроскопа
- •85. Термический анализ
- •86. Дифференциальный термический анализ.
- •87. Дифференциальные кривые нагревания.
- •89.Термогравиметрический анализ.(тгма)
- •90. Диф. Термогравиметрическая кривая (дтг)
- •93,94. Качественный и количественный термический анализ. Определение чистоты хим. Веществ методом дта (дифференциальный термический анализ).
- •98. Сенсоры на основе мдп-структур
- •99.Тепловые сенсоры. Термокаталитические сенсоры
33.Основы теории молекулярных спектров.
Молекулярный спектр – спектры испускания и поглощения эл-магнитн излучения свободными либо слабо связанными молекулами. Это полосы имеют вид совокупных полос в УФ , видимой, ИК и радиоволновой областях спектра.
Положение полос в спектрах испускания и поглощения хар-ся частотами, длинами волн и волновыми числами вихmax.
К собственно молекул спектрам относят только спектры, которые связаны с оптическими переходами между электронно-колебат-вращат уровнями энергии молекулы, т.е. они связаны с 3-мя типами внутр движения в молекулах. В молекуле сущ. 3 типа энергии: 1.электронная (Еэл) 2. колебательная (Екол) 3. вращательная (Евр)
Суммарная энергия молекулы равна сумме этих 3х составляющих: Е=Еэл+Екол+Евр
У молекулы не м.б. чисто электронных переходов с уровня на уровень, возможны только электрон.колеб. вращат. переходы (э.к.в.).
Число этих переходов у молекулы значительно больше чем у атомов. Поэтому спектры молекулы сложнее и состоят из большого числа спектральных линий, кот.сливаются в спектральные полосы различной ширины.
Под воздействием электронно-магнитных излучений в молекуле могут происходить э.к.в. переходы поглощения или излучения.
Э.к.в. переходы поглощения соотв. поглощению УФ и видимого диапазонов. Они лежат в основе фото- и спектрофотометр.ан.
Э.к.в. переходы испускания соотв. испусканию этого же диапазона и лежат в основе явления люминесценции и основан на нем флуоресцентного анализа.
15. Определение строения вещества с помощью коэффициента преломления.
Каждое
химическое соединение имеет строго
определённое значение показателей
преломления, величина которого зависит
от строения этого вещества. При прохождении
света через неполярное вещество
происходит деформационная поляризация
молекул,
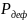 ,которая
вызывается за счёт смещения электронов
относительно ядер атомов (электронная
поляризация). А также поляризация молекул
осуществляется за счёт смещения ядер
атомов относительно друг друга – атомная
поляризация.
,которая
вызывается за счёт смещения электронов
относительно ядер атомов (электронная
поляризация). А также поляризация молекул
осуществляется за счёт смещения ядер
атомов относительно друг друга – атомная
поляризация.
В связи с поляризацией, электронной и атомной, происходит пропорциональное изменение напряжённости поля.
Центр тяжести положительных и отрицательных зарядов в молекуле при поляризации не совпадают, поэтому возникает индуцированный дипольный момент, который пропорционален напряжённости поля.
При
прохождении света через полярное
вещество, кроме деформационной поляризации
добавляется так называемая ориентационная
поляризация
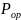 ,
которая связана с тем, что под влиянием
электромагнитного поля полярные молекулы
ориентируются вдоль силовых линий
электромагнитного поля, стремясь принять
устойчивое положение, отвечающее min
потенциальной энергии.
,
которая связана с тем, что под влиянием
электромагнитного поля полярные молекулы
ориентируются вдоль силовых линий
электромагнитного поля, стремясь принять
устойчивое положение, отвечающее min
потенциальной энергии.
Р = + (0-5)
Так как у неполярных веществ отсутствует, то: Р = . (0-6)
В этом случае взаимосвязь деформационной поляризации с коэффициентом преломленияn осуществляется формулой:
=
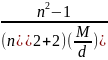 (0-7) - формула Лорентса-Лоренса, где n
- коэффициент
преломления, d
– плотность вещества, M
– молекулярная
масса вещества.
(0-7) - формула Лорентса-Лоренса, где n
- коэффициент
преломления, d
– плотность вещества, M
– молекулярная
масса вещества.
В
этой формуле
называется молярной рефракцией и
обозначается
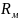 :
=
:
=
Молярная
рефракция служит мерой деформационной
поляризации молекул вещества и имеет
размерность
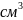 /моль.
/моль.
Молярная рефракция рассчитывается для различных веществ на основе правила аддитивности, то есть рефракция молекулы равна сумме рефракций составляющих её частиц с учётом валентных связей состояний атомов и их расположения.
Для молекул различных веществ молярные рефракции приводятся в справочной литературе. Сравнивая полученную опытным путём с помощью формулы (0-7) молярную рефракцию с литературной, можно точно определить строение исследуемого вещества.
