
- •Глава 8 методы генной инженерии. Промышленный синтез белков, инсулина, соматотропина и интерферона
- •8.1. История создания генетической инженерии
- •8.2. Схема строения молекулы днк и триплетность генетического кода
- •Модель днк
- •8.3. Ферменты в генной инженерии
- •8. 4. Технология получения рекомбинантной молекулы днк
- •Рекомбинантной молекулы днк
- •8. 5. Векторы, используемые для клонирования днк
- •8. 6. Экспрессия генов в бактериальных клетках и микроорганизмах
- •До копирования всего структурного гена
- •С большой рибосомной субъединицей
- •В качестве объекта для клонирования и экспрессии
- •8.7. Метод электрофорезного разделения днк и этапы идентификации днк по Саузерну
- •Для электрофореза днк в агаровом геле
- •Идентификации днк методом Саузерн-блот гибридизации
- •8. 8. Секвенирование днк и получение генов
- •Семейства меченных фрагментов днк
- •Полученной методом секвенирования днк
- •Днк ферментативным методом
- •8. 9. Амплификация (увеличение числа копий) фрагментов днк с помощью метода полимеразной цепной реакции (пцр)
- •Фрагмента днк
- •8.10. Генетическая инженерия и ее возможности для практики
- •8. 11. Промышленный синтез белков
- •«Расплодки»
- •8. 12. Биотехнология получения инсулина, гормона роста и интерферона
- •При синтезе интерферона человека в e. Coli.
- •Глава 9
- •9. 2. Трансгенные животные (метод получения)
- •9. 2. 1. Методы введения чужеродного гена в организм животного
- •9.2.2. Создание разных видов трансгенных животных
- •9. 2. 3. Клонирование
- •В яйцеклетку (по Беквисту)
- •Методом пересадки ядер
- •9. 2. 4. Межвидовые пересадки эмбрионов и получение химерных животных
- •9. 2. 5. Получение гомозиготных диплоидных потомков
- •Диплоидных потомков
- •9. 2. 6. Создание партеногенетических животных
- •9. 2. 7. О генетическом риске и биобезопасности в биоинженерии и трансгенных технологиях
- •9. 3. Государственное регулирование безопасности генно-инженерной деятельности в Республике Беларусь
- •Глава 10 иммобилизованные ферменты
- •10. 1. Понятие «инженерная энзимология»
- •И иммобилизация ферментов
- •И Saccharomyces carlsberqensis, используемые для получения фермента инвертазы
- •10.2. Механизм биотехнологического действия ферментов
- •10. 3. Технология глубинного культивирования микроорганизмов – продуцентов ферментов.
- •10. 4. Технология выделения и очистки ферментных препаратов
- •10. 5. Иммобилизованные ферменты. Методы иммобилизации
- •10. 6. Практическое применение иммобилизованных ферментов
- •При растворении тромбов в кровеносных сосудах
- •«Искусственная почка»
- •Глава 11
- •Гидроксилирование кортизола
- •11. 2. Методы контроля репродуктивной функции у животных
- •11. 3. Нейро-гуморальная регуляция внутрияичниковых процессов. Рост и развитие эмбрионов
- •Внутрияичниковых процессов
- •11. 4. Биотехнология получения потомков животных желаемого пола
- •Быков производителей по полу
- •Глава 12 получение аминокислот и белка одноклеточных организмов
- •12.1. Содержание незаменимых аминокислот в белках некоторых микроорганизмов
- •12. 2. Выращивание кормовых дрожжей
- •12.3. Белковые концентраты из бактерий
- •На газообразных углеводородах
- •12.4. Кормовые белки из водорослей
- •12. 5. Белки микроскопических грибов
- •12. 6. Кормовые белковые концентраты из растений
- •12. 7. Производство незаменимых аминокислот
- •Из аспарагиновой кислоты
- •12. 8. Производство кормовых витаминных препаратов
- •12. 9. Кормовые липиды
- •12. 10. Производство ферментных препаратов
- •Глава 13
- •13. 2. Результаты использования пребиотиков
- •13. 3. Эффективность использования гербиотиков и симбиотиков
- •13. 4. Результаты применение заквасок для силосования
- •Заключение
- •Литература Основная
- •Дополнительная
- •Содержание
10. 4. Технология выделения и очистки ферментных препаратов
Выделение и очистка фермента как из культуры микроорганизма (выращенного любым способом), так и из других природных источников весьма трудоёмкая и дорогостоящая процедура. Поэтому, если фермент можно использовать в виде неочищенного препарата, его не очищают. В промышленности широко применяют коммерческие препараты ферментов, частота которых составляет всего 0,1% (т. е. 99,9% составляют примеси). К таким отраслям относятся сельское хозяйство, спиртовая, кожевенная, текстильная промышленность, производство бытовой химии. Например, ферментный препарат, употребляемый в пивоварении, представляет собой высушенную биомассу плесневых грибов. В большинстве отраслей пищевой промышленности и особенно в биотехнологии используют только очищенные препараты ферментов, частично или полностью освобождённые от балластных веществ и полностью охарактеризованные в отношении их специфичности и физико-химических свойств. Исходным материалом для получения препаратов ферментов служат биомасса продуцента, фильтрат культуральной жидкости, экстракт из культуры микроорганизма или из тканей и органов растений и животных. Из них готовят препараты различной степени очистки.
Ферментные препараты получают:
1. Путём высушивания в мягком режиме культуры микроорганизмов вместе с остатками питательной среды;
2. Путём упаривания экстракта из культуры продуцента, выращенного поверхностным способом;
3. Путём глубинного выращивания микроорганизмов, т. е. из фильтрата культуральной среды;
4. Путём применения метода ацетоновых порошков, состоящий в осаждении и быстром обезвоживании при температуре не выше -10 С тканей или вытяжек из них, содержащих ферменты.
Препараты ферментов представляют собой либо высушенные до порошкообразного состояния продукты, либо жидкие концентраты, характеризующиеся 50% - м содержанием сухой массы веществ.
Для выделения фермента из клеточного содержимого необходимо очень тонкое измельчение исходного материала путём разрушения клеточных структур: лизосом, митохондрий, ядер и др. Они имеют в своём составе многие индивидуальные ферменты. Для этого используют:
- Специальные мельницы и гомогенизаторы;
- Ультразвук;
-Метод попеременного замораживания и оттаивания ткани.
Особое внимание при выделении ферментов уделяют проведению всех операций в условиях исключающих денатурацию белка (нейтральное значение рН, стабилизирующие добавки в виде белков, солей и специальных соединений).
Пример, иллюстрирующий получение очищенного препарата β-галактозидазы из мутанта E. coli, представлен на рис. 10.4.
Схема очистки включает отделение клеток микроорганизма при выходе их из ферментёра с культуральной жидкостью посредством центрифугирования и последующее разрушение клеток в гомогенизаторе высокого давления.
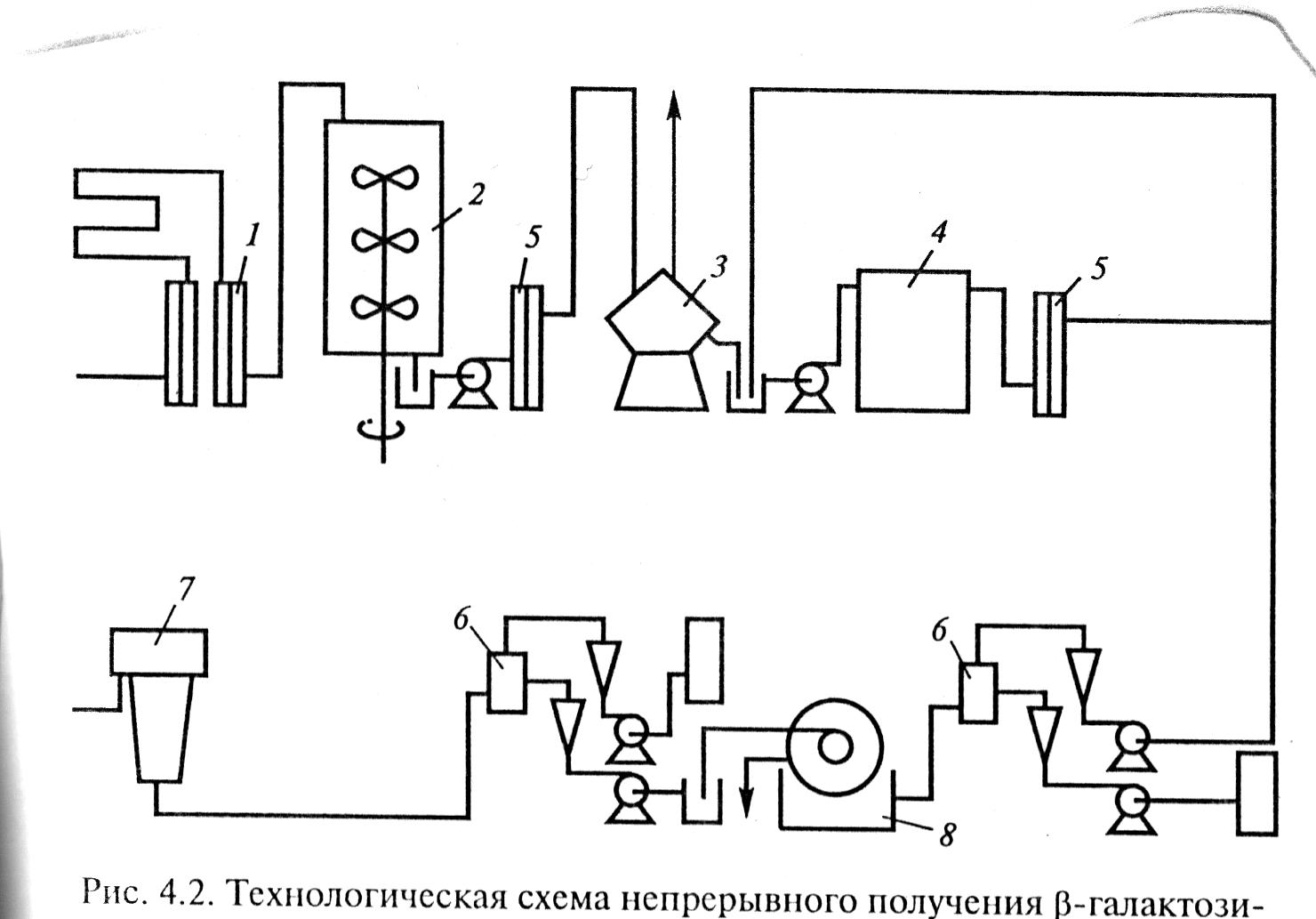
Рис.10.4. Технологическая схема непрерывного получения
β-галактозидазы
1 - стерилизатор среды; 2 - ферментёр; 3, 7 - центрифуги;
4 - гомогенизатор; 5 - теплообменник; 6 - смесительные камеры;
8 - ротационный вакуум фильтр
Для освобождения белков и нуклеиновых кислот полученный гомогенат обрабатывают сульфатом марганца до конечной концентрации этой соли в смеси, равной 0,05М. Осадок нуклеиновых кислот отделяется с помощью ротационной вакуум-фильтрации. Вся процедура очистки энзима от момента подачи бактерий в систему до момента получения осадка β-галактозидазы занимает всего 1 час.
В производственных условиях активность получаемого ферментного препарата оценивается количеством субстрата преобразованного 1 кг (1 мг) препарата при оптимальных условиях за 1 мин, и измеряется в Е/мг, моль/мг белка.
Очищенные ферментные препараты хранят при низкой температуре - до -80С. Для стабилизации ферментов в их препараты добавляют коферменты и субстраты. Ферментные препараты для промышленного применения стабилизируют, добавляя глицерин, моносахариды, дисахариды (глюкоза, сахароза, лактоза), отдельные аминокислоты и желатину.
В настоящее время из 2003 включённых в список известных в настоящее время ферментов более 1500 выделено и в той или иной степени очищено. Это служит базой для дальнейшего изучения физико-химических основ их химического производства на промышленном уровне.
