
- •Глава 8 методы генной инженерии. Промышленный синтез белков, инсулина, соматотропина и интерферона
- •8.1. История создания генетической инженерии
- •8.2. Схема строения молекулы днк и триплетность генетического кода
- •Модель днк
- •8.3. Ферменты в генной инженерии
- •8. 4. Технология получения рекомбинантной молекулы днк
- •Рекомбинантной молекулы днк
- •8. 5. Векторы, используемые для клонирования днк
- •8. 6. Экспрессия генов в бактериальных клетках и микроорганизмах
- •До копирования всего структурного гена
- •С большой рибосомной субъединицей
- •В качестве объекта для клонирования и экспрессии
- •8.7. Метод электрофорезного разделения днк и этапы идентификации днк по Саузерну
- •Для электрофореза днк в агаровом геле
- •Идентификации днк методом Саузерн-блот гибридизации
- •8. 8. Секвенирование днк и получение генов
- •Семейства меченных фрагментов днк
- •Полученной методом секвенирования днк
- •Днк ферментативным методом
- •8. 9. Амплификация (увеличение числа копий) фрагментов днк с помощью метода полимеразной цепной реакции (пцр)
- •Фрагмента днк
- •8.10. Генетическая инженерия и ее возможности для практики
- •8. 11. Промышленный синтез белков
- •«Расплодки»
- •8. 12. Биотехнология получения инсулина, гормона роста и интерферона
- •При синтезе интерферона человека в e. Coli.
- •Глава 9
- •9. 2. Трансгенные животные (метод получения)
- •9. 2. 1. Методы введения чужеродного гена в организм животного
- •9.2.2. Создание разных видов трансгенных животных
- •9. 2. 3. Клонирование
- •В яйцеклетку (по Беквисту)
- •Методом пересадки ядер
- •9. 2. 4. Межвидовые пересадки эмбрионов и получение химерных животных
- •9. 2. 5. Получение гомозиготных диплоидных потомков
- •Диплоидных потомков
- •9. 2. 6. Создание партеногенетических животных
- •9. 2. 7. О генетическом риске и биобезопасности в биоинженерии и трансгенных технологиях
- •9. 3. Государственное регулирование безопасности генно-инженерной деятельности в Республике Беларусь
- •Глава 10 иммобилизованные ферменты
- •10. 1. Понятие «инженерная энзимология»
- •И иммобилизация ферментов
- •И Saccharomyces carlsberqensis, используемые для получения фермента инвертазы
- •10.2. Механизм биотехнологического действия ферментов
- •10. 3. Технология глубинного культивирования микроорганизмов – продуцентов ферментов.
- •10. 4. Технология выделения и очистки ферментных препаратов
- •10. 5. Иммобилизованные ферменты. Методы иммобилизации
- •10. 6. Практическое применение иммобилизованных ферментов
- •При растворении тромбов в кровеносных сосудах
- •«Искусственная почка»
- •Глава 11
- •Гидроксилирование кортизола
- •11. 2. Методы контроля репродуктивной функции у животных
- •11. 3. Нейро-гуморальная регуляция внутрияичниковых процессов. Рост и развитие эмбрионов
- •Внутрияичниковых процессов
- •11. 4. Биотехнология получения потомков животных желаемого пола
- •Быков производителей по полу
- •Глава 12 получение аминокислот и белка одноклеточных организмов
- •12.1. Содержание незаменимых аминокислот в белках некоторых микроорганизмов
- •12. 2. Выращивание кормовых дрожжей
- •12.3. Белковые концентраты из бактерий
- •На газообразных углеводородах
- •12.4. Кормовые белки из водорослей
- •12. 5. Белки микроскопических грибов
- •12. 6. Кормовые белковые концентраты из растений
- •12. 7. Производство незаменимых аминокислот
- •Из аспарагиновой кислоты
- •12. 8. Производство кормовых витаминных препаратов
- •12. 9. Кормовые липиды
- •12. 10. Производство ферментных препаратов
- •Глава 13
- •13. 2. Результаты использования пребиотиков
- •13. 3. Эффективность использования гербиотиков и симбиотиков
- •13. 4. Результаты применение заквасок для силосования
- •Заключение
- •Литература Основная
- •Дополнительная
- •Содержание
При синтезе интерферона человека в e. Coli.
Установлено, что интерфероны синтезируются в клетке сначала в виде предшественников, содержащих на N-конце полипептидной цепи сигнальный пептид, который затем отщепляется и, в результате, образуется зрелый интерферон, обладающий полной биологической активностью. Бактерии не содержат ферментов, способных отщепить сигнальный пептид с образованием зрелого белка. Для того чтобы бактерии синтезировали зрелый интерферон, следует ввести в плазмиду только ту часть гена, которая его кодирует, и удалить часть гена, кодирующую сигнальный пептид. Процедура требует соблюдения следующих условий:
- Ген интерферона должен содержать три участка расщепления рестриктазой Sau 3A1, из которых один находится рядом с сигнальной частью.
- Неполное расщепление гена этим ферментом позволяет выделить фрагмент гена, содержащий нуклеотидную последовательность, кодирующую зрелый интерферон.
- Триплет ATG, кодирующий цистеин, отщепляется ферментом вместе с сигнальной частью.
-Для восстановления полинуклеотидной последовательности полного гена химически был синтезирован фрагмент ДНК, содержащий этот триплет, а также примыкающий к нему триплет ATG-точка инициации синтеза белка.
- Этот фрагмент присоединили к изолированной части зрелого гена, в результате был восстановлен полный ген зрелого интерферона.
- Реконструированный ген ввели в плазмиду таким образом, что с ним оказался рядом участок ДНК-промотор, обеспечивающий начало синтеза мРНК.
- Экстракты из E. Coli, содержащие такую плазмиду, обладали противовирусной активностью.
Синтезированный генно-инженерным способом интерферон был выделен, очищен, и его физико-химические свойства оказались близкими свойствам интерферона, полученного из крови доноров. Удалось получить бактерии, способные синтезировать до 5 мг интерферона на 1 л бактериальной суспензии, содержащей примерно 1011 бактериальных клеток, что в 5000 раз превосходит то количество интерферона, которое можно извлечь из 1 литра крови доноров.
В настоящее время гены интерферонов клонированы в дрожжи и клетки высших эукариот, способных осуществлять гликолизирование.
В 1991 году в США впервые для синтеза лейкоцитарного интерферона человека были употреблены генетически сконструированные клетки дрожжей Saccharomyces cerevisiae. Полученная эффективная экспрессия гена LeIF и замена бактерий клетками дрожжей позволили увеличить производство интерферона в 10 раз.
В России в 1994 году был осуществлён полный синтез гена α-И размером примерно 600 н. п. (нуклеотидных пунктов) в Институте биоорганической химии под руководством Н. М. Колосова.
Несмотря на успехи, достигнутые в области получения интерферонов с помощью генно-инженерных технологий и их применения для лечения различных вирусных заболеваний, в том числе онкологических, предстоит решить ещё многие вопросы, касающиеся расшифровки механизмов их биосинтеза и взаимодействия с другими веществами.
Схема биологического действия интерферона представлена на рисунке 8.34.
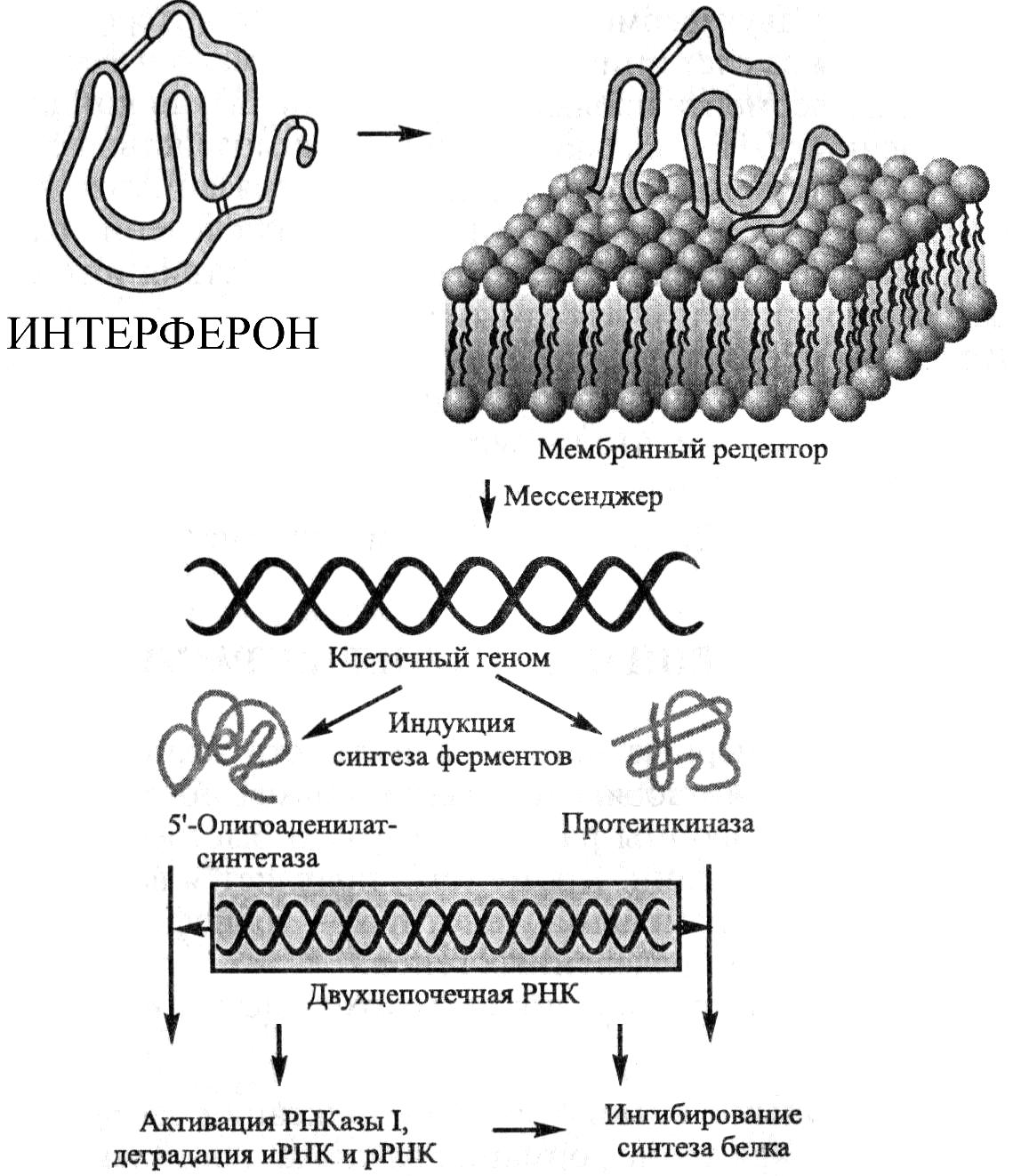
Рис. 8.34. Механизм действия интерферона
Механизм действия интерферона можно свести к следующим основным этапам:
1. Связываясь с клеточными рецепторами, интерфероны инициируют синтез ферментов 5'-олигоаденилансинтетазы и протеинкиназы за счёт инициации транскрипции соответствующих генов;
2. Оба фермента проявляют свою активность в присутствии двухцепочных ДНК, являющихся продуктами репликации многих вирусов;
3. Фермент 5'-олигоаденилансинтетаза катализирует синтез 2' 5'-олигоаденилатов (из АТР), которые активируют клеточную рибонуклеазу;
4. Протеинкиназа фосфорилирует и тем самым активирует фактор инициации трансляции IF2. В результате этих событий ингибируется биосинтез белка и размножение вируса (деградация иРНК и рРНК) в инфицированной клетке, что вызывает её лизис.
