
- •Основная
- •Дополнительная
- •Методические указания, разработанные на кафедре и изданные в ризо бгу.
- •Вопросы по аналитической химии для подготовки к экзамену студентам биологического факультета.
- •Лекция Буферные растворы
- •Механизм действия буферной системы
- •РН некоторых биологических жидкостей.
- •Расчёт рН буферного раствора
- •Лекция Способы выражения концентрации растворов.
- •Домашние задания
- •Подготовка к второму занятию.
- •Подготовка к третьему занятию.
- •Подготовка к четвёртому занятию.
- •Принципы аналитической оптической спектроскопии.
- •Атомно – эмиссионная спектроскопия
- •Лекция 8 Атомно-абсорбционная спектроскопия
- •Способ атомизации.
- •Способы определения концентрации
- •Достоинства метода.
- •Недостатки метода.
- •Полярография
- •Качественный полярографический анализ
- •Количественный полярографический анализ
- •Амперометрия
- •Электрохимические методы анализа потенциометрия
- •Электроды сравнения и индикаторные электроды
- •Электроды сравнения
- •Индикаторные электроды.
- •Требования к индикаторным электродам.
- •Способы потенциометрического анализа Ионометрия, рН-метрия
- •Потенциометрическое титрование
- •Кулонометрический анализ (кулонометрия) Принципы метода.
- •Прямая кулонометрия
- •Кулонометрическое титрование
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
- •Типовые тренировочные задачи по теме «Инструментальные методы анализа» для подготовки к рубежному контролю Модуля 2.
Атомно – эмиссионная спектроскопия
Метод атомно – эмиссионной спектроскопии (АЭС) основан на испускании (эмиссии) квантов электромагнитного излучения возбуждёнными атомами. Схему атомной эмиссии можно представить следующим образом:
А + Е → А• → А + hν,
где А – атом элемента; Е – энергия, поглощаемая элементом; А• - возбуждённый атом; hν – испускаемый квант света.
Блок схема
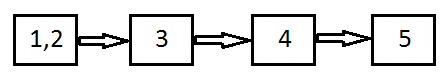
1,2 - источник света, выполняет три функции:
1) испарение образца;
2) атомизация молекул;
3) возбуждение атомов.
3 - селектор частоты (излучаемый свет для анализа необходимо диспергировать на монохроматические линии).
4 - детектор излучения.
5- регистрирующее устройство.
В качестве источника возбуждения применяют пламя, электрические дуги (постоянного и переменного тока), низковольтную или высоковольтную конденсированную искру, тлеющие разряды, высокочастотные разряды (индуктивно связанная плазма, микроволновой разряд и лазер). Возбуждение атома происходит при столкновении с частицами плазмы, дуги или сикры, обладающими высокой кинетической энергией. При поглощении атомом энергии внешний электрон переходит на более высокий энергетический уровень и через 10-7 – 10-9 секунд возвращается на основной уровень, при этом энергия выделяется в виде кванта света – hν. Положение спектральной линии в спектре зависит от природы элемента, а интенсивность зависит от количества атомов, в которых осуществляется переход.
В атомной спектроскопии необходимо перевести вещество в атомарное состояние – атомизировать. В атомно – эмиссионных методах способ атомизации является одновременно и способом возбуждения атомов. Образуются линейчатые спектры атомов. Атомизацию осуществляют пламенным и электротермическим способами.
Эмиссионная фотометрия пламени. Метод основан на измерении интенсивности излучения, испускаемого атомами, возбуждаемыми в пламени.
Пламя образуется при сгорании горючего газа в окислителях. Температура пламени невысока (1700 – 3000 оС), однако её достаточно для возбуждения резонансных линий наиболее легко возбудимых атомов (щелочные и щелочноземельные металлы). Интенсивность излучения атомами пропорциональна их концентрации в пламени, которая, в свою очередь, пропорциональна концентрации ионов в растворе:
I = K ∙ c,
где I – интенсивность спектральной линии; c – концентрация вещества.
Эта прямолинейная зависимость соблюдается при постоянстве коэффициента К, на значение которого могут повлиять помехи: образование труднолетучих соединений, ионизация, изменение режима работы источника возбуждения, самопоглощение. Не все кванты, испускаемые возбуждёнными частицами, достигают приёмника света, квант может быть поглощён невозбуждённым атомом и , таким образом, не будет зафиксирован приёмником излучения. Это так называемое самопоглощение.
Интенсивность излучения измеряют в пламенных фотометрах и спектрофотометрах, преобразуя световой поток спектральной линии при определённой резонансной длине волны в электрический ток (фототок) с помощью фотоэлемента.
Способы определения концентрации такие же как в молекулярной спектроскопии: метод градуировочного графика и метод добавок.
Атомно – эмиссионный анализ с электротермическим возбуждением. Для большинства элементов для возбуждения используют дуговые и искровые электротермические источники, дуги постоянного и переменного тока с температурой 5 000 – 7 000 оС в зависимости от материалов электрода. Можно определять почти все металлы периодической системы Менделеева.
Конденсированная искра – температура 10 000 оС, возбуждаются все элементы периодической системы.
Спектральную линию наблюдают визуально (в спектроскопах и стилоскопах), регистрируют на фотопластинках (в спектрографах), преобразуют в электрический сигнал с помощью фотоэлементов и фотоумножителей (в квантометрах).
Определяя длину волны анализируемой спектральной линии можно проводить качественный анализ пробы, т.е. идентифицировать вещества, присутствующие в образце.
Количественный эмиссионный спектральный анализ основан на зависимости интенсивности спектральной линии от концентрации вещества (c) в пробе – формула Ломакина-Шайбе
I = a ∙ cb,
где a – коэффициент, зависящий от режима работы источника возбуждения, его стабильности, температуры и т.д.; b – коэффициент самопоглощения, учитывающий поглощение кванта света невозбуждёнными атомами.
При логарифмировании этого уравнения получаем:
Ig I = Ig a + bIg c = const + bIg c
Это уравнение является основой количественного спектральног анализа.
Чтобы исключить искажения спектральной линии за счёт различных помех применяют для анализа гомологическую пару линий.
Аналитическая линия – линия определяемого элемента. Линия сравнения – линия основы и специальной добавки (внутренний стандарт), заранее введённый в образец.
При фотографической регистрации используют зависимость
∆S=f (Ig c),
где S – почернение спектральной линии на фотопластинке
∆S=Sx - SСТ
В квантометрах для приёма сигнала используют фотоэлектрические детекторы.
Преимущества метода.
Атомно – эмиссионный метод с применением дуги используется для качественного и полуколичественного анализа различных объектов.
Можно анализировать твёрдые и жидкие образцы. Метод избирательный. Из одной пробы можно обнаружить до 30 элементов без предварительного разделения.
Документальность.
Для анализа требуется незначительное количества вещества.
Недостаток.
Невысокая точность метода.
Эмиссионная фотометрия пламени – это самый распространённый, чувствительный и воспроизводимый метод определения натрия и калия в почвах, биологических и медицинских объектах, водах.
