
Лабораторные работы по материаловедению 3 семестр / ЛАБОРАТОРНАЯ РАБОТА 7
.docФедеральное агентство по образованию Российской Федерации
Филиал государственного образовательного учреждения
высшего профессионального образования
«Уфимский государственный авиационный технический университет» в г. Стерлитамаке
Кафедра ОТиМ
ДИАГРАММЫ СОСТОЯНИЯ И СТРУКТУРЫ СПЛАВОВ СИСТЕМ «МЕДЬ-НИКЕЛЬ» И «СВИНЕЦ-СУРЬМА»
отчет
по лабораторной работе №7
Группа: МХС – 204д
Студент:
Преподаватель: Хужахметов З.И.
Стерлитамак, 2005
ЛАБОРАТОРНАЯ РАБОТА №7
ДИАГРАММЫ СОСТОЯНИЯ И СТРУКТУРЫ СПЛАВОВ СИСТЕМ «МЕДЬ - НИКЕЛЬ» И «СВИНЕЦ - СУРЬМА»
-
ЦЕЛЬ РАБОТЫ:
-
Ознакомиться со структурами сплавов систем «медь-никель» и «свинец - сурьма» в равновесном состоянии.
-
Научиться, пользуясь диаграммами состояния, анализировать формирование структуры сплавов при изменении температуры и состава.
-
СВЕДЕНИЯ ИЗ ТЕОРЕТИЧЕСКОЙ ЧАСТИ:
а) об использовании правила отрезков для определения фазового состояния, химического состава фаз и относительного количества фаз;
При сплавлении этих металлов образуются неограниченные твердые растворы замещения; не образуются химические соединения и механические смеси фаз.
Медь и никель имеют одинаковую решетку (ГЦК), близкие атомные радиусы (Сu - 0,128 нм, Ni -0,125 нм) и расположены в соседних (VIII и 1в) группах периодической системы.
Линия асе на диаграмме состояния Сu - Ni (рисунок 3.1) называется "ликвидус". Выше этой линии все сплавы данной системы находятся в жидком состоянии. Линия acfe называется "солидус".
Ниже этой линии все сплавы находятся в твердом состоянии. Между ликвидусом и солидусом одновременно находятся две фазы: жидкий и твердый (α) растворы. Чтобы охарактеризовать фазовое состояние конкретного сплава при заданной температуре, необходимо определить природу фаз, находящихся в равновесии при данной температуре, их химический состав и относительное количество. Для примера рассмотрим изменение фазового состояния, происходящее при снижении температуры в сплаве, содержащем 30 % Ni и 70 % Сu (рисунок 3.1).
Для определения фазового состояния сплава в интервале кристаллизации применяют правило отрезков. Например, при произвольно выбранной температуре t1 (рисунок 3.1) через точку К, лежащую на ординате сплава, проводят горизонтальную линию (изотерму) до пересечения с ближайшими линиями диаграммы. Точки пересечения укажут, какие фазы находятся в равновесии у данного сплава при t1: m - соответствует жидкому раствору, n - твердому раствору α. По проекциям точек пересечения на ось концентрации определяют химические составы равновесных фаз: в жидкой фазе содержится om' % Ni (остальное Сu); в α -фазе - on' % Ni (остальное Сu).
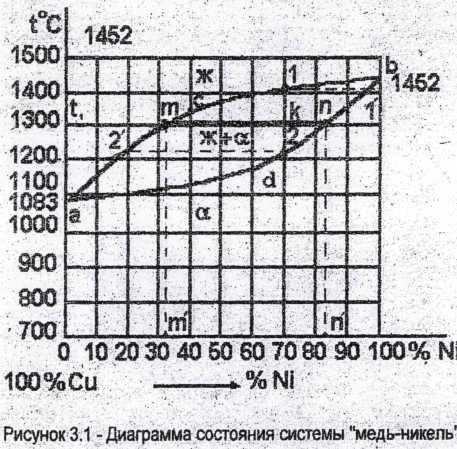
Количественное соотношение равновесных фаз определяют по отрезкам: количество жидкой фазы пропорционально kn, а α фазы - mk. Линию mn называют конодой.
При охлаждении сплава из жидкого состояния ниже точки 1, лежащей на линии ликвидус, начинается кристаллизация. При переходе через точку 2 на линии солидус кристаллизация заканчивается. В процесс кристаллизации концентрация компонентов в жидком растворе изменяется согласно ликвидусу от точки 1 до точки 2', а в растворе α - согласно солидусу от точки 1' до точки 2.
После окончания кристаллизации структура сплава состоит из зерен твердого раствора α, имеющих одинаковый состав. Поскольку сплав был выбран произвольно, то рассуждения о формировании его структуры применимы к любому сплаву этой системы, кроме чистых Сu и Ni.
б) о методике определения химического состава сплава по микроструктуре;
В сплавах, содержащих две структурные составляющие, по их микроструктуре можно определить химический состав. Например, определим химический состав доэвтектического сплава состава X (рисунок 3.2). Весовое количество Sb в этом сплаве равно сумме его весовых количеств в первичных кристаллах α и эвтектике. Относительное количество первичных кристаллов α и эвтектики можно определить по структуре сплава. Пусть Fα - относительная доля площади шлифа, занимаемая первичными кристаллами α, Fэвт. - занимаемая эвтектикой. Тогда, пренебрегая разностью удельных весов α и эвтектики, можно считать, что отношение Fα/Fэвт равно отношению весовых количеств этих структурных составляющих и, следовательно,

где 0,44 - содержание Sb в а фазе, %;
13 - содержание Sb в эвтектике, %.
Микроструктура сплавов выявлена травлением шлифов травителем состава 4 % HNO3 + 96 % С2Н5ОН. При наблюдении и изображении структур сплавов системы Рb - Sb необходимо иметь в виду, что α - фаза темная, β -фаза светлая, эвтектика - однородная смесь, темной составляющей α с небольшим количеством светлых включений β - фазы.
-
ДИАГРАММА СОСТОЯНИЯ СИСТЕМЫ Cu – Ni.
-
ДИАГРАММА СОСТОЯНИЯ СИСТЕМЫ Pb – Sb.
-
КРИВАЯ ОХЛАЖДЕНИЯ СПЛАВА Pb-Sb:
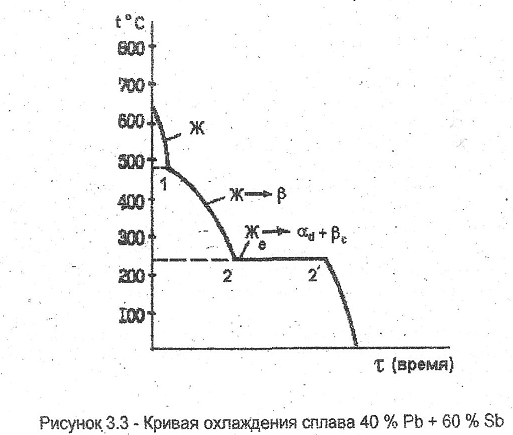
-
ВЫВОД:
-
ОТВЕТЫ НА КОНТРОЛЬНЫЕ ВОПРОСЫ:
-
Твердыми растворами называются кристаллические фазы переменного состава. Атомы растворенного компонента размещаются в кристаллической решетке компонента-растворителя, либо замещая атомы растворителя в узлах его решетки, либо располагаясь в межузлиях. В первом случае образуются твердые растворы замещения, во втором твердые растворы внедрения.
-
После окончания кристаллизации структура сплава состоит из зерен твердого раствора , имеющих одинаковый состав. Поскольку сплав был выбран произвольно, то рассуждения о формировании его структуры применимы к любому сплаву этой системы, кроме чистых Cu и Ni.
-
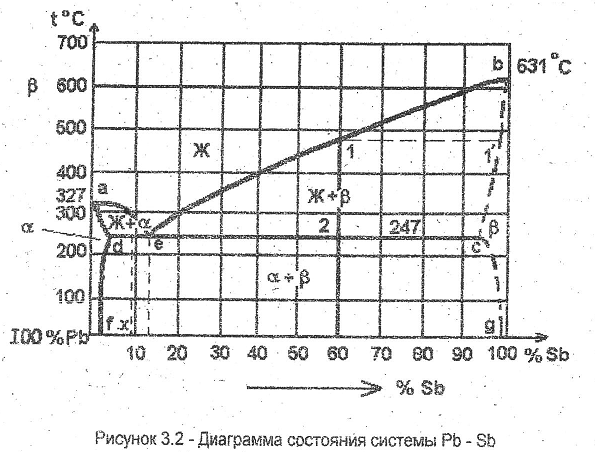
Диаграмма состояния системы «свинец-сурьма» характеризуется тем, что компоненты, неограниченно растворимые друг в друге в жидком состоянии, лишь ограниченно растворимы в твердом состоянии и образуют эвтектику (рисунок 3.2).
-
Ликвидус состоит из двух ветвей – ае и еb. Ниже ае начинается кристаллизация твердого раствора (твердый раствор замещения Sb и Pb), а ниже линии еb – кристаллизация твердого раствора β (твердый раствор замещения Pb и Sb).
Солидус состоит из трех участков ad, bc и dec. Ниже линии ad завершается кристаллизация твердого раствора , ниже линии be завершается кристаллизация твердого раствора β. На линии dec имеет место эвтектическое равновесие:
![]()
