
- •Учебно-методическое пособие
- •080502 «Экономика и управление на предприятии (металлургия)»
- •Глава 1 Основы теории процессов обработки металлов давлением………6
- •Глава 2 Прокатное производство…………………………………………...24
- •Глава 7 Специальные процессы обработки металлов давлением……….106
- •Глава 1 Основы теории процессов обработки металлов давлением
- •1.1 Основные процессы обработки металлов давлением
- •1.2 Кристаллическое строение металлов
- •1.3 Упругая и пластическая деформация
- •1.4 Напряженно – деформированное состояние металла в процессах обработки давлением
- •1.5 Механизмы пластической деформации металлов
- •1.6 Наклеп и рекристаллизация
- •1.7 Пластичность металлов и сопротивление металлов пластической деформации
- •1.8 Внешнее трение при обработке металлов давлением
- •Глава 2 Прокатное производство
- •2.1 Общая характеристика прокатного производства
- •2.2 Профильный и марочный сортамент прокатной продукции
- •2.3 Сущность процесса прокатки. Характеристики деформации при прокатке
- •2.4 Классификация прокатных станов
- •2.5 Технологические операции при производстве проката
1.2 Кристаллическое строение металлов
В металлах и их сплавах в твердом состоянии элементарные частицы – ато-мы – характеризуются закономерным упорядоченным размещением. Благодаря такому размещению атомы, находящиеся на различных направлениях, можно как бы соединить прямыми линиями. Совокупность таких пересекающихся ли-ний представляет собой своеобразную пространственную решетку, которая при многократном повторении в пространстве воспроизводит объемную или пространственную кристаллическую решетку.
Кристаллические решетки разных металлов отличаются по форме и раз-мерам элементарных ячеек. Различают простые пространственные решетки, в которых атомы размещаются только в узлах решетки (в вершинах основной элементарной ячейки), и сложные пространственные решетки, у которых внутри основных элементарных ячеек также размещены атомы. Для описания строения пространственной решетки обычно выбирают систему координат, в которой осями служат три прямые, проведенные из одной точки, например, узла решетки. Эти прямые совпадают с прямыми, соединяющими атомы.
Самой простой решеткой является кубическая (рисунок 6, а). Элемен-тарную ячейку простой кубической решетки представляет куб, в вершинах ко-торого размещены восемь атомов.
Металлам присущи более сложные типы кубических решеток – объемно-центрированная (ОЦК), гранецентрированная (ГЦК) кубические решетки и гек-сагональная плотноупакованная (ГПУ) (рисунок 6, б, в, г).
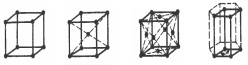
а б в г
а – кубическая; б – объемноцентрированная; в – гранецентрированная; г – гексогональная плотноупакованная
Рисунок 6 – Типы элементарных решеток
Основу ОЦК
составляет кубическая решетка, в
которой атомы нахо-дятся не только в
вершинах куба, но и в его центре, 

 на
пересечении его диа-гоналей.
на
пересечении его диа-гоналей.
В ГЦК ячейкой служит куб с атомами, расположенными не только в вер-шинах куба, но и в центре граней.
В ГПУ ячейка состоит из параллельных центрированных гексагональных оснований.
Показанный на рисунке 6 характер расположения атомов является услов-ным, так как в действительности ионы расположены плотнее, непосред-ственно соприкасаясь друг с другом. Такие решетки и соответствующие им ячейки называются плотноупакованными. Расстояние между ближайшими ато-мами в ячейке называется параметром кристаллической решетки.
Параметры кристаллической решетки имеют величины порядка атомных размеров и измеряются в ангстремах (1А = 10-8 см). В металлах параметры изменяются в пределах 2 – 7 А.
Вышеизложенные рассуждения характерны лишь для монокристалла. Мо-нокристалл – это отдельный кристалл с непрерывной кристаллической ре-шеткой. Реальные металлы состоят из множества кристаллов, форма, размеры и направление кристаллических осей которых зависят от условий кристаллизации и последующей их обработки. Такое строение называется поликрис-таллическим. Взаимное расположение атомов, расстояние между ними, плот-ность их расположения, кристаллические направления и плоскости определя-ют механические и физические свойства кристаллов. Эти свойства вдоль раз-личных кристаллографических направлений и в различных кристаллографи-ческих плоскостях зависят от числа находящихся в них атомов и не явля-ются одинаковыми. Такое явление называется анизотропией свойств. Сле-дует иметь в виду, анизотропия проявляется только в пределах одного моно-кристалла или зерна-кристаллита. В поликристаллических телах, какими яв-ляются реальные металлы, состоящие из огромного количества произвольно ориентированных друг относительно друга зерен, она не наблюдается. Это объясняется тем, что в поликристаллических телах недостаток какого-либо свойства по одному из направлений в одних зернах компенсируется из-бытком данного свойства по этому же направлению в других зернах. Поэтому реальные металлы являются изотропными телами, т.е. телами с одинако-выми свойствами по различным направлениям.
