
- •Биохимические аспекты физических нагрузок
- •Содержание
- •Общий химический состав мышечной ткани
- •Строение эукариотической клетки
- •Скелетные мышцы
- •Б елки мышечного волокна Саркоплазматические белки
- •Миофибрилярные белки
- •Механизм мышечного сокращения
- •Типы мышечных волокон
- •Сердечная мышечная ткань
- •Гладкие мышцы
- •Энергетика мышечного сокращения
- •Доставка кислорода к мышцам и его потребление
- •Классификация физических упражнений
- •Динамика биохимических изменений при утомлении
- •Ведущие факторы утомления при выполнении упражнений различной мощности и интенсивности
- •Биохимия репаративиых процессов в организме после физической нагрузки
- •Детоксикационные системы, их роль в обеспечении физической деятельности
- •Биохимические изменения в организме, происходящие при выполнении упражнений различной мощности и продолжительности в разных видах спорта
- •Биохимические основы нейроэндокринной регуляции обмена веществ во время занятий спортом
- •Зависимость биохимического состояния организма от особенностей нервной деятельности спортсменов
- •Энергообеспечение скоростно-силовых физических нагрузок и адаптация в процессе спортивных тренировок
- •Адаптация или приспособление организма человека к изменяющимся условиям внешней и внутренней среды.
- •Биохимические основы рационального питания спортсменов
- •Влияние биологически активных веществ на работоспособность спортсменов
- •Увеличение мышечной массы. Коррекция компонентного состава тела . Природные анаболики и антикатаболические средства.
- •Биохимический контроль развития систем энергообеспечения организма при мышечной деятельности
- •Биохимический контроль за уровнем тренированности, утомления и восстановления организма
- •Оценка функционального состояния организма и готовности к повышенным нагрузкам
- •Увеличение скорости метаболизма и энергообразования. Активация регуляторных механизмов энергообмена и других метаболических процессов. Энергодающие средства
- •Природные стимуляторы и антидепрессанты
- •Ускорение репаративных процессов
- •Иммуномодуляторы
- •Адаптогены
- •Снижение массы тела
- •Создание мышечного объема
- •Биохимический контроль в спорте
- •Анаболические стероиды (ас)
- •Последствия длительного приема анаболических стероидов на различные органы и системы организма спортсмена Патология печени и желчевыводящих путей
- •Влияние на мочеполовую систему
- •Влияние на эндокринную систему
- •Нарушения функций щитовидной железы и желудочно-кишечного тракта
- •Психические нарушения
- •Влияние на сердечно-сосудистую систему
- •Побочные эффекты действия ас
- •Побочные эффекты действия ас у детей и подростков
- •Допинги нестероидной структуры
- •Допинг-контроль: организация, порядок проведения
- •Задачи, объекты и методы допинг-контроля
- •Организация и проведение допинг-контроля
- •Современные биохимические методы исследований в спорте
- •Терминологический словарь
- •Рекомендованная литература
- •69035, М. Запоріжжя, проспект Маяковського, 26
Сердечная мышечная ткань
Кардиомиоциты (рис. 12), входящие в сердечную мышцу, представлены двумя типами клеток: обычные миоциты, которые во многом схожи с клетками скелетной мышечной ткани и образуют мышцы предсердий и мышцу желудочков и атипичные кардиомиоциты (специальные клетки), обладающие свойством ритмической автоматии и проводимости возбуждения.
Рис. 12. Клетки сердечной мышцы (кардиомиоциты). Тёмным окрашены ядра.
Полное прекращение деления кардиомиоцитов (КМЦ) в сердце млекопитающих в первую неделю постнатальной жизни является неразрешенной загадкой эволюции и не преодолимым препятствием для гистотипической регенерации поврежденного миокарда у человека.
Проводящие сердечные миоциты или атипичные кардиомиоциты, обеспечивают ритмичное координированное сокращение различных отделов сердца. Они способны к генерации и быстрому проведению электрических импульсов. Совокупность атипичных кардиомиоцитов формирует так называемую проводящую систему сердца.
В состав проводящей системы входят:
синусно-предсердный, или синусный, узел;
предсердно-желудочковый узел;
предсердно-желудочковый пучок (пучок Гиса) и
его разветвления (волокна Пуркинье), передающие импульсы на сократительные мышечные клетки.
Различают три типа миоцитов, которые в разных соотношениях находятся в различных отделах проводящей системы сердца.
Первый тип проводящих миоцитов - это P-клетки, или пейсмейкерные миоциты, - водители ритма. Они светлые, мелкие, отросчатые. Эти клетки встречаются в синусном и предсердно-желудочковом узле и в межузловых путях. Они служат главным источником электрических импульсов, обеспечивающих ритмическое сокращение сердца. При слабом развитии саркоплазматической сети высокое содержание свободного кальция в цитоплазме этих клеток обусловливает способность клеток синусного узла генерировать импульсы к сокращению. Поступление необходимой энергии обеспечивается преимущественно процессами анаэробного гликолиза.
Второй тип проводящих миоцитов - это переходные клетки. Они составляют основную часть проводящей системы сердца. Это тонкие, вытянутые клетки, встречаются преимущественно в узлах (их периферической части), но проникают и в прилежащие участки предсердий. Функциональное значение переходных клеток состоит в передаче возбуждения от Р-клеток к клеткам пучка Гиса и рабочему миокарду.
Третий тип проводящих миоцитов - это клетки Пуркинье. Они часто лежат пучками. Они светлее и шире сократительных кардиомиоцитов, содержат мало миофибрилл. Эти клетки преобладают в пучке Гиса и его ветвях. От них возбуждение передается на сократительные кардиомиоциты миокарда желудочков.
Сердечная мышца работает в определенном ритме, чередуя сокращение (систола) около 0,4 сек. и расслабление (диастола) около 0,6 сек. Сердечная мышца за время жизни среднего человека успевает совершать около трёх миллиардов циклов сокращения и расслабления. Работа миокарда не подвластна воле человека и частота сердечных сокращений (ЧСС) регулируется симпатической, парасимпатической нервной системами и гормонально.
При микроскопии с небольшим увеличением видно, что сердечная мышечная ткань представляет собой единую сеть, состоящую из высокоорганизованных сильно ветвящихся и воссоединяющихся вновь мышечных клеток. Эти клетки длиной ~110 мкм и шириной ~15 мкм связаны друг с другом по преимуществу из конца в конец (рис. 13) особыми соединениями – вставочными дисками.
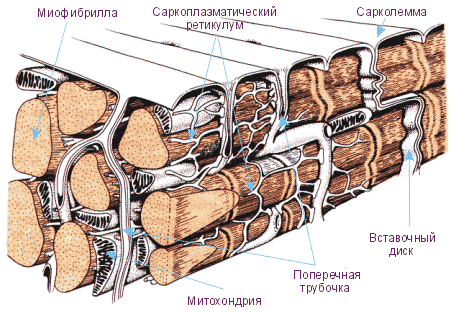
Рис. 13. Строение кардиомиоцита
Важными компонентами каждой клетки кардиомиоцита, обеспечивающими любые её функции, являются внешняя мембрана (сарколемма), система поперечных трубочек, связанных с Z‑дисками, продольный саркоплазматический ретикулум и терминальные цистерны, а также митохондрии (рис. 14). По периферии клетки и между митохондриями находится множество частичек гликоген. Строение главной структуры кардиомиоцита – миофибриллы подобно строению миофибриллы скелетной поперечнополосатой мышечной ткани. Как и скелетная, сердечная мышечная ткань имеет поперечную исчерченность. При большем увеличении видно, что эта исчерченность, также как и в миоцитах скелетной мышечной ткани, обусловлена упорядоченным положением актиновых и миозиновых нитей, собранных в пучки в миофибриллах. Толстые (миозиновые) и тонкие (актин, тропонин и тропомиозин) белковые нити упорядочены в сократительные единицы (саркомеры, простирающиеся от одного до другого Z‑диска) с поперечной исчерченностью, подобной той, что есть в скелетной мышечной ткани. Темные полосы, пересекающие миофибриллы - это соединения отдельных клеток. Их называют вставочными дисками. Они образованы мембранами соседних кардиомиоцитов, образующих сердечное мышечное волокно. Электрическое сопротивление такого соединения составляет ~1/400 сопротивления сарколеммы волокна сердечной мышечной ткани. Через соединение осуществляются хорошо управляемые ионные потоки. Потенциал действия, движущийся по оси одной клетки, легко переходит через вставочный диск на соседний кардиомиоцит.
Эффективное взаимодействие кардиомиоцитов через многочисленные вставочные диски позволяет считать, что сердечная мышечная ткань образует два функциональных синцития: предсердный синцитий и желудочковый синцитий. Хотя морфологическими синцитиями они не являются. Эти функциональные синцитии отделены друг от друга соединительной тканью, окружающей клапанные отверстия. Однако синцитии могут эффективно взаимодействовать друг с другом через специальную проводящую систему (атриовентрикулярный пучок).

Рис. 14. А. Сердечная мышечная ткань.
Б. Сокращение и расслабление миофибрилл происходит в результате изменения концентрации ионов кальция (Са2+) в цитозоле кардиомиоцитов. Ионы кальция входят в расслабления кардиомиоцита. Небольшое количество ионов кальция транспортируется через сарколемму из цитозоля посредством кальций-натриевого насоса и заменяется ионами натрия (Na+). Кальций-натриевый насос имеет меньшее значение в трансмембранных потоках ионов кальция, чем кальциевый насос.
В. Нити актина и миозина вдвигаются друг в друга. Степень перекрытия нитей актина и миозина определяет сокращение и расслабление кардиомиоцитов во время систолы и диастолы.
Г. Глобулярные части (головки) нитей миозина взаимодействуют с нитями актина и обеспечивают скольжение (вдвижение или выдвижение) нитей вдоль их главных осей и сокращение или расслабление кардиомиоцитов.
Возникновение мембранного потенциала кардиомиоцитов обусловлено избирательной проницаемостью их мембраны для ионов калия. Его величина у сократительных кардиомиоцитов составляет 80-90 мВ а у клеток синоатриального узла 60-65 мВ. Возбуждение кардиомиоцитов проявляется генерацией потенциалов действия, которые имеют своеобразную форму. В них выделяются следующие фазы:
1. Фаза деполяризации
2. Фаза быстрой начальной реполяризации
3. Фаза замедленной реполяризации
4. Фаза быстрой конечной реполяризации .
Длительность ПД кардиомиоцитов составляет 200-400 мсек. Это во много раз больше, чем у нейронов или скелетных миоцитов. Амплитуда ПД около 120 мВ. Фаза деполяризации связана с открыванием натриевых и кальциевых каналов мембраны, по которым эти ионы входят в цитоплазму. Фаза быстрой начальной реполяризации обусловлена инактиваиией натриевых, а замедленной кальциевых каналов. Одновременно активируются калиевые каналы. Ноны калия выходят из кардиомиоцитов, развивается фаза быстрой конечной реполяризации. Автоматия, т.е. генерация спонтанных ПД пейсмекерными клетками обусловлена тем, что их мембранный потенциал не остается постоянным. В период диастолы в Р-клетках синоатриального узла происходит его медленное уменьшение. Это называется медленной диастолической деполяризацией МДД . Когда ее величина достигает критического уровня, генерируется ПД, который по проводящей системе распространяется на все сердце. Возникает систола предсердий, а затем желудочков. Медленная диастолическая деполяризация связана с постепенным нарастанием натриевой проницаемости мембраны атипических кардиомиоцитов. Истинными пейсмекерами является лишь небольшая группа Р-клеток синоатриального узла. Остальные Р-клеткн проводящей системы являются латентными водителями ритма. Пока спонтанные ПД поступают из синоатриального узла, латентные пейсмекеры подчиняются его ритму. Это называется усвоением ритма. Но как только проведение нарушается, в них начинают генерироваться собственные спонтанные ПД. Поэтому при некоторых заболеваниях возникает патологическая импульсация в клерках проводящей системы, миокарде предсердий и желудочков. Такие очаги автоматии называют эктопическими т.е. смешенными.
Сокращение кардиомиоцитов, как и других мышечных клеток является следствием генерации ПД. В них как и в скелетных миоцитах, имеется система трубочек саркоплазматического ретикулума содержащих ионы кальция. При возникновении ПД эти ионы выходят из трубочек в саркоплазму. Начинается скольжение миофибрилл. Нов. сокращении кардиомиоцитов принимают участие и ионы кальция, входящие в них в период генерации ПД. Они увеличивают длительность сокращения и обеспечивают пополнение запасов кальция в трубочках.
