
- •Методичні вказівки до виконання лабораторних та самостійних робіт з органічної хімії
- •Лабораторна робота № 9 тема: Ароматичні вуглеводні та їх властивості
- •Хід роботи
- •Контрольні запитання і завдання
- •Лабораторна робота №10 Тема: Феноли та нафтоли. Ароматичні спирти.
- •Хід роботи
- •Контрольні запитання і завдання
- •Лабораторна робота №11
- •Контрольні запитання і завдання
- •Лабораторна робота № 12
- •Хід роботи
- •Лабораторна робота № 13
- •Хід роботи
- •Контрольні запитання і завдання
- •Лабораторна робота №14
- •Хід роботи:
- •Лабораторна робота №15
- •Хід роботи
- •Контрольні запитання і завдання
- •Лабораторна робота № 16
- •Контрольні запитання і завдання
- •Лабораторна робота № 17
- •Хід роботи:
- •Контрольні запитання і завдання
- •Лабораторна робота № 18
- •Хід роботи
- •Контрольні запитання і завдання
Контрольні запитання і завдання
для сомостійної роботи
У яких розчинниках розчиняються ліпіди?
Які функції виконують ліпіди?
Які сполуки належать до ліпідів?
Які властивості характерні для жирних кислот, що входять до складу ліпідів вищих рослин і тварин?
У складі який нейтральний жирів (триацилгліцеролів) є лінолева та ліноленова кислоти (пальмова олія, льняна олія, соняшникова олія, конопляна олія, свиняче сало)?
75
Яка хімічна природа нейтральних жирів (триацилгліцероли, диацилгліцероли, фосфогліцериди, сфінголіпіди, змішані триацилгліцероли)?
Які сполуки є фосфоліпідами (кефалін, лецитин, фосфатидилсерин, спермацет, ланолін?
Яка хімічна структура воску (ацилгліцероли, ефіри вищих жирних кислот і моноокисиспиртів з довгим ланцюгом, стероїди, фосфогліцерини, гліколіпіди)?
Які сполуки є стероїдами (жовчні кислоти, гормони надниркових залоз, гангліозиди, статеві гормони, сфінгомієліни)?
Які вітаміни належать до ліпоїдів (вітамін С, вітамін К, вітамін А, вітамін Е, вітамін Д)?
76
Лабораторна робота № 18
ТЕМА: Визначення хімічних параметрів жирів.
Основні теоретичні відомості
Складні ліпіди.
1. Фосфатиди (фосфоліпіди) - естери, молекули яких утворено залишками спиртів (гліцерину, інозиту, сфінгозину), ВЖК (насиченими і ненасиченими), ортофосфорної кислоти і нітрогенної основи. Разом з білками складають хімічну основу біомембран клітин.
Молекула фосфатиду складається з гідрофільної (полярної) і гідрофобної (неполярної) частин. Гідрофільна «голова» має негативний заряд фосфату і позитивний - нітрогену, і є перманентним диполем (цвітер-йоном). Гідрофобний «хвіст» складається з довгих ланцюгів залишків ВЖК. Це зумовлює поверхнево-активні властивості ліпіду, дає можливість формувати плівкові структури у моношарі на межі розділу фаз, взаємодіяти з різними (полярними і неполярними) сполуками. Фосфатидами багаті нервова тканина (26-30%), печінка (16%). За природою спиртових залишків розрізняють такі групи фосфатидів: гліцерофосфатиди, інозит фосфатиди, сфінгозитфосфатиди.
2. Гліколіпіди - складні ліпіди, молекули яких побудовано з ліпідного і вуглеводного фрагментів, що з'єднанні між собою ковалентним зв'язком. Розрізняють такі групи гліколіпідів: глікосфінголіпіди; глікозилдигліцериди; глікозиди жирних гідроксикислот; естери жирних кислот і цукрів; фосфоровмісні гліколіпіди – глікозиди фосфорогліцеридів і фосфосфінголіпідів. Гліколіпіди - складові частини біомембран клітин. Типовим гліколіпідом є нервон - цереброзид нервової тканини людини і тварин:
77
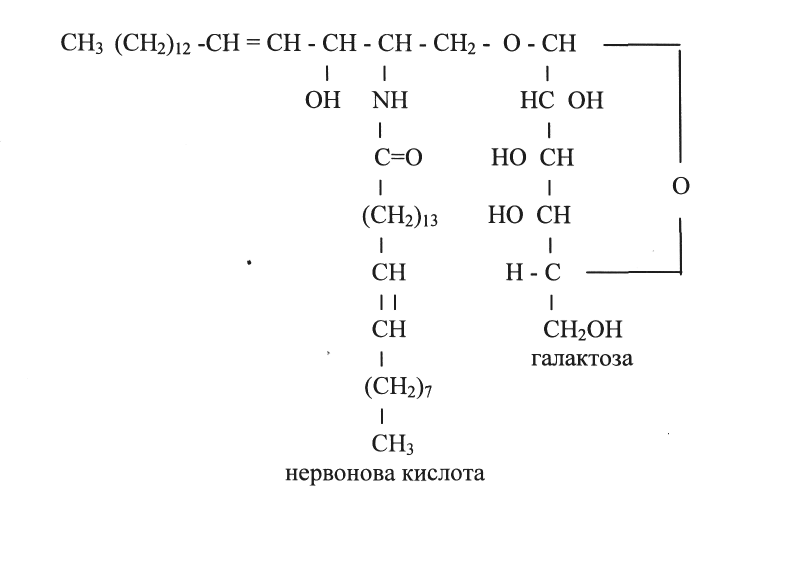

78
Хід роботи
ДОСЛІД 1. Визначення кислотного числа жиру.
Обладнання та реактиви: спирт, нейтралізований за фенолфталеїном, розчин КОН (0,1 моль/л), 0,1%-й розчин фенолфталеїну, жир, конічні колби об'ємом 50мл, піпетки.
До 1г жиру додають 5мл спирту, перемішують для максимального розчинення вільних жирних кислот і титрують розчином КОН до появи рожевого забарвлення (забарвлення не повинно зникати протягом 0,5 – 1 хв.).
Кількість КОН, мг, витрачену на титрування вільних жирних кислот, що містяться в 1г жиру, визначають за формулою:
KЧ=AζQ/a,
де А - об'єм розчину КОН (0,1 моль/л), витрачений на титрування досліджуваної проби, мл;
а - наважка жиру, г;
ζ - коефіцієнт поправки на титр розчину КОН (0,1 моль/л); Q - кількість КОН (5,61мг), еквівалентна 1 мл розчину КОН (0,1моль/л).
Висновки: кислотністю жиру, або кислотним числом (КЧ), називають кількість КОН, мг, яка потрібна для нейтралізації вільних жирних кислот, що містяться в 1г жиру.
ДОСЛІД 2. Визначення йодного числа жиру.
Обладнання реактиви: жир; спиртовий розчин йоду (0,1моль/л); 1%- й розчин крохмалю, розчин Na2 S2O3 (0,05моль/л); дві конічні колби об'ємом 50 мл; піпетки.
В одну колбу (досліджувана проба) вносять наважку жиру 0,1-0,2г, у другу воду (контрольна проба) - 0,1-0,2мл води, додають по 10 мл спиртового розчину йоду, перемішують і залишають на 15хв. Далі вміст колб титрують розчином Na2 S2O3 до появи жовтуватого забарвлення. Потім, додавши 1 мл
79
розчину крохмалю, суміш титрують до зникнення синього забарвлення.
Йодне число визначають за формулою:
ЙЧ=(В-А)* ζ *Q-100/a*1000
де (В-А) - різниця результатів титрування контрольного та досліджуваного зразків у розчині гіпосульфіту (0,05моль/л), мл;
а - наважка досліджуваного жиру, г;
q - коефіцієнт поправки на титр розчину Na2 S2O3 (0,05моль/ л);
Q - кількість І2 (12,69 мг), еквівалентна 1 мл розчину Na2 S2O3 (0,05моль/л).
ХІМІЗМ:
R-CH=CH-R'+12 + Н2О → R-CH-CH-R1 + HI
│ │
І ОН
ВИСНОВКИ: йодним числом (ЙЧ) називають кількість йоду, г, яка може прореагувати з 100г жиру. Це число відповідає кількості ненасичених жирних кислот у жирі.
ДОСЛІД 3. Визначення пероксидного числа в згірклому жирі.
Обладнання та реактиви: жир; насичений розчин КІ; хлороформ; розчин Na2S2O3 (0,005моль/л); 1%-й розчин крохмалю; льодяна оцтова кислота; дві конічні колби об'ємом 50мл; піпетки.
В одну колбу (досліджувана проба) вносять наважку жиру (1 г), у другу (контрольна проба) – 1 мл води, додають 5мл льодяної оцтової кислоти, по 6 мл хлороформу та по 1 мл насиченого розчину КІ, струшують 5 хв і титрують розчином Na2 S2O3 за наявності 10 краплин розчину крохмалю як індикатора. Пероксидне число, тобто кількість 0,005моль/л розчину Na2 S2O3 мл, витрачена на титрування 1г жиру, дорівнює:
80
C=(A-B)ζ
де (А-В) - різниця результатів титрування досліджуваного та контрольного зразків розчином Na2 S2O3 (0,005 моль/л);
ζ - коефіцієнт поправки на титр розчину Na2 S2O3 (0,005 моль/л);
Хімізм:

ДОСЛІД 4. Якісні реакції на холестерин.
Обладнання та реактиви: хлороформний розчин холестеролу (2-3кристали
розчиняють у 2-3 мл хлороформу); концентрована сульфатна кислота; оцтовий альдегід і штатив з пробірками; фарфорова чашка; піпетки.
A.Реакція Шиффа. У пробірку вносять 1 мл холестеролу в хлороформі. По стінці пробірки доливають 1 мл H2SO4 (конц). На межі розділу кислоти та розчину холестеролу утворюється кільце червоного кольору.
Б. Реакція Сальковського. У пробірку з 0,5мл розчину холестеролу, додають 0,5мл Н2SО4 (конц.) і струшують. Після розшарування фаз спостерігають за зміною забарвлення: верхній шар, що містить холестерол, забарвлюється в пурпурно-червоний колір, а нижній (шар сульфатної кислоти) - в темно-червоний колір із зеленою флуоресценцією.
81
Розчин холестеролу зливають у фарфорову чашку. Забарвлення розчину з часом змінюється на фіолетове, потім зелене й, нарешті, жовте.
В. Реакція Лібермана - Бурхарда. У пробірку з 1 мл розчину холестеролу додають 2-Змл оцтового ангідриду й дві краплини концентрованої Н2SО4. Пробірку струшують і спостерігають утворення червоного забарвлення, яке переходить у червоно- фіолетове, фіолетове, синє і, нарешті, в зелене.
Висновки: Реакції якісного виявлення холестеролу ґрунтується на його здатності перетворюватися з вторинного спирту в ненасичений вуглеводень. За наявності сульфатної кислоти відбувається дегідратація та окиснення холестерину. Внаслідок цього дві молекули холестеролу сполучаються між собою за третім атомом карбону. Утворенні ненасичені вуглеводні з спряженими подвійними зв’язками формуються різні похідні з сульфатною кислотою та оцтовим ангідридом.
