
- •Введение техническая термодинамика как теоретическая основа теплоэнергетики
- •1. Общие определения и понятия
- •1.1. Термодинамическая система
- •1.2. Термодинамические параметры состояния
- •Основные термические параметры состояния
- •Удельный объем
- •Давление
- •Соотношения единиц измерения давления
- •Температура
- •1.3.2. Уравнение состояния термодинамической системы
- •1.3.3. Термические коэффициенты
- •1.3.4. Термодинамический процесс
- •2. Первый закон термодинамики для закрытой системы
- •2.1. Работа изменения объема
- •2.2. Теплота, теплоемкость, энтропия
- •2.3. Внутренняя энергия
- •2.4. Первый закон термодинамики для закрытой системы
- •2.4.1. Аналитические выражения первого закона термодинамики.
- •2.4.2. Энтальпия
- •3. Газы и газовые смеси
- •3.1. Законы идеальных газов
- •3.1.1. Внутренняя энергия идеального газа
- •3.1.2. Теплоемкости газов
- •Удельные теплоемкости
- •Теплоемкости процессов
- •Теплоемкости идеальных газов
- •Теплоемкость реальных газов
- •Отношение изобарной и изохорной теплоемкостей
- •3.1.3. Энтальпия идеальных газов
- •3.1.4. Энтропия идеальных газов
- •3.2. Газовые смеси
- •Основные характеристики смеси газов
- •Теплоемкости газовых смесей
- •4. Газовые процессы
- •4.1. Политропные процессы
- •4.2. Частные случаи политропных процессов
- •Уравнения процессов, расчетные выражения их теплоты, работы, изменения внутренней энерги, энтальпии и энтропи
- •4.3. Изображение политропных процессов в р,V и t,s- диаграммах Политропа в р,V- диаграмме
- •Политропа в t,s- диаграмме
- •4.4. Установление показателя политропы по опытным данным
- •4.5. Качественный и количественный анализ политропных процессов в р,V- и t,s- диаграммах
- •4.6. Определение термодинамических свойств идеальных газов с учетом влияния температуры на их изобарную и изохорную теплоемкости
- •Определение энергетических параметров идеальных газов с учетом влияния температуры на cp и cv
Теплоемкости газовых смесей
Полная теплоемкость смеси газов представляет собой сумму теплоемкостей газов, составляющих смесь. Это справедливо, поскольку теплота подчиняется закону суммирования (адитивности).
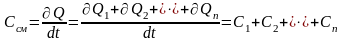 .
(3.79)
.
(3.79)
Удельную массовую теплоемкость смеси газов можно получить, разделив выражение (3.79) на массу смеси газов и выразив полные теплоемкости каждого газа через произведение их масс на соответствующие им удельные массовые теплоемкости:

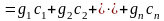 .
.
Получили, что удельная массовая теплоемкость смеси газов равна сумме произведений массовых долей на удельные массовые теплоемкости газов, составляющих смесь:
 .
(3.80)
.
(3.80)
Удельную объемную теплоемкость смеси газов можно получить, разделив выражение (3.79) на объем смеси и выразив полные теплоемкости каждого газа в виде произведения их парциальных объемов на соответствующие им удельные объемные теплоемкости:

 .
.
И спользование
парциальных объемов правомерно (рис.3.4),
поскольку они соответствуют массовому
количеству каждого газа, входящему в
смесь, т.е. количество теплоты можно
представить выражением
спользование
парциальных объемов правомерно (рис.3.4),
поскольку они соответствуют массовому
количеству каждого газа, входящему в
смесь, т.е. количество теплоты можно
представить выражением

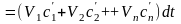 .
.
Получили, что удельная объемная теплоемкость смеси газов равна сумме произведений объемных долей на удельные объемные теплоемкости газов, составляющих смесь:
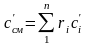 .
(3.81)
.
(3.81)
Удельную мольную теплоемкость смеси газов можно получить, умножив выражение (3.81) на объем одного киломоля, поскольку по закону Авогадро объем одного киломоля всех идеальных газов при одинаковых параметрах одинаков (Vcм=V1=V2==Vn):

 .
.
Получили, что удельная мольная теплоемкость смеси газов равна сумме произведений объемных долей на удельные мольные теплоемкости газов, составляющих смесь:
 .
(3.82)
.
(3.82)
Для простоты запоминания расчетных выражений характеристик смеси идеальных газов можно воспользоваться следующей закономерностью: все характеристики смеси газов, которые рассчитываются в виде суммы произведений характеристик отдельных газов на их доли, имеют в расчетных выражениях массовые доли, если характеристика в знаменателе имеет единицу измерения массы килограмм (кг), во всех остальных случаях их характеристики умножаются на объемные доли.
Например, единица измерения газовой постоянной смеси Rсм (Дж/(кгК)) – она рассчитывается в виде алгебраической суммы произведений газовых постоянных Ri на массовые доли ее компонентов gi, т.к. в знаменателе ее единицы измерения находится килограмм (кг).
4. Газовые процессы
Термодинамическим газовым процессом называется процесс изменения состояния газа, при котором происходит энергетическое взаимодействие газа и окружающей среды в виде теплоты и работы, в результате чего происходит изменение параметров газа.
В термодинамике рассматриваются закономерные процессы. Закономерность процесса может быть выражена закономерным энергетическим взаимодействием газа и окружающей среды. Следствием такого энергетического взаимодействия будет закономерное изменение параметров газа [8].
