- •Оглавление.
- •Введение.
- •Аминокислоты.
- •Структура белков
- •Конформация белков
- •Тема: пептиды, белки: их строение, свойства, значение в организме, методы исследования. Физико-химические свойства белков. Пептиды
- •Роль белков в организме человека
- •Методы разделения белков и пептидов:
- •Признаки коллоидного состояния:
- •Сходство растворов вмс и коллоидных растворов:
- •Отличие растворов вмс от коллоидных растворов:
- •Сходство растворов вмс с ионно-молекулярными растворами:
- •Специфические свойства растворов вмс:
- •Анализ мембранного равновесия Доннана
- •Ферменты
- •Отличие ферментов от неорганических катализаторов
- •Строение ферментов
- •Активный центр ферментов.
- •Механизм действия ферментов
- •Специфичность
- •Кинетика ферментативных реакций
- •2. Концентрация субстрата
- •РН среды
- •Активирование ферментов
- •6. Ингибирование.
- •Определение активности фермента
- •Классификация ферментов
- •Трансферазы
- •Гидролазы
- •Изомеразы
- •Лигазы (синтетазы)
- •Тема: ферменты, как биологические катализаторы
- •Классификация ферментов
- •Свойства ферментов
- •Специфичность действия ферментов
- •Активирование и ингибирование ферментов
- •Регуляция путём ковалентной модификации
- •Путь нековалентной модификации
- •Типы ингибирования
- •Конкурентное ингибирование
- •Неконкурентное ингибирование
- •Регуляция путем изменения биосинтеза ферментов
- •Компартментализация (отделение, отсек) в клетке
- •Изоферменты
- •Анализ уравнения Михаэлиса—Ментен:
- •Количественная характеристика активности фермента
- •Количественная характеристика активности ферментов в биологических жидкостях
- •Энзимодиагностика
- •Наследственные нарушения (энзимопатии)
- •Энзимотерапия
- •Липиды. Классификация липидов. Характеристика фосфолипидов и восков.
- •Обмен липидов
- •Ресинтез жирных кислот в стенке кишечника.
- •Транспорт липидов
- •Цикл трикарбоновых кислот (цикл Кребса)
- •Тема углеводы
- •Классификация углеводов
- •Моносахариды.
- •Стериоизомерия моносахаридов.
- •Циклические (полуацетальные) формы моносахаридов.
- •Основные реакции моносахаридов.
- •1. Реакции полуацетального гидроксила.
- •3. Реакции с участием карбонильной группы.
- •Олигосахариды
- •Полисахариды
- •Гетерополисахариды.
- •Промежуточный обмен углеводов в организме
- •Витамины
- •Классификация витаминов
- •Жирорастворимые витамины Витамины группы а (ретинол, антиксерофтальмический)
- •Биологическая роль
- •Витамины группы к (филлохиноны, менахиноны,антигеморрагический)
- •Витамины группы е (токоферол, антистерильный. Витамин размножения)
- •Водорастворимые витамины Витамин в1 (тиамин, антиневрический)
- •Биологическая роль
- •Витамин в2 (рибофлавин, витамин роста)
- •Витамин в6 (пиридоксин, антидермический)
- •Витамин в12 (кобаламин,антианемический)
- •Витамин с (аскорбиновая кислота, антискорбутный витамин).
- •Витамин р (рутин, цитрин, витамин проницаемости)
- •Витамин рр (никотиновая кислота, никотинамид, ниацин, антипеллагрический)
- •Авитаминоз и гиповитаминоз
- •Химия нуклеиновых кислот. Общая характеристика нуклеиновых кислот
- •Химическое строение рнк и днк.
- •Азотистое основание Углеводный компонент Фосфорная кислота
- •П уриновые Пиримидиновые Рибоза Дезоксирибоза
- •Углеводный компонент
- •Азотистое основание
- •Структура нуклеиновых кислот.
- •Вторичная структура днк характеризуется правилом э. Чаргаффа (закономерность количественного содержания азотистых оснований):
- •Тема: обмен нуклеиновых кислот и нуклеотидов в организме человека.
- •Этапы репликации:
- •Транскрипция
- •Этапы транскрипции:
- •Биосинтез белка
- •Регуляция транскрипции. Теория Оперона
- •Тема: энергетический обмен. Цикл лимонной кислоты - цикл трикарбоновых кислот (цтк), цикл Кребса - конечный общий путь окисления белков, липидов, углеводов.Цтк - амфиболический цикл.
- •Цикл лимонной кислоты — цтк — цикл Кребса
- •Энергетическая роль цтк
- •Регуляция цикла Кребса
- •Биоэнергетика. Биологическое окисление Роль кислорода в метаболизме
- •Токсичность кислорода
- •Макроэргические молекулы
- •Нуклеозидтрифосфаты
Макроэргические молекулы
К макроэргическим относятся соединения, при гидролизе которых выделяется энергия не менее 7 ккал/моль. Это число — условная единица, означающая всего лишь некий уровень отсчета, согласно которому АТФ и несколько других соединений отличаются от остальных природных соединений. Соответственно название «макроэргический» употребляется для объединения соединений в группу веществ макроэргических и для указания их особой важности в переносе энергии в живой клетке.
Нуклеозидтрифосфаты
Наиболее распространенными
высокоэнергетическими общими
промежуточными продуктами являются
нуклеозидтрифосфаты (НТФ), которые
могут передавать свою концевую
высокоэнергетическую фосфатную группу
любой из многочисленных органических
молекул - акцепторов (чаще всего энергия
образуется в виде АТФ). Особ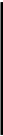 енность
высокоэнергетических нуклеотидов
состоит в том, что они выступают в
качестве универсального источника
энергии для большого числа энергозависимых
реакций.
енность
высокоэнергетических нуклеотидов
состоит в том, что они выступают в
качестве универсального источника
энергии для большого числа энергозависимых
реакций.
Молекула АТФ состоит из аденилатной группы и трех остатков фосфорной группы. Значительная часть свободной энергии этой молекулы обусловлена взаимным электростатическим отталкиванием этих фосфатных остатков аналогично взаимному отталкиванию одноименно заряженных зарядов. Разрыв связей между остатками фосфорной кислоты сопровождается освобождением энергии. Соединением, играющим наиболее важную роль в клеточной энергетике, является АТФ, так как:
Химическая энергия запасается путем образования АТФ, сопряженного с катаболическими реакциями расщепления.
Затем химически энергия утилизируется путем расщепления АТФ, сопряженного с эндэргическими реакциями синтеза в ходе анаболизма и других процессов, требующих затрат энергии, например активного транспорта и сокращения мышц.
Гидролиз АТФ — термодинамическая движущая сила процессов, которые сами по себе являются термодинамически невыгодными.
АТФ и другие нуклеозидтрифосфаты ответственны за перенос энергии во многих сопряженных реакциях. АТФ — постоянный источник энергии для клетки. Он мобилен и может доставлять химическую энергию в любую часть клетки. Когда клетка нуждается в энергии, единственное, что потребуется для ее получения, — это гидролиз АТФ. АДФ может быть рефосфорилирован в АТФ в результате дыхательной активности или за счет другого высокоэнергетического соединения, например, креатинфосфата, присутствующего в мышечных клетках. Если весь АДФ мышечной ткани превращается в АТФ, то фосфат от АТФ переносится на креатин с образованием креатинфосфата. При этом вновь появляется некоторое количество АДФ, который может, присоединив фосфат, образовать АТФ. При понижении уровня АТФ происходит обратный процесс: фосфат переносится от креатинфосфата на АДФ, и запасы АТФ восстанавливаются.
Таким образом, АТФ играет важную метаболическую роль благодаря своему центральному положению в клеточной активности. Он действует как связующее клеточное звено между дыханием и процессами, требующими затраты энергии. При этом его высокоэнергетические фосфатные группы непрерывно отщепляются и замещаются новыми.
Аргининфосфат и креатинфосфат выполняют роль своеобразных аккумуляторов химической энергии, которые используются для быстрого фосфорилирования АТФ во время энергичного мышечного сокращения. Их называют фосфагенами.
Ацилфосфаты — макроэргические соединения с ангидридной связью, в которых карбонильный атом углерода ацильной группы особенно легко участвует в реакции с нуклеофилами. Значение G = -12,8 ккал/моль.
Например, глицеро-1,3-дифосфат + НОН глицеро-3-фосфат + Н3РО4.
Тиоэфиры играют очень важную роль в метаболизме в качестве метаболически активной формы ацильной группы. В природе основными тиолсодержащими соединениями являются: кофермент А, липоевая кислота, белки с -SH группой:
ацетил-КоА + НОН ацетат + HSKoA;
G = -7,37 ккал/моль.
Восстановленные формы НАДН + Н+ и НАДФН + Н+, будучи синтезированными в клетке, затем вновь окисляются, при этом происходит перенос электронов на кислород. Этот способ используется в качестве основного способа, посредством которого клетка превращает химическую энергию поступивших извне питательных веществ в утилизируемую метаболическую энергию.
С тандартная
энергия гидролиза некоторых соединений
тандартная
энергия гидролиза некоторых соединений
G, ккал/моль
Нуклеозидтрифосфаты —7,3
1,3-Дифосфоглицерат —11,8
Фосфоенолпируват —14,8
Ацилтиоэфиры —7,37
Креатинфосфат —10,3
Восстановленные эквиваленты (при окислении):
НАДН + Н+; НАДФН + Н+ —52,6
Структура макроэргических соединений
НТФ, например ГТФ:
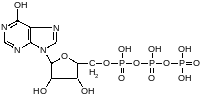
1,3-Дифосфоглицерат:
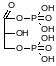
Фосфоенолпируват:
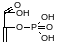
Ацилтиоэфиры:
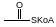
Восстановленные эквиваленты, например ФМН-Н2:
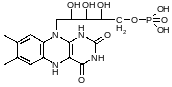
Креатинфосфат: