
- •Оглавление.
- •Введение.
- •Аминокислоты.
- •Структура белков
- •Конформация белков
- •Тема: пептиды, белки: их строение, свойства, значение в организме, методы исследования. Физико-химические свойства белков. Пептиды
- •Роль белков в организме человека
- •Методы разделения белков и пептидов:
- •Признаки коллоидного состояния:
- •Сходство растворов вмс и коллоидных растворов:
- •Отличие растворов вмс от коллоидных растворов:
- •Сходство растворов вмс с ионно-молекулярными растворами:
- •Специфические свойства растворов вмс:
- •Анализ мембранного равновесия Доннана
- •Ферменты
- •Отличие ферментов от неорганических катализаторов
- •Строение ферментов
- •Активный центр ферментов.
- •Механизм действия ферментов
- •Специфичность
- •Кинетика ферментативных реакций
- •2. Концентрация субстрата
- •РН среды
- •Активирование ферментов
- •6. Ингибирование.
- •Определение активности фермента
- •Классификация ферментов
- •Трансферазы
- •Гидролазы
- •Изомеразы
- •Лигазы (синтетазы)
- •Тема: ферменты, как биологические катализаторы
- •Классификация ферментов
- •Свойства ферментов
- •Специфичность действия ферментов
- •Активирование и ингибирование ферментов
- •Регуляция путём ковалентной модификации
- •Путь нековалентной модификации
- •Типы ингибирования
- •Конкурентное ингибирование
- •Неконкурентное ингибирование
- •Регуляция путем изменения биосинтеза ферментов
- •Компартментализация (отделение, отсек) в клетке
- •Изоферменты
- •Анализ уравнения Михаэлиса—Ментен:
- •Количественная характеристика активности фермента
- •Количественная характеристика активности ферментов в биологических жидкостях
- •Энзимодиагностика
- •Наследственные нарушения (энзимопатии)
- •Энзимотерапия
- •Липиды. Классификация липидов. Характеристика фосфолипидов и восков.
- •Обмен липидов
- •Ресинтез жирных кислот в стенке кишечника.
- •Транспорт липидов
- •Цикл трикарбоновых кислот (цикл Кребса)
- •Тема углеводы
- •Классификация углеводов
- •Моносахариды.
- •Стериоизомерия моносахаридов.
- •Циклические (полуацетальные) формы моносахаридов.
- •Основные реакции моносахаридов.
- •1. Реакции полуацетального гидроксила.
- •3. Реакции с участием карбонильной группы.
- •Олигосахариды
- •Полисахариды
- •Гетерополисахариды.
- •Промежуточный обмен углеводов в организме
- •Витамины
- •Классификация витаминов
- •Жирорастворимые витамины Витамины группы а (ретинол, антиксерофтальмический)
- •Биологическая роль
- •Витамины группы к (филлохиноны, менахиноны,антигеморрагический)
- •Витамины группы е (токоферол, антистерильный. Витамин размножения)
- •Водорастворимые витамины Витамин в1 (тиамин, антиневрический)
- •Биологическая роль
- •Витамин в2 (рибофлавин, витамин роста)
- •Витамин в6 (пиридоксин, антидермический)
- •Витамин в12 (кобаламин,антианемический)
- •Витамин с (аскорбиновая кислота, антискорбутный витамин).
- •Витамин р (рутин, цитрин, витамин проницаемости)
- •Витамин рр (никотиновая кислота, никотинамид, ниацин, антипеллагрический)
- •Авитаминоз и гиповитаминоз
- •Химия нуклеиновых кислот. Общая характеристика нуклеиновых кислот
- •Химическое строение рнк и днк.
- •Азотистое основание Углеводный компонент Фосфорная кислота
- •П уриновые Пиримидиновые Рибоза Дезоксирибоза
- •Углеводный компонент
- •Азотистое основание
- •Структура нуклеиновых кислот.
- •Вторичная структура днк характеризуется правилом э. Чаргаффа (закономерность количественного содержания азотистых оснований):
- •Тема: обмен нуклеиновых кислот и нуклеотидов в организме человека.
- •Этапы репликации:
- •Транскрипция
- •Этапы транскрипции:
- •Биосинтез белка
- •Регуляция транскрипции. Теория Оперона
- •Тема: энергетический обмен. Цикл лимонной кислоты - цикл трикарбоновых кислот (цтк), цикл Кребса - конечный общий путь окисления белков, липидов, углеводов.Цтк - амфиболический цикл.
- •Цикл лимонной кислоты — цтк — цикл Кребса
- •Энергетическая роль цтк
- •Регуляция цикла Кребса
- •Биоэнергетика. Биологическое окисление Роль кислорода в метаболизме
- •Токсичность кислорода
- •Макроэргические молекулы
- •Нуклеозидтрифосфаты
Изомеразы
Систематическое название ферментов этого класса образуют по схеме: субстрат-тит реакции изомеризации-изомераза. При внутримолекулярном переносе групп ферменты имеют тривиальные названия мутызы.Катализируют различные реакции изомеризации (90 ферментов). Например превращение глюкозы-6-фосфат во фруктозу –6-фосфат.
CH2O- РО3Н2 CH2O- РО3Н2
O
O

O
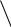 ОН
ОН
ОН ОН глюкозофосфат- ОН CH2OН
ОН изомераза
ОН
α-глюкоза-6-фосфат β-фруктоза-6-фосфат
CH2O- РО3Н2 CH2OН
O

ОН ОН фосфоглюкомутаза
ОН O- РО3Н2
ОН ОН
Глюкоза-6-фосфат глюкоза-1-фосфат
Мутаротаза осуществляет взаимные превращения α- и β- изомеров.
Лигазы (синтетазы)
Систематическое название образуется по схеме: А : В лигаза (образующая АДФ), где А и В – соединяющиеся молекулы, в скобках указывается продукт расщепления нуклеозидтрифосфата, который использовался в данной реакции. Делятся на подклассы, ускоряющие реакции синтеза различных связей.
а). С-С-лигазы. Представителями лиаз, образующих С-С-связи, являются карбоксилазы, вызывающие удлинение углеродных цепей.
Например, пируваткарбоксилаза:
CН3 СООН
С О + CO2 + АТФ СН2 + АДФ + Фн
СООН С= О
СООН
ПВК оксилоацетат
б). С-О-лигазы. Такой тип связи возникает при действии аминоацил-тРНК-синтетаз, активирующих аминокислоты и передающих их на т-РНК:
АТФ АМФ + ФФн
R -CH-COOH + тРНК R-CH-CO~тРНК
NH2 NH2
в). С-N-лиазы.Эти ферменты участвуют, например, в синтезе различных амидов. К ним относится аспарагинсинтетаза.
NH2
СООН С=О
C H2 NH3 АТФ АДФ + Фн CH2
С Н-NH2 СН-NH2
COOH COOH
Асп. Асн.
Тема: ферменты, как биологические катализаторы
Ферменты – биологические катализаторы белковой природы. Синтезируются клетками организма. Некоторые клетки могут содержать до 1000 различных ферментов. За последние 50 лет из всех типов организмов удалось выделить 2500 ферментов. Из них удалось получить в кристаллическом виде, а для 50 ферментов с помощью рентгено-структурного анализа определена трехмерная пространственная структура.
