
- •1.2 Роль і значення промивання свердловин та промивальних рідин в процесі буріння свердловин
- •1.3 Основні функції промивальних рідин
- •1.3.1 Гідродинамічні функції
- •1.3.2 Гідростатичні функції
- •1.3.3 Функції кіркоутворення
- •1.3.4 Фізико-хімічні функції
- •1.3.5 Різнобічні функції промивальної рідини
- •1.4 Класифікація дисперсних систем
- •1.5 Процеси на межі розділу фаз у дисперсних системах
- •2.2 Компонентний склад бурових промивальних рідин
- •2.3 Особливості будови та складу основних глинистих мінералів
- •2.3.1 Глини групи монтморилоніту
- •2.3.2 Глини групи гідрослюд
- •2.3.3 Глини групи каолініту
- •2.3.4 Глини групи палигорскіту
- •2.4 Катіонний обмін у глинистих суспензіях. Обмінна ємкість глинистих мінералів
- •3.2 Вплив мінерального складу глин і типу обмінних катіонів на гідратацію, диспергування і бубнявіння глинистих мінералів
- •3.3 Будова глинистих частинок у водній суспензії. Теорія Штерна і будова деш. Дзета ( ) – потенціал і його вплив на властивості бпр
- •3.4 Агрегатна та седиментаційна стійкість колоїдних розчинів. (Стійкість дисперсних систем)
- •3.5 Явище коагуляції та колоїдний захист у глинистих суспензіях
- •4.2 Визначення якості глинопорошків
- •4.3 Розрахунки при приготуванні глинистих розчинів
- •5.2 Типи обважнювачів і їх характеристика
- •5. 2.1 Баритові обважнювачі
- •5.2.2 Карбонатні обважнювачі
- •5.2.3 Залізисті обважнювачі
- •5.2.4 Свинцеві обважнювачі
- •5.3 Вплив обважнювачів на структурно-механічні властивості бурових розчинів
- •Різної густини
- •1, 2, 3 І 4 густини обважнювачів відповідно 3000 кг/м3, 3500 кг/м3;
- •5.4 Методи обважнення бурових розчинів
- •Розчин у вигляді пульпи
- •5.5 Розрахунки при обважненні бурових розчинів
- •6.2 Реологічні властивості бурових промивальних рідин
- •Напруження зсуву відповідного градієнта швидкості
- •6.3 Степеневий закон
- •Лекція № 7 тіксотропні властивості бурових промивальних рідин
- •7.1 Поняття про механізм структуроутворення
- •Частинками розчину в момент структуроутворення
- •7.2 Типи структур в дисперсних системах і їх видозміни у буровому розчині
- •7.4 Статичне напруження зсуву бурових розчинів і методи його визначення
- •7.5 Методи та прилади для заміру снз
- •Лекція № 8 фільтраційні і кіркоутворюючі властивості бурових розчинів
- •8.1 Основні положення статичної фільтрації
- •8.2 Статична та динамічна фільтрація бурових промивальних рідин
- •8.3 Вплив основних факторів на статичну та динамічну фільтрацію
- •8.4 Фільтраційна кірка бурового розчину
- •8.4.1 Товщина фільтраційної кірки
- •На товщину фільтраційної кірки
- •8.4.2 Проникність фільтраційної кірки
- •Густина бурового розчину та її значення в процесі буріння свердловин. Вміст газу у буровому розчині
- •9.1 Вибір густини бурового розчину
- •9.2 Регулювання густини бурового розчину в процесі буріння
- •Швидкість буріння
- •9.3 Вміст газу у бурових промивальних рідинах
- •Лекція № 10
- •10.2 Шлам, як колоїдний компонент бурового розчину
- •10.3 Вплив вмісту твердої фази на властивості бурового розчину
- •11.1 Класифікація хімічних реагентів
- •Лекція № 12 вода і суспензії із вибурених порід
- •12.1 Призначення та умови застосування
- •12.2 Склад і властивості суспензій із вибурених порід
- •12.3 Технологія приготування
- •12.4 Перевід в інші типи розчинів
- •12.5 Вплив на наступні технологічні процеси
- •13.2 Склад та властивості гуматних бурових розчинів
- •Гуматнокальцієві розчини
- •13.3 Технологія застосування
- •13.4 Контроль властивостей розчину в процесі буріння
- •13.5 Перевід в інші типи розчинів
- •13.6 Вплив гуматних розчинів на наступні технологічні процеси
- •Лекція № 14 лігносульфатні бурові розчини
- •14.1 Призначення та умови застосування лігносульфатних бурових розчинів
- •14.2 Склад та властивості бурового розчину
- •14.3 Технологія застосування
- •14.4 Регулювання властивостей бурового розчину
- •14.6 Вплив розчину на наступні технологічні операції
- •14.5 Перевід в інші типи розчинів
- •Лекція № 15 полімер-глинисті бурові розчини
- •15.1 Призначення та умови застосування полімер-глинистих бурових розчинів
- •15.2 Склад та властивості бурового розчину
- •15.3 Технологія застосування бурового розчину
- •Лекція № 16 хлоркальцієві бурові розчини
- •16.1 Призначення та умови застосування
- •16.2 Склад і граничні значення показників властивостей
- •Густина 10602200 залежно від вмісту глини та обважнювача. В дужках дані взаємозамінні матеріали
- •16.3 Технологія приготування
- •16.4 Регулювання властивостей розчину
- •16.5 Перевід в інші типи розчинів
- •16.6 Вплив розчину на наступні технологічні операції
- •Лекція №17 Застосування гіпсо-калієвого бурового розчину
- •17.1 Призначення розчину і умови застосування
- •17.2 Склад і граничні значення показників властивостей
- •17.3. Технологія приготування
- •17.4 Регулювання властивостей розчину
- •17.5. Перевід в інші типи розчинів
- •17.6. Вплив розчину на наступні технологічні операції
- •Хлоркалієві бурові розчини
- •18.1. Призначення та умови застосування
- •18.2. Склад і допустимі показників властивостей
- •18.3. Технологія приготування
- •Контроль властивостей у процесі буріння
- •18.5 Перехід до інших типів розчинів
- •18.6 Вплив розчину на наступні технологічні операції
- •Лекція № 19 малосилікатні бурові розчини
- •19.1 Призначення розчинів та умови застосування
- •19.2 Склад і властивості малосилікатних розчинів
- •19.3 Технологія приготування малосилікатних розчинів
- •19.4 Управління властивостями розчину в процесі буріння
- •19.5 Перевід в інші типи розчинів
- •20.2 Склад і властивості розчинів Склад і граничні значення показників властивостей розчинів оброблених солями алюмінію наведені в табл. 20.1. В дужках дані взаємозамінні матеріали
- •20.3 Технологія приготування
- •20.4 Регулювання властивостями розчину в процесі буріння
- •Алюмокалієвий розчин. Регулювання показників властивостей алюмокалієвого розчину здійснюють аналогічно алюмінизованому.
- •20.5 Перевід в інші типи розчинів
- •20.6 Вплив розчинів оброблених солями алюмінію на наступні технологічні операції
- •Лекція № 21 соленасичені бурові розчини
- •21.1 Призначення соленасичених розчинів та умови їх застосування
- •21.2 Склад і властивості соленасичених розчинів
- •21.4 Регулювання властивостей розчину
- •21.6 Вплив на наступні технологічні операції
- •Лекція № 22 застосування розчинів на основі гідрогелю магнію
- •22.1 Призначення розчинів і умови застосування
- •22.2 Склад і властивості розчинів на основі гідро гелю магнію
- •В дужках дані взаємозамінні матеріали
- •22.3 Технологія приготування
- •22.4 Регулювання властивостями розчину в процесі буріння
- •22.5 Перевід в інші типи розчинів
- •22.6 Вплив на наступні технологічні операції
- •23.2 Склад і властивості вапнисто-бітумних розчинів
- •23.3 Технологія приготування розчину (вбр-4)
- •Примітка
- •23.4 Регулювання властивостей вбр в процесі буріння
- •23.5 Перехід на промивку вбр. Особливості його застосування
- •23.6 Вплив на наступні технологічні операції
- •24.2 Склад і властивості інертно-емульсійних розчинів
- •24.3 Перевід в інші типи розчинів
- •24.4 Регулювання властивостями іер в процесі буріння
- •24.5 Вплив на наступні технологічні операції
- •25.2 Склад і властивості еарованих бурових розчинів
- •25.3 Технологія приготування
- •25.4 Регулювання властивостей розчину в процесі буріння
- •25.6 Вплив розчину наступні технологічні операції
3.4 Агрегатна та седиментаційна стійкість колоїдних розчинів. (Стійкість дисперсних систем)
Під агрегатною стійкістю розуміють здатність частинок дисперсної фази чинити опір злипанню (з’єднанню) і тим самим утримувати встановлену дисперсність. Іншими словами агрегатна стійкість – це здатність дисперсної системи зберігати свою дисперсність та індивідуальність частинок дисперсної фази.
Фактори, які впливають на агрегативну стійкість:
– електричний бар’єр, обумовлений силами відштовхування;
– адсорбційно-сольватний бар’єр, який оточує частинку.
Ці фактори взаємозв’язані і діють одночасно.
Під седиментаційною стійкістю розуміють здатність дисперсної фази утримуватися у взмуленому стані під впливом броунівського руху, іншими словами – це стійкість до масо-гравітаційних сил.
Основний фактор седиментаційної стійкості – це броунівський рух.
Інші фактори:
– ступінь дисперсності. Чим більша дисперсність, тим система седиментаційно стійкіша;
– в’язкість дисперсійного середовища; (різниця густин дисперсійного середовища і дисперсної фази).
Перші два фактори входять в класичне рівняння Стокса, яке описує швидкість осідання частинок у дисперсійному середовищі.
 ,
(3.2)
,
(3.2)
де
F –
в’язкісний опір д.с. осіданню частинок;
 – в’язкість дисперсійного середовища
Па·с;
– в’язкість дисперсійного середовища
Па·с;
 – розмір частинок.
– розмір частинок.
Осідання частинок під дією сил гравітації називається седиментацією.
Тверді частинки дисперсної фази, як правило мають більшу густину у порівнянні із дисперсійним середовищем. В дисперсних системах типу емульсії частинки із меншою густиною випливають поверх рідини із більшою густиною. Гравітаційна сила, яка діє на дисперсну фазу:
 ,
(3.3)
,
(3.3)
де
 – маса частинок;
– маса частинок;
 – маса дисперсійного середовища.
– маса дисперсійного середовища.
Для сферичних частинок
 ,
,
 ,
(3.4)
,
(3.4)
У випадку, коли осідання припиняється, сила гравітації і сила в’язкістного опору урівноважується
 ,
(3.5)
,
(3.5)
 ,
(3.6)
,
(3.6)
 ,
(3.7)
,
(3.7)
 ,
,
 ,
(3.8)
,
(3.8)
 ,
,
 ,
(3.9)
,
(3.9)
На
підставі цієї залежності можна встановити
час осідання у воді глибиною
 мм частинок різного розміру
мм частинок різного розміру
r мкм |
50 |
10 |
5 |
1 |
0,1 |
t |
12 c |
5 хв |
20 хв |
8,3 год |
> 1 міс |
3.5 Явище коагуляції та колоїдний захист у глинистих суспензіях
Частинки дисперсної фази у дисперсних системах безліч разів зустрічаються і знову розходяться. Взаємодія двох частинок 1 і 2 із молекулою води дисперсійного середовища демонструється схемою, яка показана на рис. 3.2
Дві
частинки 1 і 2 розташовані на деякій
віддалі від молекули води А, яка здатна
притягувати до себе інші молекули води,
що знаходяться у сфері її дії, всі сили
у ромбі урівноважені. Праворуч молекул
води більше, тому рівнодійна направлена
вправо. В той же час молекула знаходиться
під дією сил
 і
і
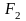 зі сторони твердої фази. Сумарна сила
зі сторони твердої фази. Сумарна сила
 направлена вліво. Якщо
направлена вліво. Якщо
 ,
то відбувається злипання частинок. Якщо
,
то відбувається злипання частинок. Якщо
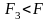 ,
то частинки розходяться внаслідок дії
розклинюючого тиску.
,
то частинки розходяться внаслідок дії
розклинюючого тиску.

Рисунок 3.2 – Схема взаємодії частинок дисперсної фази із водою
Процес злипання глинистих частинок називається коагуляцією. Злипаючись частинки утворюють комки, а точніше агрегати частинок, які злиплися. Дисперсна система стала нестійка. Це агрегативна нестійкість. Грудки випадають в осад внаслідок седиментації. Отже дія агрегативної нестійкості спричиняє седиментаційну нестійкість. Частинки дисперсної фази вся поверхня яких гідрофобна здатні до коагуляції утворюючи щільні грудки, які швидко седиментують. Злипання частинок відбувається гранями і вода залишає простір між частинками. Така коагуляція називається гідрофобна. Якщо частинки глини злипаються вершинами то така коагуляція називається гідрофільною. В цьому випадку формуються розсипчасті агрегати, які підлягають седиментації значно повільніше. Осад, який утворився у цьому випадку називають гелем, а система із змулених частинок, які не злиплися – золем. На рис. 3.3 показані коагуляційні явища які притаманні буровим розчинам

Рисунок 3.3 – Схема коагуляційних явищ у бурових промивальних рідинах
У бурових промивальних рідинах постійно відбуваються процеси коагуляції і забезпечити над ними контроль є складною технологічною задачею. Колоїдний захист суттєво послаблює коагуляцію в бурових розчинах.
Бурові промивальні рідини можна застосовувати тільки у випадку, якщо вона володіє достатньою седиментаційною стійкістю і при використанні не підлягає осадоутворенню, зберігаючи свої технологічні властивості. В той же час надлишкова, або недостатньо агрегативна стійкість також небажана, в першому випадку виникають надлишкові тиски під час прокачування, а в другому низька утримуюча здатність. Отже, седиментаційна нестійкість повинна бути виключена повністю, а агрегативна – регулюватися в необхідних межах.
Достатньо високий ступінь дисперсності глин у сукупності зі структуроутворенням дає змогу практично повністю припинити сидементаційні явища у бурових розчинах.
Послаблення коагуляції у бурових розчинах досягається шляхом надання всім частинкам дисперсної фази одинаковою за знаком електричного заряду, щоб вона відштовхувалася під час взаємодії між собою. Збільшуючи заряд аніонів, які захищають частинку також вдається пригальмувати коагуляційні процеси. У першому випадку необхідно уникати надлишку позитивних катіонів, які швидко нейтралізують від’ємний заряд частинок і коагуляція відновиться. А в другому випадку під час адсорбції аніонів на поверхні твердої фази сили, які їх утримують слабкі, що є причиною слабкого захисту від коагуляції.
Сильний і стабільний колоїдний захист від коагуляції забезпечується застосуванням органічних сполук, які добре розчиняються у воді.
В порівнянні із неорганічними сполуками вони володіють значною мірою молекулярною масою і крім цього у них атоми вуглецю разом із іншими складовими елементами утворюють довгі ланцюжки Водень у гідроксильних (ОН), спиртових (СН2ОН), карбоксильних (СООН) групах заміщається натрієм і при розчиненні у воді спостерігається дисоціація цих сполук. Катіонами у цьому випадку є іони натрію, а аніонами – високогідрофільні залишки молекул органічних сполук. Завдяки великій кількості названих вище груп аніони володіють значним електричним зарядом, який підсилює електричний захист під час адсорбції цих аніонів на частинках дисперсної фази. Для багатьох органічних сполук додатково спостерігається хімічна фіксація аніонів на поверхні частинок дисперсної фази. Крім цього адсорбуючись на твердій фазі органічні сполуки утворюють стійку абсорбційну оболонку, яка запобігає коагуляції, цю оболонку називають структурно-механічним бар’єром.
Таким чином, органічні сполуки забезпечують колоїдний захист такими чинниками:
– значною кількістю електричних зарядів;
– хемосорбцією;
–структурно-механічним бар’єром.
Наявність такого ланцюжка навколо твердої фази зменшує її чутливість до накопичення катіонів під час захисту від коагуляції. Речовини, які забезпечують сильний калоїдний захист називаються захисними колоїдами, або стабілізаторами.
ЛЕКЦІЯ № 4
ГЛИНОПОРОШКИ, ТЕХНОЛОГІЯ ЇХ ВИРОБНИЦТВА ТА
ПОКАЗНИКИ ЯКОСТІ
4.1 Технологія виробництва глин.
Типи і марки глинопорошків
Технологія виготовлення глинопорошків на вітчизняних заводах однакова і складається з таких операцій:
– вивезення глин із кар’єрів та її складування на проміжному механізованому складі;
– дроблення глини кар’єрної вологості яка визначається умовами тонкого помолу;
– сушіння меленої глини;
–подрібнення сухої глини;
– дрібний помол сухої глини;
– пакування готової продукції та відвантажування її на склад.
На рис. 4.1 показана технологічна схема виготовлення глинопорошків.
В табл. 4.1 наведені типи і марки глинопорошків і основні показники їх якості.
Основні технологічні параметри при виготовленні глинопорошків є: сушіння, помол та дозування реагентів для модифікації.
Тонкий помол відрізняється від грубого застосуванням ролико-маятникрвого млина.
Згідно галузевого стандарту розрізняють такі марки глинопорошків:
В США запаси глин є в 26 штатах, найкраще придатні глини знаходяться в штаті Монтана, Вайомінг та Південна Дакота. Вайомінський бентоніт має обмінну ємність в межах 100-110мГекв./100г, це забезпечує вихід 16М3/т.
Високу дисперсність має і палигорскітовий глинопорошок, який отримують із палигорскіту штатів Вайомінг та Флорида.

Рисунок 4.1 – Технологічна схема виготовлення глинопорошків
Вайомінський бентоніт має обмінну ємність в межах 100-110мГекв./100г, це забезпечує вихід 16М3/т.
Високу дисперсність має і палигорскітовий глинопорошок, який отримують із палигорскіту штатів Вайомінг та Флорида.
