
- •Федеральное агентство по образованию Государственное образовательное учреждение высшего профессионального образования Ухтинский государственный технический университет
- •Оглавление
- •Введение
- •Теоретические основы процесса обезвоживания и обессоливания нефти
- •Теоретические аспекты процессов перегонки и ректификации нефти
- •Влияние технологических параметров на процесс перегонки нефти
- •Химическая природа и групповой углеводородный состав нефтей и нефтяных газов
- •Фракционный и химический состав нефти
- •Основные физические свойства нефти и нефтепродуктов
- •Классификация и товарные характеристики нефтей и нефтепродуктов
- •Подготовка нефти к переработке
- •Нефтяные эмульсии. Условия образования эмульсий
- •Свойства и способы разрушения нефтяных эмульсий
- •Первичная переработка нефти
- •Процессы первичной и вторичной переработки нефти
- •Вторичная перегонка нефтяных фракций
- •Продукты первичной перегонки
- •1, 12, 14, 23, 24, 29, 30, 32-35 – Насосы; 17 – холодильник; 2-5, 7, 25 – теплообменники;
- •9, 10, 18, 19, 27 – Конденсаторы холодильники; 15, 31 – трубчатые печи;
- •VIII – фракция 180-2300с; IX – фракция 230-3500с; X – фракция выше 3500с;
- •Вторичная перегонка нефтяных фракций
- •Вторичная перегонка бензина
- •Вторичная перегонка масляных франкций
- •Общая характеристика термических процессов Термические процессы переработки нефти
- •Термические превращения углеводородов
- •Термические процессы
- •Пиролиз, газоразделение, получение низших олефинов
- •Компримирование пирогаза
- •1, 8, 14, 19, – Колонны; 2, 4 – холодильники; 3, 5, 11, 17, 22 – насосы; 7 – теплообменнник;
- •6, 12, 18, 23 – Кипятильник; 9, 15, 20 – конденсаторы-холодильники; 10, 16, 21 – емкости.
- •Переработка жидких продуктов пиролиза
- •Термокаталитические процессы переработки
- •Катализ и свойства катализаторов
- •Сырьё, параметры и продукты каталитического крекинга
- •Каталитический риформинг
- •Гидрогенизационные процессы
- •5, 6, 11, 28 – Сепараторы; 7, 13, 25 – теплообменник; 8, 18, 19, 26 – колонны;
- •9, 12, 20, 21, 29 – Насосы; 14 – компрессор; 16, 17, 22 – емкости; 30 – кипятильник.
- •Производство водорода
- •Производство твердых парафинов
- •Газы, конденсаты
- •Пределы взрываемости (воспламеняемости)
- •Переработка природных и попутных газов
- •Газофракционирующие установки
- •VIII – конденсат водяного пара; IX – водородсодержащий газ на сероочистку разделение газов ректификацией
- •Переработка нефтяных газов
- •Разделение газов
- •VIII – теплоноситель (пар); IX – конденсат водяного пара
- •Вопросы для самоконтроля Нефть и её свойства
- •Подготовка нефти к переработке
- •Первичная переработка нефтяного сырья
- •Понятие о вторичных процессах переработки нефтяного сырья
- •Термический крекинг
- •Процессы коксования
- •Пиролиз
- •Общие представления о катализе и катализаторах
- •Каталитический крекинг
- •Каталитический риформинг
- •Катализаторы и механизм гидрогенизационных процессов
- •Характеристика газообразных углеводородов, очистка и осушка газов
- •Разделение газов
- •Процессы алкилирования разветвленных алканов алкенами
- •Полимеризация (олигомеризация) алкенов
- •Изомеризация лёгких алканов
- •Процессы депарафинизации
- •Очистка светлых дистиллятов
- •Основы технологии производства нефтяных масел
- •Адсорбционная очистка масел
- •Сернокислотная и щелочная очистка масел
- •Гидроочистка и гидрокрекинг в производстве масел
- •Бензины
- •Керосины
- •Дизельные топлива
- •Нефтяные масла
- •Нефтяные смазки
- •Основные и дополнительные единицы си
- •Приложение а2
- •Некоторые производные единицы си, наименование которых образованы из наименования основных и дополнительных единиц
- •Приложение а3
- •Некоторые основные единицы си
- •Приложение в
- •Соотношения между единицами тепловых величин
- •Приложение с Алфавиты
- •Латинский и греческий алфавиты
- •Приложение д1 Определение баррелей в тонне
- •Приложение д2
- •Количество баррелей в тонне нефти (типы нефти по гост р51858-2002)
- •Библиографический список
- •Указатель терминов
- •Надежда Семёновна Вишневская
- •Технология переработки углеводородного сырья
- •169300, Республика Коми, г. Ухта, ул. Первомайская, д. 13.
- •169300, Республика Коми, г. Ухта, ул. Октябрьская, д. 13.
Термокаталитические процессы переработки

Рис .27. Схема установки каталитического крекинга
I – сырье; II – катализатор; III – бензин; IV – жирный газ; V – легкий газойль;
VI – сырье для производства технического углерода; VII – тяжелый газойль; VIII – воздух;
IX – водяной пар; X – дымовые газы; XI – циркулирующее орошение
На второй ступени гидрогенизационной переработки проводится полное удаление сернистых соединений, что достигается исчерпывающим годрогенолизом сероорганических соединений, включая тиофен. В результате образуется сероводород и соответствующий парафиновый углеводород. Одновременно гидрируются все алифатические и циклические непредельные углеводороды до парафиновых и нафтеновых углеводородов.
На третьей ступени в условиях высокой температуры неароматические компоненты полностью гидрокрекируются с образованием легких газов – метана и небольшого количества этана и т.д. Толуол и другие алкилбензолы гидродеалкилируются и дают бензол. Бензольное кольцо в условиях ГТП устойчиво, оно практически не затрагивается. Важным продуктом является дифенил, который вновь образует бензол при возврате в цикл.
Жидкая часть последней ступени обычно содержит (в %): бензол – 85-90; толуол – 5-8; ксилолов и этилбензола 1-3; дифенил – 3-5; более тяжелые углеводороды – 3-4; неароматические С6-С8 – не более 0,1.
Головная фракция может гидрироваться для использования компонентом автобензина, а тяжелый остаток предварительной ректификации добавляется к котельному топливу. При этом целесообразно в производство бензола вовлекать и углеводороды С9, т.е. направлять на получение бензола фракцию 70-190°C.
Катализ и свойства катализаторов

Рис.28. Схема установки каталитического крекинга с псевдоожиженным слоем микросферического катализатора
К-1 – ректификационная колонна; К-2 – отпарная колонна; П-1 – П-3 – печи;
Р-1 – реактор; Р-2 – регенератор; ПК-1 – компрессор; ПК-2 – воздуходувка;
ХК-1 –конденсаторы-холодильники; Х 1, Х2 – холодильник; Т-1 – Т-4 – теплообменник; С1 – сепаратор; Е1 – емкость для воды; А-1 – котел-утилизатор; А-2 – электрофильтр;
А-3 – дозер; Н-1 – Н-6 – насосы.
I – сырье; II – катализатор; III – бензин; IV – жирный газ; V – легкий газоль; VI – сырье для производства технического углерода; VII – вода; VIII – воздух; IX – водяной пар; X – дымовые газы; XI – топливный газ; XII – циркулирующее орошение К-1
Сущность и значение катализатора в снижении энергии активации химических реакций и, следовательно, повышении их скорости.
Любой катализатор активно взаимодействует с исходными реагентами в начальных стадиях. В последующих стадиях он полностью регенерируется. Поэтому небольшого количества катализатора достаточно для получения больших количеств конечного продукта.
Различают гомогенный и гетерогенный катализ. При гомогенном катализе катализатор и реагенты образуют однородную систему (газовые смеси, жидкие растворы). При гетерогенном катализе катализатор чаще находится в твердой фазе, а реагенты – в газообразном, парообразном состоянии. Катализатор и реагенты могут быть жидкостями, которые не смешиваются между собой.
Наиболее распространены процессы получения топлив – каталитический крекинг, изомеризация, риформинг, алкилирование, гидрокрекинг. Каталитические реакции принято делить на кислотно-основные и окислительно-восстановительные.
Кислотно-основные (ионные) – это реакции, присоединяющие или отщепляющие ионы водорода и реакции, при которых свободная пара электронов перемещается без разобщения электронов, образуя координационную связь в комплексном соединении. К таким реакциям относятся каталитический крекинг, полимеризация, изомеризация, гидратация углеводородов и ряд других превращений. Окислительно-восстановительные реакции связаны с переходом электронов – протекают с разъединением электронной пары с разрывом валентной связи. Сюда относятся многочисленные каталитические процессы окисления, гидратирования, дегидрирования и др.
Гомогенный катализ объясняется теорией промежуточных химических соединений. Катализатор образует с реагентом неустойчивое реакционноспособное промежуточное соединение. Промежуточное соединение распадается или реагирует с новой молекулой исходного вещества, освобождая катализатор в неизменном виде.
Гетерогенный катализ. Все превращения происходят на поверхности раздела твердой фазы катализатора и газовой или паровой фазы реагирующих веществ и в значительной мере за счет сорбции. Процесс проходит в несколько этапов:
диффузия реагирующих молекул к поверхности катализатора;
активированная адсорбция на поверхности катализатора;
химическая реакция на поверхности катализатора;
десорбция с поверхности катализатора;
диффузия продуктов реакции в газовую фазу.
Скорость процесса определяется скоростью самого медленного этапа.
Хемосорбция – образование достаточно прочного мономолекулярного слоя реагентов на поверхности катализатора. Протекает за счет валентных сил катализатора и, по сути, близка к обычной химической реакции, приводящей к значительному ослаблению связей в реагирующих молекулах. Адсорбция происходит не на всей свободной поверхности твердого катализатора – только на активных центрах, где запас свободной энергии больше – острые углы, пики, неровности, ребра кристаллов, химически неоднородные участки и т.д. От реакционной способности и природы соединений зависят и скорость протекающих реакций, и состав конечных продуктов. При подборе гетерогенных катализаторов необходимо учитывать их селективность, активность и стабильность, определяющую срок службы.
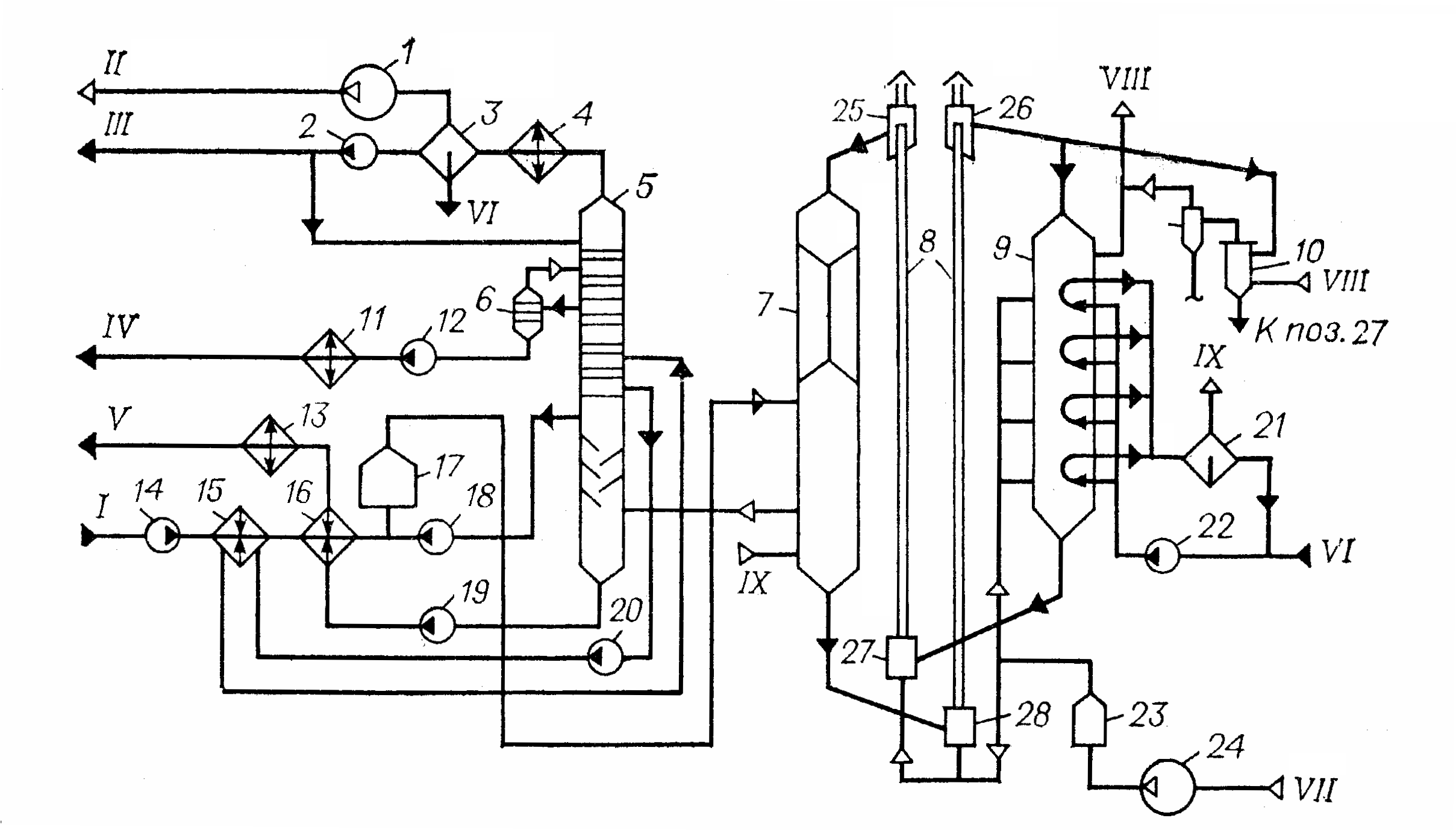
Рис. 29. Технологическая cхема установки каталитического крекинга с движущимся шариковым катализатором
1 – компрессор; 2, 12, 14, 18-20, 22 – насосы; 3, 10 – сепараторы; 4, 11, 13 – холодильники;
5, 6 – колонны; 7 – реактор; 8 – пневмоподъемник; 9 – регенератор; 13 – холодильник;
15, 16 – теплообменник; 17, 23 – печи; 21 – паросборник; 24 – воздуходувка;
25, 26 – бункеры-сепараторы; 27, 28 – дозаторы пневмотранспорта.
I – сырье; II – жирный газ; III – бензин; IV – фракция 195-3500С; V – фракция выше 3500С;
VI – вода; VII – воздух; VIII – дымовые газы; IX – водяной пар
Под селективностью (избирательностью) катализатора понимают способность ускорять только одну или несколько реакций определенного типа. Это связано как с составом катализатора, так и с условиями его применения. Активность катализатора характеризует его производительность, а активность твердого катализатора зависит главным образом от состояния его поверхности. Для увеличения площади катализатора его часто наносят на подложку (носитель), обладающую пористой поверхностью (активированный уголь, пемза, кизельгур, оксид алюминия, силикагель, искусственные цеолиты различных марок). Носитель повышает активность катализатора, придает ему механическую прочность, уменьшает его расход.
Активность катализаторов удается повысить добавлением небольшого количества промоторов или активаторов – веществ, увеличивающих внутреннюю поверхность катализаторов, воздействующих на их структуру и способствующих её сохранению во время работы. Такие промоторы называются структурными. Другие активаторы (химические) изменяют химический состав поверхности катализатора, увеличивают число активных центров. Активность катализаторов со временем падает (дезактивация, утомление, старение). Чаще всего это отложения на его активных центрах продуктов реакции (кокса, смол, парафинов) или следствие взаимодействия примесей в сырье (каталитических ядов). Они особенно опасны – для полной дезактивации катализатора, достаточно их ничтожного количества (из-за их необратимой адсорбции на активных центрах катализатора).
Наиболее чувствительны к ядам металлические катализаторы, содержащие Fe, Co, Ni, Pd, Ir, Pt, Cu, Аg. Часто встречаются каталитические яды: сероводород, другие серосодержащие соединения, оксид углерода, азотистые основания, галогены, соединения фосфора, мышьяка и сурьмы, а также металлы, содержащиеся в тяжелом нефтяном сырье (Ni, Ft, V). Причиной дезактивации является также изменение структуры поверхности катализатора, спекание и другие процессы, уменьшающие его поверхность или число активных центров.
Восстановление активности (регенерация) катализатора может производиться выжиганием с поверхности катализатора в токе воздуха углистых и смолистых отложений. Окисленные катализаторы восстанавливают действием водорода при определенной температуре. Катализаторы с редкими элементами (торий) регенерируют химическим путем – редкий элемент извлекают из отработанного катализатора и используют для изготовления новых порций катализатора. Катализаторами называют восстановленные металлы, оксиды, кислоты, основания, соли, сульфиды металлов, некоторые органические соединения.
Цеолиты. Природные и искусственные алюмосиликаты с чрезвычайно тонкопористой структурой – алюмосиликаты натрия, кальция и других металлов. Все цеолиты имеют кристаллическое строение. Их общее свойство – наличие мельчайших полостей, сообщающихся через поры. Число полостей очень велико – их общий объем может достигать половины объема кристалла. Поэтому обезвоженные цеолиты являются прекрасными адсорбентами. Размеры пор у цеолитов малы и имеют одинаковый диаметр (от 0,3 до 1,3 нм). Цеолиты обладают просеивающими свойствами – могут пропускать молекулы только определенного размера, не превышающие диаметра пор данного цеолита (молекулярное сито).
Характерная черта каталитического крекинга – процессы перераспределения или диспропорционирования водорода. Молекулы, адсорбированные на катализаторе, склонны терять водород – дегидратироваться. Увеличивается насыщенность, происходит более прочная адсорбция на катализаторе. Вновь образовавшиеся непредельные углеводороды начинают полимеризироваться и превращаться в конечный продукт процесса – кокс, который необратимо откладывается на катализаторе. Катализатор необходимо регенерировать. Водород, теряемый реагирующими молекулами, расходуется на насыщение осколков молекул – прежде всего на гидрирование изомеризированных алкенов. Одни молекулы углеводородов теряют водород, другие за их счет насыщаются водородом. В этом и заключается процесс диспропорционирования водорода. Углеводороды различных гомологических рядов ведут себя при каталитическом крекинге по-разному.
Алканы распадаются на алкен и алкан меньшей молекулярной массы.
Распад происходит в нескольких местах углеродной цепи, но не на самом её конце. Выход метана, этана, этилена незначительны. В газе накапливаются углеводороды С3-С4. Скорость распада в десятки раз больше, чем при термическом крекинге. Алканы не попадают в хемосорбционный слой. Но и за пределами этого слоя проявляется поверхностная энергия катализатора. Создается зона повышенной концентрации углеводородов с ослабленными связями С-С. Возможно дегидрирование углеводородов с числом С>4. Образующиеся при этом высшие алкены также распадаются.
Алкены. Скорость распада алкенов в тысячи раз больше, чем при термическом крекинге. Помимо распада алкены вступают в реакции полимеризации, деполимеризации, перераспределения водорода, изомеризации, циклизации. Особенно разнообразны реакции изомеризации: структурная перегруппировка, перемещение двойной связи вдоль цепи, цис- и транс-изомерия.
Циклоалканы. Происходит деалкилирование, дегидрирование, распад кольца. В присутствии катализатора реакции ускоряются в 500-4000 раз. Кроме того, заметно развиты реакции распада кольца с образованием изоалкенов, изомеризация циклов, перераспределение боковых цепей (миграция заместителей). Дегидрирование и деалкилирование циклоалканов протекает с перераспределением водорода – в результате накапливаются арены и алканы. Бициклические циклоалканы дают начало моноциклическим аренам, циклогексанам, циклопентанам и алканам. Характерно образование осколков не ниже С3.
Арены. Гомологи бензола преимущественно полностью теряют боковые цепи, что приводит к накоплению бензола. По мере увеличения длины боковой цепи и её разветвления глубина деалкилирования возрастает. Полиметилированные гомологи бензола легко изомеризуются с перераспределением метильных групп. В продуктах обнаруживаются толуол, триметилбензол, м- и о-ксилолы. Происходит как миграция метильных групп по бензольному кольцу, так и их диспропорционирование. Все реакции обратимы. Конденсированные полициклические углеводороды очень легко адсорбируются на катализаторе и крекируются на нем до кокса. Бензол в реакции не вступает и накапливается в крекинг-бензине. При каталитическом крекинге в газе меньше низкомолекулярных компонентов, но гораздо больше изобутана. Бензины обогащаются изоалканами и аренами.
