
- •Розділ 4. Біофізика білків
- •4.1. Первинна й вторинна структура білків
- •4.2. Дисперсія оптичного обертання (доо) і круговий дихроїзм (кд)
- •4.3. Домени й третинна будова білків
- •4.4. Диференціальна скануюча мікрокалориметрія
- •4.5. Динаміка структури білків
- •4.6. Абсорбційна й диференційна спектрофометрія
- •4.7. Флуоресцентна спектроскопія білків
- •4.8. Ядерний магнітний резонанс (ямр)
- •4.9. Електронний парамагнітний резонанс (епр)
- •4.10. Ферментний каталіз
- •4.11. Кінетика ферментативних реакцій
- •4.12. Вплив температури на швидкість біохімічних реакцій
- •4.13. Алостеричні ферменти. Регуляція хімічних реакцій у клітині
- •Біофізика нуклеїнових кислот
- •5.1. Структура мономерних компонентів нуклеїнових кислот
- •5.2. Первинна структура нуклеїнових кислот
- •5.3. Вторинна структура днк
- •5.4. Конформації подвійних спіралей нуклеїнових кислот
- •5.5. Структура тРнк
- •5.6. Рівні компактизації днк
- •5.7. Оптичні характеристики і гіперхромний ефект днк
- •5.8. Ренатурація й кінетика ренатурації денатурованої днк
- •5.9. Біологічна функція нуклеїнових кислот
- •5.10. Клонування днк
- •5.11. Нуклеїново-білкове впізнавання
5.4. Конформації подвійних спіралей нуклеїнових кислот
Сили, що стабілізують асоціати основ. Між основами існують два типи взаємодій: горизонтальні, за рахунок водневих зв’язків між комплементарними парами, і вертикальні, або стекінг-взаємодії за рахунок дисперсійних лондоновських і гідрофобних ефектів. У неводних розчинах й у кристалічному стані основи, нуклеозиди й нуклеотиди асоціюють за рахунок утворення водневих зв’язків. Водневі зв’язки в 20–30 разів слабкіші за ковалентні. Водневі зв’язки легше розтягуються й згинаються, в результаті чого геометрія системи атомів х-н∙∙∙∙у не є постійною. Утворення водневих зв’язків веде до перерозподілу зарядів: х і у стають ще більш електронегативними, а Н – ще більш електропозитивним.
У водних розчинах унесок у стабілізацію асоціатів за рахунок стекінгу збільшується, оскільки з донорами й акцепторами водневих зв’язків між основами конкурують молекули води. Взаємодії вертикального типу полягають у тому, що основи розміщуються одна над одною на відстані вандерваальсового радіуса 0,34 нм, утворюючи стопки. Сила стекінг-взаємодій зменшується в ряду: пурин-пурин > пурин - піримідин > піримідин - піримідин. Міжплощинні (стопкові) взаємодії основ збільшуються, якщо вони входять до складу полінуклеотидів.
Водне оточення нуклеїнових кислот відіграє важливу роль. Вода – це не просто середовище, в якому розчинені ті чи інші молекули. Вода взаємодіє з розчиненими молекулами й стабілізує вторинну та третинну структури макромолекул. Це стосується і білків, і ДНК, причому ДНК навіть більшою мірою, тому що висока діелектрична проникність води й гідратовані протиіони послаблюють електростатичне відштовхування фосфатів. Молекули води впливають і на процес самозбирання мономерних компонентів нуклеїнових кислот в упорядковані структури, тому що цей процес значною мірою зумовлено гідрофобними взаємодіями. Ступінь гідратації ДНК має визначальне значення для конформації: за високої відносної вологості ДНК перебуває в В-формі, зменшення вологості (чи збільшення іонної сили) приводить до переходу ДНК з В- в С-, А- чи (якщо дозволяє послідовність) у D- і Z-форми.
Гідратацію макромолекули визначає параметр Г, який у випадку ДНК дорівнює кількості молів води, що припадає на 1 моль нуклеотидів. Вторинна структура ДНК тісно пов’язана з параметром Г, а той у свою чергу – безпосередньо з активністю води, яка зростає з пониженням концентрації солі в розчині. Хоч вплив катіонів на активність води визначається іонною силою й загалом не залежить від виду катіона, різні катіони по-різному впливають на вторинну структуру ДНК, що свідчить про певну специфічність їхньої взаємодії.
Дві гідратні оболонки подвійної спіралі ДНК. Експериментальні дані, отримані різними методами, свідчать про те, що молекула ДНК, яка являє собою поліелектроліт, є сильно й нерівномірно гідратованою. Навколо неї утворюються два дискретні шари молекул води – первинна й вторинна гідратні оболонки. Первинна гідратна оболонка є не проникною для катіонів і за структурою не схожою на лід. Вона містить принаймні 11–12 молекул води на нуклеотид. Ці молекули, відповідно до зменшення сили зв’язування можна розбити на три класи: зв’язані із фосфатами (І), із фосфодіетерними зв’язками та залишками вуглеводів (ІІ) і з основами (ІІІ). За даними ІЧ-спектроскопії, атоми кисню фосфатів гідратовані навіть за відносної вологості менше 65 %. При цьому на нуклеотид припадає п’ять–шість молекул води. Атоми кисню фосфодіетерного зв’язку й кисень фуранозного кільця за відносної вологості нижче 60 % гідратовані лише частково. Гідратація функціональних аміно-, іміно- й кетогруп основ відбувається за відносної вологості вище 65 % і приводить до додаткового зв’язування восьми–дев’яти молекул води. За відносної вологості близько 80 % первинна гідратна оболонка подвійної спіралі ДНК заповнюється, при цьому на нуклеотид припадає приблизно по 20 молекул води. Подальше збільшення ступеня гідратації спричиняє набухання зразка, про що свідчать результати рентгенівської дифракції на волокнах ДНК. Як свідчить ІЧ-спектроскопія, первинна гідратна оболонка відрізняється за своєю структурою від звичайної води. Безпосередньо з ДНК контактують не всі 20 молекул, а 11–12 молекул внутрішньої частини гідратної оболонки, з якими зв’язані ще вісім–дев’ять молекул води. Внутрішня оболонка є не проникною для катіонів і “не замерзає” (тобто не утворює структури льоду) за температури, яка значно нижчою 0оС.
Вторинна гідратна оболонка не відрізняється від звичайної води за проникністю для іонів і за здатністю утворювати структуру льоду І.
Різні стани гідратації ДНК. а-, в- і с-днк. За високої активності води, коли катіони не порушують первинну гідратну оболонку, яка складається з 20 молекул води на нуклеотид, ДНК перебуває у В-формі. За зниження відносної вологості у волокні чи плівці, чи за збільшення концентрації солі в розчині ступінь гідратації зменшується й за певного порогового значення Г (менше 20 молекул води на нуклеотид) спостерігається структурний перехід ДНК з В-форми в С- чи А-форму залежно від природи присутнього протиіона. Перехід ВС відбувається “плавно”, як це має бути у випадку двох структурно близьких форм. Інакше кажучи, між цими крайніми формами існує множинна проміжних форм. Щодо переходів ВА і СА, то через зміни конформації вуглеводу С2-ендо С3-ендо вони відбуваються стрибкоподібно й кооперативно.
Переходи ДНК з однієї структурної форми в іншу можна спостерігати за зміною спектрів кругового дихроїзму. Зі збільшенням концентрації солі йде “плавний” структурний перехід ВС; коли концентрація солі досягає певної величини, спостерігається різкий кооперативний перехід СА чи ВА. Такі переходи відбуваються також за зміни полярності середовища, наприклад, при додаванні в систему етанолу, ізопропанолу чи діоксану до концентрацій близько 80 %. Проміжні стани, які фіксуються спектрополяриметрично, відповідають не проміжним формам між А- і В-ДНК, а різному співвідношенню цих форм.
Спектри КД й результати експериментів з рентгенівського розсіювання свідчать про те, що в розчині кількість нуклеотидів на виток ДНК у В-формі не дорівнює 10, як у волокнах, досліджених методами рентгенівської дифракції. В-ДНК у розчині є трохи розкрученою.
Поверхня а- і в-днк, доступна молекулам розчинника. Згортання поліпептидів і полінуклеотидів з утворенням вторинної структури характеризується тим, що певні групи атомів, які в неупорядкованих полімерів контактували б з розчинником, при згортанні ланцюга опиняються всередині. Для оцінки впливу розчинника на укладку полінуклеотидного ланцюга було розвинено концепцію доступної поверхні, за допомогою якої можна кількісно визначити співвідношення між захованими і доступними для молекул розчинника групами атомів.
Якщо порівнювати площі доступної поверхні повністю витягнутої ДНК і ДНК в А- чи В-формі, то ми побачимо, що при утворенні подвійного ланцюга атоми кисню фосфатних груп залишаються майже повністю відкритими, тоді як основи на 80 % маскуються іншими атомами. Інакше кажучи, якщо в розкрученому ланцюгу ДНК на частку фосфатів припадає приблизно 20 % площі поверхні, на частку основ – 50 % і на частку вуглеводів – 30 %, то в подвійному ланцюгу фосфати займають 45 % площі поверхні , основи – 20 %, а вуглеводи – 35 %. Таким чином, полярність молекули ДНК при утворенні подвійної спіралі збільшується. Така сама закономірність спостерігається й у білків при утворенні глобулярних структур: полярні групи розташовуються на поверхні, а неполярні, гідрофобні – всередині.
Структура нуклеїнової кислоти, побудована за принципом уотсон-крікових пар, припускає існування різноманітних форм подвійних спіралей. Відмінності існують лише щодо кількості пар основ на виток спіралі, кута між парами основ і віссю спіралі, діаметра спіралі тощо. Розрізняють А- і В-родини нуклеїнових кислот. РНК належить до А-родини і може перебувати у двох близьких конформаціях А і А. Конформаційна різноманітність ДНК є значно більшою. Вона може мати А-, В-, С-, D-, Е- і Т-форму, що є правими спіралями. ДНК може перебувати також у формі лівої спіралі (Z-ДНК). У табл. 5.2 наведено параметри форм, які було встановлено експериментально.
Таблиця 5.2. Параметри спіралей волокон нуклеїнових кислот за даними рентгеноструктурного аналізу
Тип |
Крок спіралі, нм |
Відстань між залишками, нм |
Кут повороту на 1 основу, град |
Кількість залишків на 1 оберт |
A |
2,82 |
0,256 |
32,7 |
11,0 |
B |
3,38 |
0,338 |
36,0 |
10,0 |
C |
3,10 |
0,332 |
38,6 |
9,3 |
D |
2,43 |
0,300 |
45,0 |
8,0 |
E |
2,43 |
0,320 |
48,0 |
7,5 |
Z |
4,50 |
0,370 |
-30,0 |
6,0 |
Наведені структури поєднують деякі спільні риси. Це праві спіралі, що мають вісь симетрії другого порядку. Кінці подвійної спіралі ідентичні й містять по одному 3 і 5 кінцю, тобто ланцюги антипаралельні. Явище антипаралельності є важливим не тільки для дволанцюгових ДНК, але й для одноланцюгових РНК, наприклад тРНК, де утворення ділянок подвійних спіралей одноланцюговою молекулою забезпечує формування відповідної функціонально активної просторової структури. Ще однією спільною рисою подвійних спіралей є стекінг, або стопкові взаємодії. Наприклад, у тРНКPhe дріжджів тільки 42 основи із 76 утворюють спіральні ділянки, а у стекінг-взаємодіях задіяна 71 основа.
Подвійні спіралі ДНК в А- і В-формах суттєво відрізняються. У В-ДНК вісь спіралі проходить посередині комплементарних пар. В А-формі пари основ зміщені відносно осі спіралі приблизно на 0,5 нм, завдяки чому ДНК нагадує спіральну драбину (рис. 5.11).

Рис. 5.11. Схематичне зображення В- і А-форм ДНК: а – вид збоку, б – вид зверху. Основи у В-формі розміщені перпендикулярно, а в А-формі – під кутом 20о до осі спіралі
Характерною відмінністю між А- і В-формами нуклеїнових кислот є конформація вуглеводу. Виявилося, що в А-формах нуклеїнових кислот вуглеводний залишок має С3-ендоконформацію, а в В- формах – С2-ендо, РНК не може існувати в В-формі через просторові утруднення, які створює гідроксильна група в положенні 2рибози. Нижче наведено відмінності в лінійних розмірах і структурі нуклеотиду в А- і В-формі на прикладі рАр (рис. 5.12).
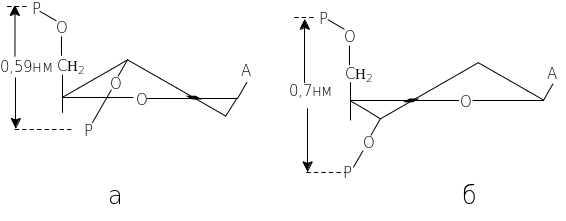
Рис. 5.12. Структура й лінійна довжина нуклеотиду: а – А-форма нуклеїнових кислот; С3-ендоконформація вуглеводу; б – В-форма ДНК; С2-ендоконформація дезоксірибози
