
- •Розроблено:
- •2. Виконавець:
- •Лекція № 1
- •Вступ до фізичної хімії, розвиток фізичної хімії.
- •Лекція № 3
- •Рідкий стан речовини. Поверхневий натяг, в'язкість.
- •Твердий стан речовини. Кристалічний і аморфний стан.
- •Лекція № 4
- •Основи хімічної термодинаміки.
- •Перший закон термодинаміки.
- •Закон Гесса і наслідки з нього.
- •II закон термодинаміки.
- •Лекція № 5
- •Фазові рівноваги. Загальні умови. Правило фаз.
- •Загальна характеристика і властивості розчинів
- •Лекція № 6
- •Фізичні властивості розчинів, дифузія, осмос.
- •Лекція № 7
- •Закони Рауля для відносного зниження тиску над розчином
- •Розчинення в розчинах електролітів
- •Закон Рауля для підвищення температури кипіння і зниження температури замерзання
- •Хімічна рівновага. Принцип Ле – Шательє
- •Лекція № 9
- •Типи хімічних реакцій
- •Лекція № 10
- •Лекція № 11
- •Електропровідність електролітів. Питома, еквівалентна і загальна.
- •Лекція № 12
- •Електрорушійні сили. Гальванічний елемент.
- •Лекція № 13
- •Дифузійний потенціал.
- •Потенціометричні визначення концентрації водневих розчинів.
- •Для виділення 1 кг речовини, потрібно пропустити через електроліт одну й ту ж кількість електрики, її позначають буквою f і називають числом Фарадея.
- •Лекція № 14
- •Колоїдна хімія. Вступ, загальна характеристика, класифікація.
- •Лекція № 15
- •Поверхневі явища. Сорбційні процеси, їх класифікація, адсорбція на межі різноманітних фаз.
- •Адсорбція тверде тіло –газ.
- •Лекція № 16
- •Адсорбція на межі тверде тіло – розчин.
- •Адсорбція на межі розчин – розчин.
- •Лекція № 17
- •Адсорбція електролітів
- •Адсорбція на межі розчин – газ.
- •Лекція № 18
- •Отримання колоїдних систем різними методами. Особливі властивості колоїдних систем по відношенню до істинних розчинів.
- •Методи очищення дисперсних систем.
- •Електролітичні властивості. Дослід Рейса. Електрофорез та електроосмос, їх практичне застосування.
- •Лекція № 19
- •Молекулярне - кінетичні властивості колоїдних систем
- •Лекція № 20
- •Оптичні властивості колоїдних розчинів. Ефект Тиндаля.
- •Лекція № 21
- •Будова міцели гідрозолю. Будова подвійного електричного шару.
- •Будова міцели золю.
- •Лекція № 22
- •Коагуляція гідрофобних золей електролітами. Поріг коагуляції. Практичне застосування коагуляції
- •Лекція № 23
- •Колоїдні поверхнево - активні речовини.
- •Вільнодисперсні системи, їх в'язкість. Зв'язанодисперсні системи, гелеутворення та пептизація.
- •Лекція № 24
- •Загальна характеристика суспензій. Агрегативна стійкість, коагуляція суспензій. Методи отримання.
- •Грубодисперсні (мікрогетерогенні) системи – емульсії.
- •Лекція № 25
- •Лекція № 26
- •Лекція № 27
- •Високомолекулярні сполуки вмс
- •Лекція № 28
- •Набухання в технології харчових виробництв.
- •Перелік літератури
Загальна характеристика і властивості розчинів
Існують два види розчинів: дійсні та дисперсні.
Розчинами називають багатокомпонентні системи, в яких одна або декілька речовин розподіляються в іншій речовині - розчиннику. Фізична хімія вивчає властивості дійсних розчинів.
Дійсними називають розчини, в яких речовина розчиняється до молекул та іонів.
Якщо речовина розчиняється до іонів, то такі розчини називають розчини електролітів.
Якщо речовина розчиняється до молекул, то такі розчини називають розчинами неелектролітів.
Розчини електролітів проводять електричний струм, а неелектроліти не проводять. До електролітів відносяться розчини кислот, солей та гідроксидів. До неелектролітів - органічні розчини: цукру, крохмалю, карбонових кислот.
Дисперсними системами називають розчини, в яких речовина розчиняється до колоїдних часток - міцел. Дисперсні системи поділяють на грубодисперсні (крейда, борошно у воді, цементний розчин) і колоїдно-дисперсні (AgСІ, Fe(ОН)3) .
Способи вираження концентрації.
1. Масова доля речовини - це безрозмірна фізична величина, яка дорівнює підношенню маси речовини до загальної маси розчину.
![]() =
=
![]() 100%
(в %)
100%
(в %)
2. Молярна концентрація виражається числом молей розчиненої речовини в 1 дм3.
СМ
=
![]() (г/моль)
(г/моль)
3. Еквівалентна концентрація (концентрація еквівалентів) виражається числом моль-еквівалентів розчиненої речовини в 1 дм3 розчину.
Сэ
=
![]() (моль
екв/дм3)
(моль
екв/дм3)
За типом розчини бувають: газові, рідкі, тверді. Газові розчини - суміш газів.
Тверді розчини - сплави металів, солей. Рідкі розчини газу у рідині, рідини у рідині, твердої речовини у рідині. Розчинність газів у рідині залежить від температури і тиску. Чим нижче температура і вищий тиск, тим краще розчинність. На відміну від газів розчинність рідини у рідині може бути різноманітною: безмежна - етиловий спирт у воді, обмежена - анілін у воді, повна нерозчинність - ртуть у воді.
Розчинність рідини залежить від температури: чим вище температура, тим більша розчинність рідини в іншій. Підвищення температури дає можливість перевести обмежену розчинність в безмежну, та температура, при якій обмежена розчинність переходить у безмежну, називають критичною.
Критична температура - це характеристика кожної рідини. По критичній температурі у харчовій промисловості відрізняють вершкове масло від маргарину.
Тверді тіла у рідких розчинниках розчиняються обмежено. Розчинність підвищується з підвищенням температури.
Але існують деякі винятки: існують речовини, які не змінюють свою розчинність з підвищенням температури і існують речовини, розчинність яких збільшується із зниженням температури.
Розчинність твердих речовин у розчинах вперше вірно пояснив Менделєєв у своїй гідратній теорії. Відповідно до гідратної теорії процес розчинення можливо пояснити на такому прикладі, якщо кристал NaСІ занурити у воду, то розчинення піде таким чином: відповідно до теорії Менделєєва процес розчинення здійснюється за такими стадіями:
1) гідратація іонів (взаємодія з молекулами води).Виникають сили когезії. Супроводжується виділенням тепла, оскільки утворюються нові зв'язки.
2) Руйнування сил когезії (руйнування кристалічної решітки супроводжується поглинанням тепла).
3)Утворення гідратів і розподіл їх у масі розчинника.
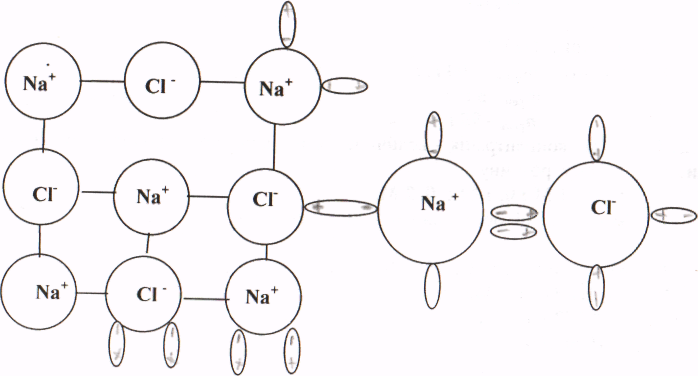
Гідрати - нестійкі фізико - хімічні з'єднання. Рушійною силою є кінетична енергія розчинника.
Теплота розчинення - це сума теплоти, яка витрачається на руйнування сил когезії та тепла, яке виділяється при утворенні сил адгезії.
Процес розчинення завжди супроводжується зміною об’єму. Об'єм може зменшитися, збільшитися чи залишитися незмінним. Це залежить від сил адгезії та когезії. Якщо сили адгезії більше сил когезії, то об'єм зменшується, і процес супроводжується виділенням тепла. Якщо сили адгезії менше сил когезії, то об'єм збільшується, і процес супроводжується поглинанням тепла. Якщо сили адгезії та когезії рівні, то об'єм не змінюється і тепловим ефектом процес не супроводжується.
