
- •1. История развития микробиологии: описательный, физиологический этапы.
- •2. Современная классификация микроорганизмов.
- •3. Размеры микроорганизмов.
- •4. Систематика прокариот, для представителей домена Bacteria.
- •5. Морфология микроорганизмов, на примере представителей домена Bacteria.
- •6. Ядерная зона и генетический аппарат прокариотной клетки.
- •Генетический аппарат кишечной палочки
- •Разнообразие типов генетического аппарата прокариот
- •7. Плазмиды.
- •8. Клеточная стенка грамположительных бактерий.
- •9. Клеточная стенка грамотрицательных бактерий.
- •10. Необычные клеточные стенки прокариот. Прокариоты без клеточной стенки.
- •11. Функции клеточной стенки прокариот.
- •12. Цитоплазматическая мембрана, строение, функции.
- •13. Внутрицитоплазматические мембраны прокариот. Включения и запасные вещества.
- •14. Цитозоль и рибосомы.
- •Рибосомные рнк
- •Рнк малой субъединицы
- •Рнк большой субъединицы
- •Низкомолекулярные компоненты
- •15. Капсулы, слизистые слои, чехлы.
- •16. Покоящиеся формы прокариот.
- •17. Процесс споруляции у прокариот.
- •19. Жгутики. Расположение и функции.
- •20. Строение жгутика у грамположительных и грамотрицательных бактерий. Синтез жгутика.
- •21. Скольжение, как тип движения бактерий.
- •22. Таксис. Виды таксиса у бактерий.
- •23. Размножение прокариот.
- •24. Разделение бактерий на группы в зависимости от температурных и pH оптимумов роста, от наличия кислорода в среде.
- •25. Питательные и селективные среды для роста бактерий.
- •26. Количественная оценка роста микроорганизмов. Чистые и смешанные культуры микроорганизмов.
- •27. Получение музеев микроорганизмов.
- •28. Периодическое культивирование микроорганизмов.
- •29. Проточное (непрерывное) культивирование микроорганизмов.
- •30. Контроль роста микроорганизмов.
- •31. Вирусы. Репродукция вирусов.
- •32. Бактериофаги. Морфология и химический состав.
- •33. Взаимодействие бактериофагов с бактериальной клеткой. Вирулентные и умеренные бактериофаги.
29. Проточное (непрерывное) культивирование микроорганизмов.
При
непрерывном способе культивирования
микроорганизмы постоянно получают
приток свежей стерильной питательной
среды, а из аппарата непрерывно отбирается
биомасса вместе с образуемыми метаболитами
(такой способ культивирования можно
назвать «открытой» системой). При
непрерывном культивировании микроорганизмы
не должны испытывать недостатка в
питательном субстрате, так как скорость
его притока сбалансирована со скоростью
выхода биомассы. Кроме того, культура
не отравляется продуктами обмена веществ
– в этом большое преимущество непрерывного
способа культивирования по сравнению
с периодическим. Непрерывно-проточное
культивирование дает возможность
поддерживать постоянные условия роста
микроорганизмов за счет ограничения
какого-то одного фактора среды. 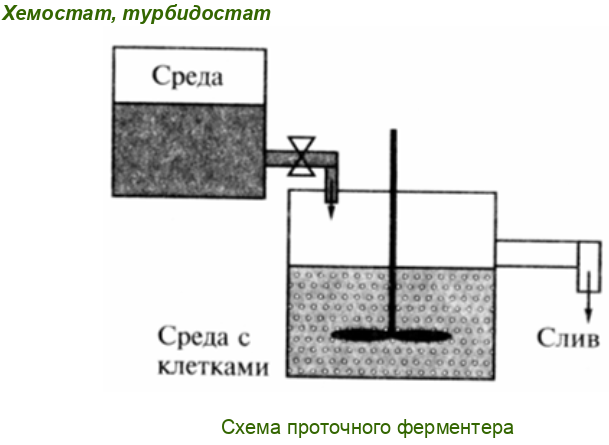
Рост в хемостате. При культивировании в условиях хемостата поддерживается постоянная концентрация одного из компонентов среды (например, углерода или азота). Благодаря этому в условиях хемостата поддерживается постоянная скорость роста культуры. Культура микроорганизма находится в условиях динамического равновесия. В хемостате скорость разбавления питательной среды является постоянной в соответствии с заданной плотностью популяции. По мере поступления питательного раствора из него вытекает суспензия микроорганизмов с той же скоростью. Изменяя скорость разбавления, можно получать режимы, обеспечивающие различную скорость роста.
Рост в турбидостате. Работа турбидостата основана на поддержании постоянной концентрации живых клеток. В сосуде для культивирования все питательные вещества содержатся в избытке, а скорость роста бактерий приближается к максимальной. В нем подача питательной среды осуществляется по команде фотоэлектрического элемента, регистрирующего оптическую плотность культуры в ферментере. Скорость разбавления устанавливается автоматически в соответствии с заданной плотностью популяции. Когда плотность биомассы увеличивается относительно некоторого выбранного уровня, фотоэлемент, соединенный системой реле, подает свежую питательную среду.
Недостатки хемостата:
1. Технические трудности, в первую очередь связанные с созданием асептических условий.
2. Не во всех случаях непрерывный процесс предпочтительнее периодического, поскольку при низкой удельной скорости роста биомассы периодический процесс по эффективности не уступает непрерывному и более выгоден, т. к. его проще осуществить.
3. Интенсивный биосинтез многих продуктов метаболизма происходит при медленном росте биомассы, поэтому в периодических процессах концентрация целевого продукта в культуральной жидкости обычно выше, чем в непрерывных, что существенно повышает эффективность стадий выделения и очистки продукта.
30. Контроль роста микроорганизмов.
Рост микроорганизмов необходимо сдерживать, если их развитие приводит к нежелательным последствиям. Так, микробная активность может вызывать инфекционные заболевания, а также порчу продуктов и материалов. В таких случаях используют антимикробные агенты. Как правило, воздействие этих веществ дозозависимое, т.е. чем выше доза, тем сильнее влияние.
Агенты, приводящие к остановке роста микроорганизма или к его уничтожению, называют бактериостатическими или бактерицидными соответственно.
Один и тот же антимикробный агент может при низкой концентрации оказывать бактериостатическое действие, а при высокой — убивать микроорганизмы. Бактериостатическое действие обратимо: при снижении концентрации или удалении такого антимикробного агента микроорганизм возобновляет свой рост. Для стерилизации следует применять бактерицидные антимикробные агенты с широким спектром действия. Следует помнить, что для некоторых микроорганизмов эти вещества, наоборот, могут быть источниками углерода и энергии.
Все антимикробные агенты для удобства разделяют на несколько групп в соответствии с механизмом их действия.
В первую группу включают вещества, повреждающие поверхностные структуры клетки. Например, бактерицидное действие 70%-го этанола связано с коагуляцией белков. Поверхностно-активные вещества нарушают избирательную проницаемость цитоплазматической мембраны.
Вторая группа веществ действует как ферментные яды, нарушая пространственную структуру белков и функционирование ферментов. К этой группе относятся тяжелые металлы (медь, ртуть, свинец), связывающиеся с SH-группами белков. Цианид и СО функционируют как дыхательные яды и др.
Третья
группа
— это аналоги нормальных метаболитов,
которые конкурируют с ними за каталитический
центр фермента. Из-за схожести структуры
аналоги могут взаимодействовать с
каталитическим центром фермента и
занимать место нормального метаболита.
Например, сульфаниламид является
структурным аналогом пара-аминобензойной
кислоты (ПАБК, рис. 5.9). 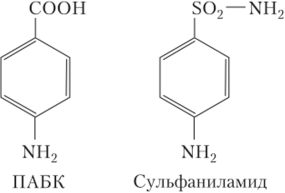
Четвертая группа — это вещества, нарушающие нормальные процессы синтеза биополимеров. Например, многие антибиотики оказывают влияние на разные этапы белкового синтеза. Так, стрептомицин и неомицин подавляют связывание аминокислот между собой, пенициллин и цефалоспорин нарушают процесс образования пептидогликана.
Вещества, оказывающие опосредованное, обычно бактериостатическое действие, относят к пятой группе. Это, например, NaCl и сахароза, в высоких концентрациях замедляющие развитие микроорганизмов из-за снижения активности воды. Такие вещества часто используют при консервировании продуктов.
