
- •Вопрос 1. Особенности геологической истории и развития биосферы в докембрийский период. Докембрийский период
- •Ранний архей. Возникновение протоконтинентальной коры (4,0‑3,15 млрд лет)
- •Поздний архей. Формирование континентальной коры (3,15 – 2,50 млрд лет)
- •Вопрос 2. Причины возникновения кислотных дождей и меры по снижению опасности. Кислотные дожди
- •Источники поступления оксидов серы
- •Источники поступления оксидов азота
- •Механизм образования кислотных осадков
- •Воздействие кислотных дождей на экосистемы и людей
- •Меры по защите окружающей среды от кислотных дождей
- •Кислотообразующие выбросы мегаполисов
Механизм образования кислотных осадков
Оксиды серы и азота после химических реакций образуют кислоты.
Основная масса диоксида серы (сернистый ангидрит) во влажном воздухе превращается в полигидрат SO2·nH2O, а затем окисляется до серной кислоты
2H2SO3 + O2 = 2H2SO4.
Другой путь – образование серной кислоты после фотохимического окисления сернистого ангидрита
2SO2 + O2 = 2SO3 и далее SO3 + H2O = H2SO4.
Процесс образования азотистой и азотной кислот можно записать следующим образом
2NO2 + 2H2O = H2NO3 + H2NO2.
Аэрозоли кислот конденсируют пары воды и становятся причиной кислотных осадков.
В балансе образования кислотных дождей следует учитывать нейтрализацию аммиака, важнейшими источниками которого являются рисовые поля, крупный рогатый скот и таяние гидрата метана, который содержится в многолетней мерзлоте. Возможные реакции нейтрализации кислот таковы:
2NH3 + H2SO4 = (NH4)2SO4 и NH3 + HNO3 = NH4NO3.
Существуют два вида кислотных дождей, которые пока не отслеживаются мониторингом атмосферы.
Один связан с хлором и метаном. Хлор поступает в атмосферу с выбросами химических предприятий, при сжигании отходов и т.д. Взаимодействие радикалов хлора с метаном ведет, в конечном счете, к образованию соляной кислоты.
Более опасны выбросы фтороводорода, которые могут происходить при производстве алюминия и стекла. Он хорошо растворяется в капельках воды и дает в итоге аэрозоли плавиковой кислоты.
В Западной Европе и Северной Америке средняя кислотность осадков составляет 4,5-5. Туманы имеют нередко кислотность 2,5-3. Площадь территорий, на которых выпадают эти осадки, достигает 10 млн км2. В России критические нагрузки отмечаются в промышленных областях: Ленинградской, Московской и др.
Особенность кислотных дождей – трансграничный перенос загрязнения на сотни и даже тысячи километров. Почти все страны являются одновременно «экспортерами» и «импортерами» выбросов. В подкисление природной среды России основной вклад приходится на Украину, Польшу и Германию. Россия оказывает негативное влияние на природу стран Скандинавии. Соотношения здесь такие: с Украиной – 1:17, Польшей 1:32, Норвегией 7:1.
Воздействие кислотных дождей на экосистемы и людей
Последствия кислотных дождей показаны на рис. 26.
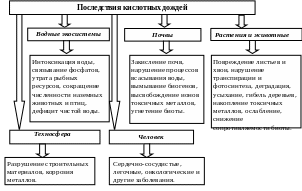
Рис. 1. Воздействие кислотных дождей на биосферу и человека
В гидросфере жизнь богаче и разнообразней в нейтральной и слабощелочной среде. Водоемы с очень кислыми водами необитаемы, как необитаемы и водоемы с pH>11. Отсюда ясен основной результат кислотных дождей – снижение продуктивности водоемов. Побочные эффекты связаны с ионами тяжелых металлов (Cd, Pb и др.).
Опасен гидрооксид алюминия. Взаимодействуя с кислотой, он образует растворимое соединение
Al(OH)3 +3H+ = Al3+ + 3H2O.
Концентрация алюминия 0,2 мкг/л смертельна для рыб. Для продуцентов алюминий вреден по другой причине. Фосфаты, соединяясь с алюминием
Al3+ + PO43– → AlPO4,
выпадают в осадок и становятся недоступными для фитопланктона и водорослей.
Гидрокарбонат-ион HCO3–, образующийся при диссоциации угольной кислоты, нейтрализует кислоты и основания, а потому карбонатные воды отличаются высокими буферными свойствами. Однако большинство пресных водоемов северных районов отличает слабокислая реакция (7>pH>4), а потому их чувствительность к кислотным дождям повышена. Степень опасности зависит и от горных пород, слагающих ложе водоемов. В Канаде, Скандинавии и на Северо-Западе России подстилающими породами являются граниты, как следствие, воды имеют слабокислую реакцию и чувствительны к кислотным дождям.
По данным Госкомэкологии в России многие реки и озера относится к загрязненным. При таком положении кислотные осадки мало меняют характеристики вод.
Почвенные организмы менее чувствительны к понижению pH, но и они угнетаются возрастающей кислотностью, особенно восприимчивы азотфиксирующие бактерии и грибы.
Для растений подкисление почв ведет к нарушению корневой системы, а прямое воздействие кислотных осадков на листья – к разрушению хлорофилла. Больше всего страдают хвойные и дубовые леса. В то же время повышение содержания азота может на первой стадии стимулировать растения, однако, по мере увеличения подкисления происходит угнетение растительности.
Наибольший урон кислотные дожди нанесли лесам Центральной Европы. Так в Германии поражено около 35% лесов.
Строительные материалы под воздействием кислотных осадков разрушаются быстрее, т.к. вещества, содержащие карбонат кальция (известняк, мрамор и др.), реагируют с кислотой:
CaC03 + H2SO4 = Ca2+ + SO42– +CO2 +H2O или CaC03 + H2NO3 = Ca2+ + NO3– +CO2 +H2O.
Под действием кислотных дождей выщелачиваются не только карбонаты, но и силикаты. При pH=3‑4,5 ионы алюминия вымываются из кристаллической решетки плевого шпата – основы бетона и других строительных материалов:
3KAlSi3O8 + 12H2O + 2H+ = Al3Si3O10(OH)2 + 6H4 SiO4 + K+,
3KAlSi3O10(OH)2 + 18H2O + 2H+ = Al3Si3(H2O)3 + 6H4 SiO4 + K+.
Железо особенно подвержено действию кислотных дождей. Вначале на поверхности изделий возникает корка гигроскопичного сульфата железа, который окисляется и превращается в ржавчину
FeSO4 + H2O + O2 → Fe(OH)SO4.
