
- •Симетрія – основні поняття.
- •Матерія та її єдність із законами симетрії.
- •Чотири типи взаємодій та їх характеристики.
- •Симетрія фізичних законів.
- •Симетрія законів збереження.
- •Фізична картина світу.
- •1) Місце фізики у сучасному житті.
- •2) Підрозділи фізики та предмети їх досліджень.
- •4) Матеріальна точка (мт). Визначення положення мт у просторі, радіус-вектор.
- •5) Написати і охарактеризувати кінематичні рівняння поступального і о бертального рухів.
- •6)Характеристики руху. Середня та миттєва швидкість. Нормальне та тангенціальне прискорення. Одиниці виміру швидкості та прискорення.
- •7) Види руху
- •8) Зв'язок лінійних і кутових фізичних величин.
- •10. Третій закон Ньютона.
- •11. Робота та потенціальна енергія. Зв'язок сили з потенціальною енергією мт. Розрахунок роботи.
- •12. Закон збереження енергії.
- •13. Однорідне силове поле. Рух мт в однорідному силовому полі.
- •18. Правило важелів Архімеда
- •19. Дисипативна енергія
- •14. Визначення коефіцієнта вязкості
- •16. Теорія подібності та її використання у фізико-технологічних процесах
- •9) Імовірність розподілу молекул за швидкостями
- •10. Теорія хімічної будови бутлерова.
- •11. Структурна і просторова ізомерія. Фізичні методи визначеннях структури.
- •12. Основні типи молекулярних зв’язків – іонний, ковалентний. Квантово-механічне пояснення ковалентного зв’язку.
- •14. Явище переносу в газах.
- •Нульове начало термодинаміки.
- •Внутрішня енергія ідеального газу.
- •Перше начало термодинаміки. Робота газу при сталому тиску.
- •Теплоємність газу за сталого обєму і сталого тиску.
- •5. Закон дюлонга та пті
- •9. Питома теплота плавлення та пароутворення речовини
- •10. Робота теплових двигунів та холодильників
- •12. Третій закон термодинаміки
- •12. Третій закон термодинаміки
- •Причини утворення поверхневого шару рідини.
- •Розрахунок висоти підняття рідини в капілярі
- •Формула Лапласа і її характеристика
- •Електризація тіл. Два роди зарядів.
- •Поле точкового заряду. Силові лінії електричного поля. Геометрична інтерпретація полів силовими лінями.
- •Теорема Гауса та її застосування до тіл простої геометричної форми.
- •10. Поведінка провідників в електричному полі. Електроємність провідників. Одиниці вимірювання електроємності.
- •11. Конденсатори. Ємність плаского, сферичного конденсатора.
- •12. Паралельне та послідовне з’єднання конденсаторів.
- •13.Енергія плаского конденсатора
- •Класифікація матеріалів за електричними властивостями. Провідники, діалектрики, напівпровідники і надпровідники.
- •Електричний диполь , дипольний момент, поле диполя.
- •Теорема гауса.
- •Полярні і неполярні молекули. Поляризація речовини.
- •Вплив речовини діалектрика на електричне поле.
- •Основна задача електростатики.
- •Пєзоелектрики, сегнетоелектрики, піроелектрики.
- •Робота, енергія, обємна густина енергії.
- •1) Постійний електричний струм. Середня швидкість спрямованого руху електронів.
- •2) Густина струму. Закон Ома у локальній формі.
- •3) Провідність та питомий опір речовини.
- •5) Паралельне та послідовне з’єднання резисторів.
- •6) Перше та друге правило Кірхгофа (на прикладах)
- •7) Електричні прилади та їх використання.
- •12) Класична електронна теорія металів
- •95. Робота електростатичного поля з переміщення одиничного заряду.
- •96. Потенціал. Різниця потенціалів. Еквіпотенціальні поверхні. Одиниці вимірювання потенціалу.
- •101. Дослід Міллікена-Йоффе.
Причини утворення поверхневого шару рідини.
Кожна молекула, розміщена всередині об’єму рідини, рівномірно оточена сусідніми молекулами і взаємодіє з ними, а рівнодійна цих сил дорівнює нулю. В поверхневому шарі в наслідок неоднорідності оточення на молекулу діє сила R, не скомпенсована силами з боку інших молекул рідини. Внаслідок цього рідина в поверхневому шарі перебуває в розтягнутому напруженому стані. Густина рідини в цьому шарі менша, ніж усередині. Молекули поверхневого шару перебувають на більших відстанях одна від одної, ніж молекули всередині рідини, тому їх потенціальна енергія більша, ніж в інших молеку
Сила поверхневого натягу спрямована по дотичній до поверхні рідини, перпендикулярно до ділянки контура, на який вона діє і пропорційна довжині цієї ділянки.
Коефіцієнт пропорційності γ - сила, яка припадає на одиницю довжини контуру - називається коефіцієнтом поверхневого натягу. Він вимірюється в (ньютонах на метр) Н/м.
Відношення поверхневої енергії Un будь-якої частини поверхні рідини до площі S цієї поверхні називається коефіцієнтом поверхневого натягу
![]()
Явище
виникнення сил, що перешкоджають
збільшенню площі вільної поверхні
рідини:
![]()
Енергетичне (термодинамічне) визначення: поверхневий натяг - це питома робота збільшення поверхні при її розтягуванні за умови сталості температури.
Силове (механічне) визначення: поверхневий натяг - це сила, що діє на одиницю довжини лінії, яка обмежує поверхню рідини.
Явища піднімання чи опускання рідини по тоненьких трубках-капілярах
називаються капілярними.
-Якщо сили притягання між молекулами рідини і твердого тіла більші ніж сили
притягання між самими молекулами рідини, то рідина змочує поверхню твердого тіла.
Якщо капіляр змочується рідиною, то в ньому утворюється вгнутий меніск і тиск
на рідину стає меншим, ніж у широкій посудині.
- Якщо сили притягання між самими молекулами рідини більші, ніж сили притягання
між молекулами рідини і твердого тіла, то рідина не змочує поверхню твердого тіла.
Якщо капіляр не змочується рідиною, то в ньому утворюється опуклий меніск і
тиск на рідину стає більшим, ніж у широкій посудині.
Розрахунок висоти підняття рідини в капілярі
ρgh=
 => h=
=> h=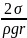
Формула Лапласа і її характеристика

Поверхне́во-акти́вні речови́ни (ПАР, сурфактанти, детергенти) — хімічні речовини, які знижують поверхневий натяг рідини, полегшуючи розтікання і знижуючи поверхневий натяг на межі двох рідин. Це речовини, молекули або йони яких концентруються під дією молекулярних сил (адсорбуються) біля поверхні розділу фаз і знижують енергію поверхневу. У вужчому значенні ПАР здебільшого називають речовини, що знижують поверхневий натяг на межі поділу: рідина (вода) — повітря (пара), рідина (вода) — рідина (масло), рідина — тверда поверхня.Поверхнево-активні речовини — зазвичай амфіфільні органічні сполуки (термін амфіфільні означає, що вони містять як гідрофільні групи («хвости»), так і гідрофобні групи («головки»). Через таку будову вони розчинюються як у неполярних жирах і органічних розчинниках, так і в полярних середовищах (воді).
Поверхнево-неактивні речовини – підвищують поверхневий натяг речовини.
Рідкі кристали
Рідкий кристал - проміжна фаза (мезофаза) між ізотропною рідиною і кристалічним твердим тілом. Рідкі кристали це флюїди, молекули яких певним чином впорядковані, тобто існує певна симетрія. Як наслідок, існує анізотропія механічних, електричних, магнітних та оптичних властивостей речовин цього класу. Поєднуючи властивості рідин та твердих тіл (текучість, анізотропія), рідкі кристали проявляють специфічні ефекти, багато з яких не спостерігаються у рідинах та твердих тілах. Зокрема, в рідких кристалах спостерігається подвійне променезаломлення, флексоелектричний ефект, перехід Фредерікса.
Застосування рідких кристалів. Найпопулярніше поле для використання рідких кристалів — рідкокристалічні дисплеї..Крім цього, рідкі кристали застосовують при виготовленні термодавачів, детекторів НВЧ-випромінювання тощо.
Полімери — природні та штучні сполуки, молекули яких складаються з великого числа повторюваних однакових або різних за будовою атомних угруповань, з'єднаних між собою хімічними або координаційними зв'язками в довгі лінійні або розгалужені ланцюги. Структурні одиниці, з яких складаються полімери називаються мономерами.
природні або натуральні, до яких відноситься велика група (білки, крохмаль, целюлоза, натуральний каучук, природний графіт та ін.).
синтетичні — утворені синтезом з низькомолекулярних речовин — мономерів (поліетилен з етилену, полістирол із стиролу). Це ведуча група, тому що синтез дозволяє цілеспрямовано регулювати склад і властивості.
штучні — утворюються з природних полімерів шляхом їхньої хімічної модифікації (наприклад, при взаємодії целюлози з азотною кислотою утворюється нітроцелюлоза).
Полімерні матеріали мають комплекс характеристик, які при умілому їхньому використанні забезпечують ефективні експлуатаційні властивості виробів та рентабельність їхнього виробництва.
Фазові переходи. Метастабільність Фазовий перехід першого роду – це ф.п., що супроводжується стрибкоподібними змінами внутрішньої енергії та об’єму системи і отже супроводжується поглинанням або виділенням теплоти переходу. Фазовий перехід другого роду – ф.п., при якому внутрішня енергія та об’єм системи залишаються незмінними, теплоти фаз переходу немає, але змінюється стрибком теплоємність термічного коефіцієнту. Метастабільний стан — це такий стан, де не повністю стійкі стани системи з великим шляхом частинок, яка здатна до фазового перетворення першого роду.
Квантова рідина. Надплинність Квантова рідина, рідина, властивості якої визначаються квантовими ефектами. Прикладом До. ж. є рідкий гелій при температурі, близькій до абсолютного нуля. Квантові ефекти починають виявлятися в рідині при досить низьких температурах, коли довжина хвилі де Бройля для часток рідини, обчислена по енергії їх теплового руху, стає порівнянною з відстанню між ними. Надплинність — стан речовини, в якому вона втрачає в'язкість. Спостерігається виключно в рідких гелію-4 й гелію-3.
ЕЛЕКТРОСТАТИЧНЕ ПОЛЕ ТА ЙОГО ЗАКОНИ
