
- •1. Материальный баланс химических реакций и его характеристика
- •2. Безразмерные характеристики материального баланса
- •3. Концентрация, парциальное давление и мольные доли
- •4. Скорость превращения веществ, скорость реакции и кинетические уравнения
- •5. Экспериментальные установки для кинетических исследований и характеристические уравнения идеальных реакторов
- •6. Идеальный периодический реактор (рпс) и его характеристическое уравнение
- •7. Реактор идеального вытеснения (рив) и его характеристическое уравнение
- •8. Реактор полного идеального смешения (рпс) и его характеристическое уравнение
- •9. Гипотеза о схеме превращений и способы её подтверждения
- •10. Механизм и кинетика элементарных реакций
- •11. Механизм и кинетика сложных реакций
- •12. Основы кинетического исследования
- •13. Интегральный метод обработки опытов по уравнениям с одним неизвестым параметром
- •13.1. Необратимые простые реакции в периодических условиях.
- •13.2. Необратимые простые реакции в условиях идеального вытеснения.
- •13.3 Обратимые реакции в интегральных условиях.
- •14. Дифференциальный метод обработки для простых и обратимых реакций
- •15. Интегральные методы исследования параллельных реакций
- •15.1. Параллельные необратимые реакции одинакового порядка
- •15.2. Метод конкурирующих реакций
- •16. Интегральные методы исследования последовательных реакций
- •17. Исследование влияния температуры
- •18. Удельная производительность реакторов и их сочетаний
- •18.1. Реакторы ипр
- •18.2. Непрерывно-действующие реакторы
- •18.3. Реакторы идеального вытеснения
- •18.4.Реакторы полного смешения
- •18.5. Секционированные реакторы и каскады реакторов
- •18.6. Сочетания реакторов
- •19. Оптимизация процессов
- •19.1.Последовательные необратимые реакции:
- •19.2. Последовательно-параллельные реакции
- •20. Влияние типа реакторов и способа введения реагентов на селективность процесса
- •21. Экономические критерии и их применение для оптимизации процесса
- •Вопросы для контроля
- •Теория химико-технологических процессов органических веществ
- •625000, Тюмень, ул. Володарского, 38.
- •6 25039, Тюмень, ул. Киевская, 52.
7. Реактор идеального вытеснения (рив) и его характеристическое уравнение
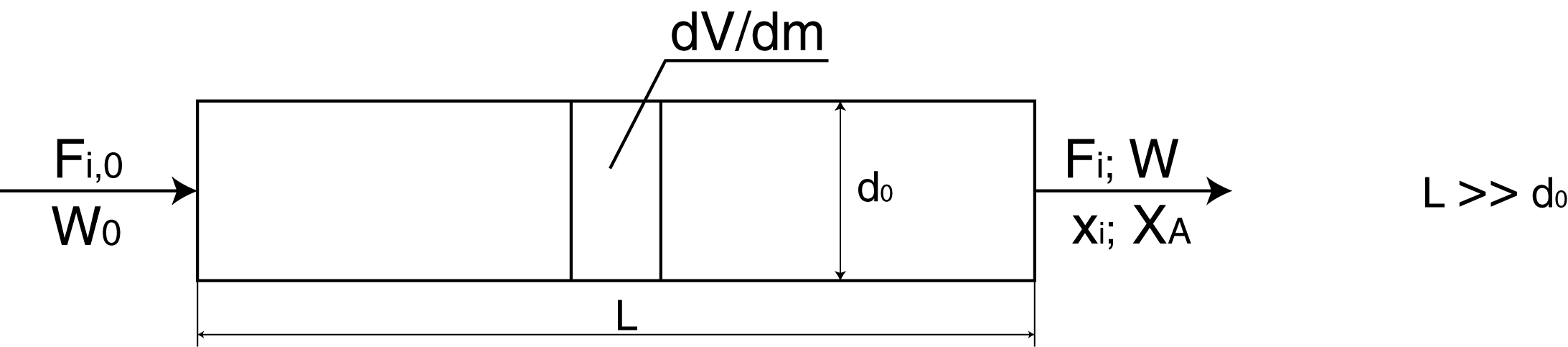
Рис. 7.1. Схема реактора идеального вытеснения.
Реактор идеального вытеснения (рис. 7.1) является моделью непрерывно действующих аппаратов вытеснения, в которых реакционная масса движется вдоль оси, вытесняя последующие слои.
Условием идеальности РИВ является отсутствие продольного перемешивания. В стационарных условиях при постоянстве скорости подачи и состава исходной смеси, а также при постоянстве условий теплообмена каждый элемент пребывает в таком реакторе в течении одинакового времени, а концентрация и температура в каждом поперечном сечении остаются постоянными. При этом, в отличие от периодического реактора, концентрация веществ изменяется не во времени, а по длине реактора (рис. 7.2).
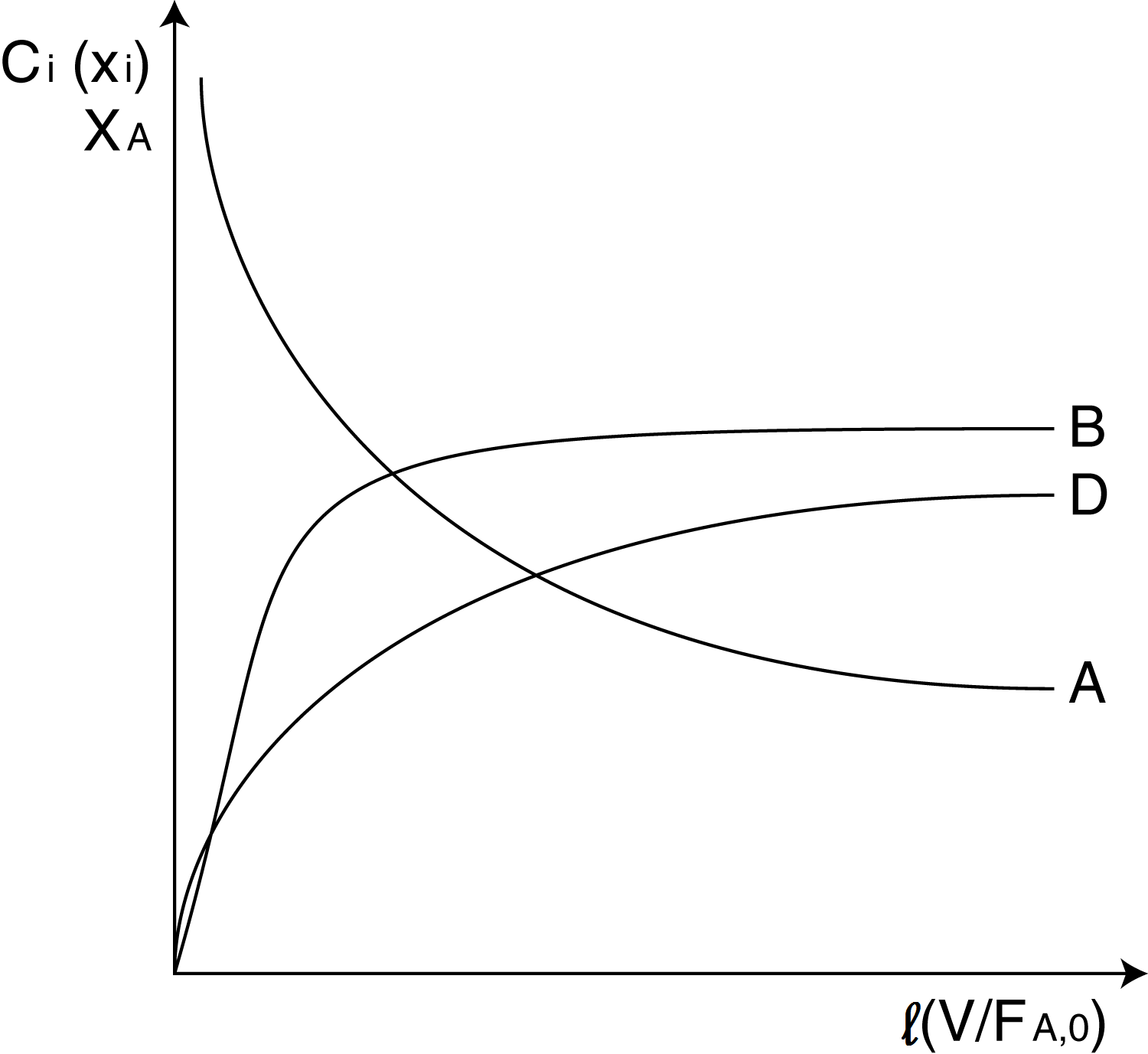
Рис. 7.2. Концентрационные кривые реактора идеального вытеснения.
l – величина обратная мольной нагрузке на единицу мольного объёма в единицу времени. Это позволяет составить уравнение материального баланса для бесконечно малого элемента объёма, поперечного потоку реагентов:
dFi = ri ∙ dV;
это следует из уравнения (4-4).
7.1. Гомогенные реакции. После разделения переменных интегрирования получим общее характеристическое уравнение:
![]() ; (7-1)
; (7-1)
Уравнение (7-1) можно записать для субстрата А:
![]() ; (7-2а)
; (7-2а)
dFA,0 = –FA,0 dXA
Разделим обе части уравнения (7-1) на W0:
![]() ;
(7-2)
;
(7-2)
V – объём;
W0 – объём/время;
(V/W0) = rист – истинное время контакта.
![]() ;
;
В уравнении (7-2) V/W0 имеет размерность времени и при отсутствии насадки в реакторе или за вычетом её объёма равно истинному времени контакта.
Очевидно, что в этом случае уравнения (6-3) и (7-2) для периодического реактора и реактора вытеснения соответственно полностью совпадают. Более общую форму уравнения для РИВ верную и для изменяющего объема смеси можно вывести изменяя Fi в уравнении (7-1) через химические выходы ключевых веществ.
![]() ;
;
Это из уравнения (2-6) при условии, что Fi,0 = 0
Подставив значение Fi в уравнение (7-1) получим:
![]() ; (7-3)
; (7-3)
Это уравнение годится и для основного реагента A, если полагать, что его выход xA = 1 – XA.
В левой части уравнения (7-3) находится величина обратная мольной нагрузке единицы объема реактора по основному реагенту в единицу времени и имеющая размерность:
V/FA,0 = [(объем)(время)(моль)–1];
Эта величина называется условным временем контакта и является временной характеристикой гомогенных непрерывных процессов, заменяющей время реакции при периодических условиях.
7.2. Гетерогенно-каталитические реакции. Для гетерогенно-каталитических реакций материальный баланс можно составить для микромассы катализатора.
dFi = ridmK;
Разделив переменные, выведем характеристические уравнения:
![]() ; (7-4)
; (7-4)
Разделим обе части на W0:
![]() ;
;
Отсюда можем выразить характеристическое уравнение гетерогенно-каталитических реакций:
![]() ; (7-5)
; (7-5)
Чаще всего используют уравнение. в левой части которого находится величина, обратная мольной нагрузке единицы массы катализатора по основному реагенту в единицу времени и имеющая размерность:
FА,0/mK = [(масса)(время)(моль)-1]
Эту величину также называют условным временем контакта и она является временной характеристикой непрерывных гетерогенно-каталитических реакций. Хотя она и не имеет размерности времени.
В технологии используют ещё одну временную характеристику, а именно объёмную скорость [u] = [(время)-1]. Если её выражать по объёму всей поступающей смеси, приведенному к условиям в реакторе, то u=W/V, т.е. объёмная скорость равна объёмной нагрузке единицы реакционного объёма, в единицу времени. Тогда при неизменности объёма смеси во время реакции u = τ –1ист. Объёмную скорость применяют и для характеристики гетерогенно-каталитических процессов, относя её к насыпной массе катализатора. Кроме того, её часто выражают по объёмному потоку не всей смеси, а только основного реагента и при том в нормальных условиях.
РИВ применяют для кинетических исследований реакций в потоке, особенно для газофазных процессов, в том числе гетерогенно-каталитических. К условиям идеального вытеснения близки аппараты большой длины и малого диаметра. Поэтому реактор изготавливают в виде трубки или змеевика, имеющих карманы для термопары. Для обеспечения постоянной температуры по длине реактора и диаметру его термостатируют. Ввиду трудностей с теплообменом в этом типе реактора допускается регулирование температуры с пониженной точностью до 12C. Перед началом каждого опыта через реактор пропускают 35 объёмов реакционной смеси, чтобы в аппарате установился стационарный режим. После этого накапливают пробу продуктов и анализируют её тем или иным методом. Начинают следующий опыт при других параметрах процесса, т.о. каждый опыт даёт только одну экспериментальную точку. По сравнению с периодическим условием здесь большая длительность и трудоёмкость исследований. В РИВ варьируют те же параметры, но вместо времени изменяют условное время контакта (V/FA,0 и mK/FA,0 ) Экспериментальные данные сводят в таблицы или представляют в виде кинетических кривых в координатах:
xiA(XA, Ci) – V/FA,0(mK/FA,0).
