- •1. Материальный баланс химических реакций и его характеристика
- •2. Безразмерные характеристики материального баланса
- •3. Концентрация, парциальное давление и мольные доли
- •4. Скорость превращения веществ, скорость реакции и кинетические уравнения
- •5. Экспериментальные установки для кинетических исследований и характеристические уравнения идеальных реакторов
- •6. Идеальный периодический реактор (рпс) и его характеристическое уравнение
- •7. Реактор идеального вытеснения (рив) и его характеристическое уравнение
- •8. Реактор полного идеального смешения (рпс) и его характеристическое уравнение
- •9. Гипотеза о схеме превращений и способы её подтверждения
- •10. Механизм и кинетика элементарных реакций
- •11. Механизм и кинетика сложных реакций
- •12. Основы кинетического исследования
- •13. Интегральный метод обработки опытов по уравнениям с одним неизвестым параметром
- •13.1. Необратимые простые реакции в периодических условиях.
- •13.2. Необратимые простые реакции в условиях идеального вытеснения.
- •13.3 Обратимые реакции в интегральных условиях.
- •14. Дифференциальный метод обработки для простых и обратимых реакций
- •15. Интегральные методы исследования параллельных реакций
- •15.1. Параллельные необратимые реакции одинакового порядка
- •15.2. Метод конкурирующих реакций
- •16. Интегральные методы исследования последовательных реакций
- •17. Исследование влияния температуры
- •18. Удельная производительность реакторов и их сочетаний
- •18.1. Реакторы ипр
- •18.2. Непрерывно-действующие реакторы
- •18.3. Реакторы идеального вытеснения
- •18.4.Реакторы полного смешения
- •18.5. Секционированные реакторы и каскады реакторов
- •18.6. Сочетания реакторов
- •19. Оптимизация процессов
- •19.1.Последовательные необратимые реакции:
- •19.2. Последовательно-параллельные реакции
- •20. Влияние типа реакторов и способа введения реагентов на селективность процесса
- •21. Экономические критерии и их применение для оптимизации процесса
- •Вопросы для контроля
- •Теория химико-технологических процессов органических веществ
- •625000, Тюмень, ул. Володарского, 38.
- •6 25039, Тюмень, ул. Киевская, 52.
19.2. Последовательно-параллельные реакции
Рассмотрим последовательно-параллельные реакции, в которых имеется общий для всех стадий второй реагент.
A
![]() B
B
![]() C
C
![]() … ;
… ;
В таких реакциях порядки всех реакций по второму реагенту одинаковы, поэтому в уравнении селективности, концентрации второго реагента сокращаются:
![]() ;
;
Тогда получается решение, дающее зависимость дифференциальной селективности от константы реакции. В результате селективность таких реакций зависит от соотношения СВ/СА. В этом случае степень конверсии продукта А можно регулировать мольным соотношением вступившего в реакцию реагента Y ко всему взятому реагенту А, то есть величиной YXY. Графически это может быть представлено на рис 19.2:

Рис. 19.2. Зависимость селективности последовательно параллельных реакций от степени конверсии в реакторе полного смешения.
1. k2/k1 = 1/10 k2 > k1;
2. k2/k1 = 1 k2 = k2;
3. k2/k1 = 10 k2 < k1.
Рассмотренный прием регулирования селективности используется для следующих последовательно-параллельных реакций: алкилирования, хлорирования, оксиалкилирования.
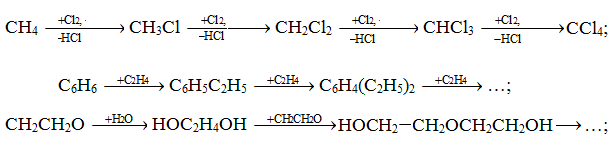
Для таких реакций селективность по первому промежуточному продукту увеличивается при недостатке второго реагента.
Рассмотрим другие способы регулирования селективности в последовательно параллельных реакциях.
Селективность можно регулировать снижая концентрацию целевого продукта в реакционной смеси, что приводит к уменьшению скорости его расходования на последующие реакции.
a) При взаимодействии газообразных реагентов с образованием жидкого целевого продукта. Последний можно разбавлять растворителем, например, реакция оксосинтеза:
СН2=СН2 + СО + Н2 СН3СН2СНО 0,5СН3СН2СН=С(СН3)СНО+ 0,5Н2О;
б) При синтезе в жидкой фазе достаточно летучего вещества. Его можно выводить из реакционной массы избытком газообразного реагента, например при получении ацетальдегида:
СН2=СН2 + 0,5О2 СН3СНО 0,5СН3СН=СН–СНО + 0,5Н2О;
Этот же прием используют при получении d-оксидов:
 Каждый
следующий продукт обладает более высокой
летучестью, поэтому давление синтеза
подбирают таким образом, чтобы СCl4
и СCl3F
находились в жидкой фазе, а CCl2F2
отгонялся из смеси по мере его образования.
Каждый
следующий продукт обладает более высокой
летучестью, поэтому давление синтеза
подбирают таким образом, чтобы СCl4
и СCl3F
находились в жидкой фазе, а CCl2F2
отгонялся из смеси по мере его образования.
20. Влияние типа реакторов и способа введения реагентов на селективность процесса
Зависимость СА(РА) = f (iV/FA)
Для любых сложных реакции, если уравнение дифференциальной селективности содержит концентрации или парциальные давления веществ, селективность должна зависеть от типа реактора. Исключением являются необратимые параллельные реакции одинакового порядка, где эта зависимость отсутствует. В то же время для идеальных реакторов ИПР и РИВ они дают одинаковую селективность.

Целевыми в одном случае является продукт В ,в другом - С.
Рассмотрим реакции в РПС, где интегральная селективность равна дифференциальной.
 ;
;
 ;
;
![]() ;
;
Интегральную
селективность для РИВ находят интегрируя
дифференциальную селективность. Покажем
это для
![]() :
:
 ;
;
![]() ;
;
![]() ;
;
 ;
;
 ;
;
![]() ;
;
 ;
;

![]()
Представим
зависимость селективности по продуктам
В и С по этим двум типам реакторов
![]() на рис. 20.1:
на рис. 20.1:
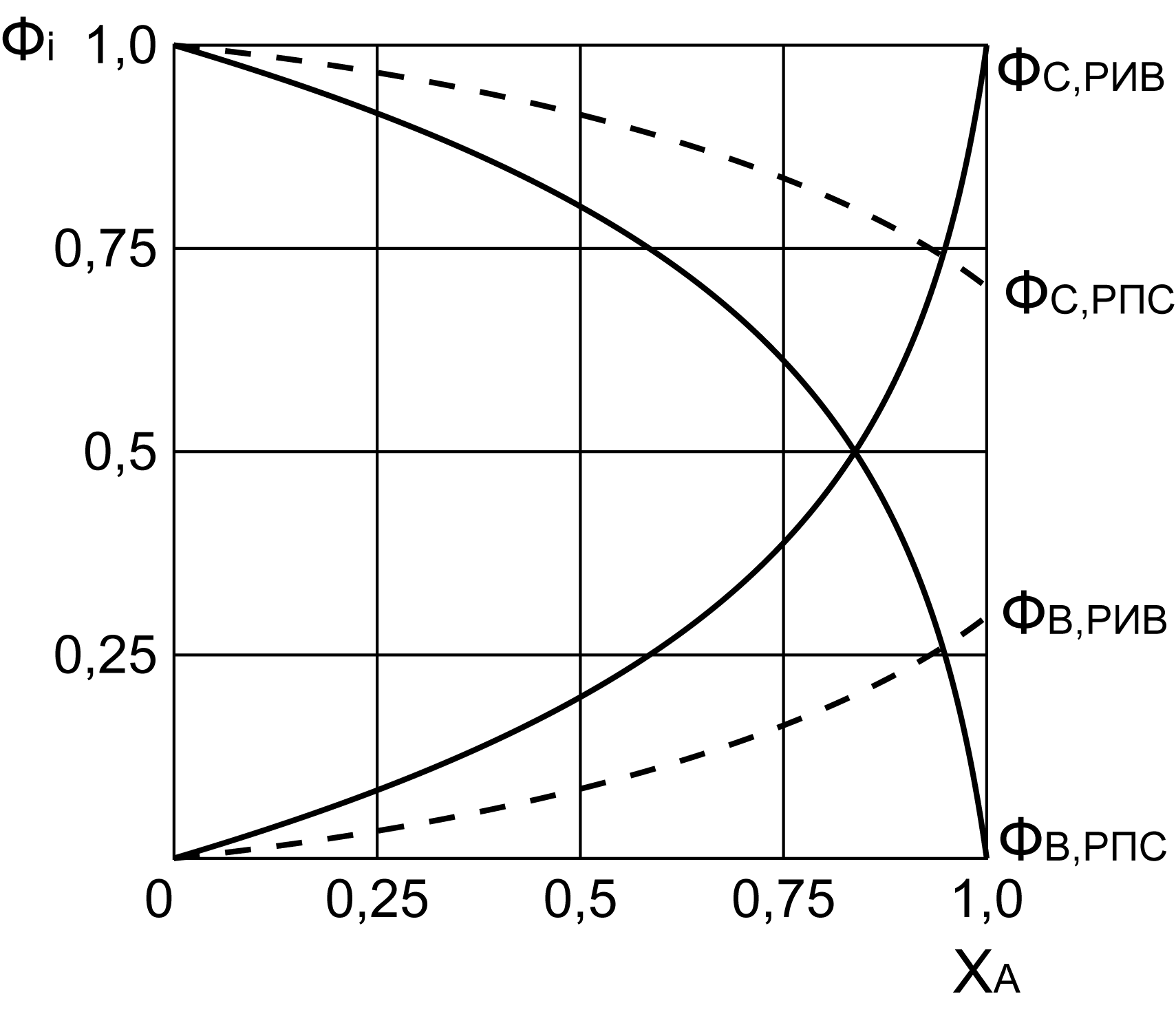
Рис. 20.1. Зависимость селективности от степени конверсии для параллельных реакций разных порядков в РПС и РИВ.
Как видно из рис. 20.1 для целевого синтеза вещества В, кроме высокой степени конверсии выгодно применение реактора полного смешения (РПС), а для целевого синтеза вещества С кроме пониженной степени конверсии выгодно использовать реактор вытеснения (РИВ). Обе реакции отличаются своим порядком, откуда следует общий вывод: для параллельных реакций, в которых целевой продукт образуется по реакции более высокого порядка, наиболее высокая селективность получается в РИВ или периодическом реакторе. РИВ или периодические реакторы более выгодны для реакции с падающей кривой селективности по степени конверсии, а РПС с возрастающей.
Кроме типа реакторов или их сочетаний на распределение концентраций по объему аппаратов, а, следовательно, и на селективность сложных реакций влияет способ введения реагентов или направление их потоков (рис 20.2)
Тип реакции |
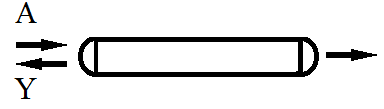
а. Периодический аппарат |
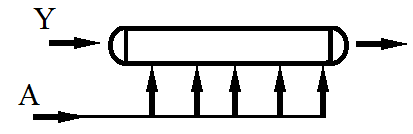
б. Ректор вытеснения |
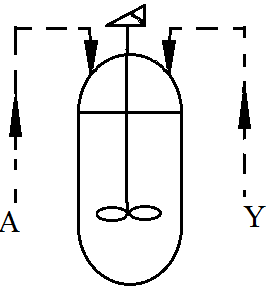
в. Реактор смешения |
|
|
|
|
|
|
|
|
|
|
|
|
Рис.20.2. Способы введения реагентов в реакторы для различных сложных реакций, оптимальные для селективности соответствующих процессов.
Для систем параллельных превращений, где целевая реакция имеет более высокие порядки по обоим реагентам, для повышения селективности выгодны более высокие их концентрации. Поэтому в периодических условиях оба реагента следует загружать в реактор сразу (1а), а для непрерывных применять идеального вытеснения (1б) или каскад аппаратов смешения (1в) с прямотоком реагентов. Это же справедливо и для последовательных превращений. При последовательно-параллельных реакциях , в которых концентрация второго реагента не влияет на селективность, способ введения реагентов безразличен: загружать его в реакцию прямотоком, секционировано (3б) или в каждый аппарат каскада (3в), но с заменой А на У и У на А.
Для систем параллельных превращений, в которых целевая реакция имеет более низкие порядки по обоим реагентам, для повышения селективности выгодны понижения их концентрации. Поэтому в периодических условиях целесообразно по степенно вводить оба реагента (2а), чтобы они успевали прореагировать с невысокой текущей концентрацией в смеси. Для непрерывных условий то же достигаются при секционированной подаче реагентов в реактор вытеснения (2б) или в аппарате полного смешения. В подобных случаях целесообразно использовать растворители или разбавители смеси.
Для параллельных реакций, в которых целевое превращение имеет более низкий порядок по одному из реагентов А и более высокий по другому – У, выгодна небольшая концентрация А и значительная концентрация У. Этого, кроме избытка второго реагента, можно достичь в периодических условиях за счет постепенного добавления реагента А ко всей загрузке реагента У (3а). Для непрерывных условий наиболее подходит аппарат идеального вытеснения с секционированной подачи реагента А (3б) или каскад реакторов смешения с введением этого реагента в каждый из аппаратов (3в).