
- •Общая характеристика современного производства алюминия и место производства глинозема в металлургии алюминия.
- •Выбор и расчет оборудования. Методы определения производительности аппарата.
- •Развернутая схема завода, работающего по способу спекания.
- •Диаграмма дробной карбонизации, факторы, влияющие на качество получаемого гидроксида алюминия.
- •Аппаратурно-технологическая схема переработки бокситов способом спекания.
- •Физико-химические основы процесса выщелачивания спеков.
- •Политермический способ получения содопродуктов из маточников после карбонизации при переработке нефелиновых руд.
- •Двухстадийное выщелачивание спеков. Аппаратура. Режим процесса.
- •Спекание шихты. Технологическая схема и аппаратурное оформление передела.
- •Комбинирование щелочных способов производства глинозема. Параллельный и последовательный вариант.
- •Взаимодействие между Al 2o3 ,Fe2o3 и CaO в системе Al 2o3-Fe2o3-SiO2-CaO.
- •Технологические схемы обескремнивания алюминатных растворов. Аппаратурное оформление.
- •Общая характеристика способа спекания. История открытия. Роль отечественных ученых в разработке и развитии способа.
- •Технологическая схема получения содопродуктов и сульфата калия при комплексной переработке нефелиновых руд.
- •Технологическая схема карбонизации. Аппаратурное оформление.
- •Взаимодействие между CaO и SiO2, CaO и Fe2o3 в системе Al 2o3-Fe2o3-SiO2-CaO.
- •Физико-химические основы процесса спекания шихты. Кинетика и механизм твердофазных реакций. Отношение составных частей шихты к нагреву.
- •Характеристика шихт глиноземного производства по способу спекания. Сфера промышленного применения.
- •Система Al 2o3-Fe2o3-SiO2-CaO. Взаимодействие между CaO и Al 2o3.
- •Технологическая схема, аппаратурное оформление отделения подготовки шихты в способе спекания.
- •3.Общая характеристика способов производства глинозема, их достоинства и недостатки
- •Система Na2o- Al 2o3- Fe2o3-SiO2. Взаимодействие между Al 2o3 и Na2co3, Fe2o3 и Na2co3, SiO2 и Na2co3.
- •Кинетика выщелачивания спеков. Понятие о первичных и вторичных потерях глинозема
- •Назначение и физико-химические основы передела обескремнивания.
- •Система Na2o- Al 2o3- Fe2o3-SiO2. Взаимодействие между Al 2o3 , SiO2 и Na2co3.
- •Физико-химические основы карбонизации. Способы карбонизации.
- •Технологическая схема передела выщелачивания в способе спекания. Аппаратурное оформление.
- •Состав и природа осадков, образующихся при обескремнивании алюминатных растворов на 1-ой и 2-ой стадии.
- •Устройство печей спекания. Пути усовершенствования их конструкции.
- •Об оптимальном гранулометрическом составе нефелиновой шихты и расходе энергии на измельчение.
- •Технологический режим и аппаратура для обескремнивания алюминатных растворов.
- •Физико-химические основы процесса карбонизации алюминатных растворов.
- •Обоснование двухстадийного обескремнивания алюминатных растворов.
- •Химизм процесса спекания бокситовых и нефелиновых шихт.
- •Влияние различных факторов на показатели второй стадии обескремнивания алюминатных растворов.
- •Характеристика шихт для спекания глиноземсодержащего сырья.
- •Назначение операции спекания глиноземсодержащего сырья.
- •О возможности замены извести карбонатным шламом на второй стадии обескремнивания алюминатных растворов.
- •Первичные и вторичные потери глинозема при выщелачивании спеков.
- •Взаимодействие основных компонентов спёка с водой, растворами соды и едкого натра (химизм процесса).
- •Назначение операции обескремнивания алюминатных растворов и ее сущность.
- •Способы карбонизации алюминатных растворов.
- •Особенности аппаратурно-технологических схем спекания бокситовых и нефелиновых шихт.
- •Экологические проблемы при переработке нефелиновых руд по способу спекания и пути их решения.
- •Качество глиноземсодержащего спёка и его физико-химические свойства.
- •Технологический режим и аппаратура для выщелачивания спёка (спекание нефелинов).
- •Влияние различных факторов на показатели карбонизации алюминатных растворов.
- •Физико-химические свойства пыли печей спекания и способы её утилизации.
- •Общая характеристика основных способов производства глинозема из алюминиевых руд: щелочных, кислотных, электротермических. Применимость их к переработке различного сырья.
- •Назначение операции подготовки шихты спекания глиноземсодержащего сырья. Способы корректировки шихты.
- •Характеристика аппаратурно-технологических схем для выщелачивания спеков, их преимущества и недостатки.
- •Порядок выполнения проекта. Части проекта.
- •Требования к шихте для спекания глиноземсодержащего сырья. Интенсификация процесса измельчения шихты.
- •Аппаратурно-технологическая схема отделения агитационного выщелачивания нефелиновых спеков.
- •Переработка нефелиновых руд по способу спекания с добавками бокситов, глин, дистен-силлиманитовых концентратов.
- •Химизм выщелачивания глиноземсодержащего спека.
- •Аппаратурно-технологическая схема отделения подготовки глиноземсодержащей шихты для спекания.
- •Производства цемента из нефелиновых шламов. Общая характеристика способа.
- •2. Превалирующая роль энергетической составляющей в структуре себестоимости глинозема, получаемого по способу спекания, и пути её снижения.
- •Аратурно-технологическая схема отделения проточного выщелачивания нефелинового спека.
- •Роль и значение расчета материального баланса.
- •Аппаратурно-технологическая схема отделения обескремнивания алюминатных растворов. Смотри ответ в билет 4 вопрос 3
- •Расчет материального баланса процесса спекания глиноземсодержащего сырья. Балансирующие величины.
Технологический режим и аппаратура для обескремнивания алюминатных растворов.
Физико-химические основы процесса карбонизации алюминатных растворов.
Карбонизация алюминатных растворов осуществляется барботированием через раствор смеси газов, содержащих CO2. Сущность процесса состоит в нейтрализации едкой щелочи с образованием соды:
2NaOH + CO2 = Na2CO3 + H2O
При взаимодействии алюминатного раствора с углекислым газом, содержание каустической щелочи уменьшается, что ведет к снижению стойкости алюминатного раствора и выделению гидроксида алюминия в осадок:
NaAl(OH)4 + CO2 = Al(OH)3+ NaHCO3
При глубокой карбонизации, проводимой на второй стадии (в присутствии карбонатной и бикарбонатной щелочей), происходит разложение оставшегося алюмината натрия с образованием гидроалюмокарбоната натрия (Na2OAl2O32CO24H2O):
2Na(Al(OH)4) + 2 NaHCO3 --------- Na2OAl2O32CO24H2O + 2NaOH
образование бикарбоната Na2CO3+CO2+ H2O = 2NaHCO3
Если сравнить скорости процессов карбонизации и декомпозиции, то в первом случае разложение идет в несколько раз быстрее. Как и при декомпозиции, лимитирующей является стадия, определяемая внешнедиффузионным подводом вещества к поверхности кристаллизации
или в объем раствора, где наблюдается образование ассоциатов и поликонденсация с выделением Al(OH)3.
Температура, при которой происходит карбонизация составляет 70-90 °С и меняется в незначительных пределах. Естественного охлаждения раствора не происходит вследствие протекания экзотермических реакций и тепла печных газов. Регулировать скорость карбонизации можно путем изменения количества подаваемого газа на единицу объема. В промышленных условиях продолжительность карбонизации составляет 6-8 ч.
Роль интенсифицирующих добавок в повышении эффективности процесса спекания (фтористые соли, уголь, и др.).
|
|
|
|

12
Обоснование двухстадийного обескремнивания алюминатных растворов.
Двустадийность и режимы процесса обусловлены необходимостью получения требуемого кремневого модуля раствора при минимальных затратах реагента-извести.
Обескремнивать растворы в одну стадию только с помощью извести нецелесообразно из-за повышенного расхода извести и глинозема в виде гидрограната.
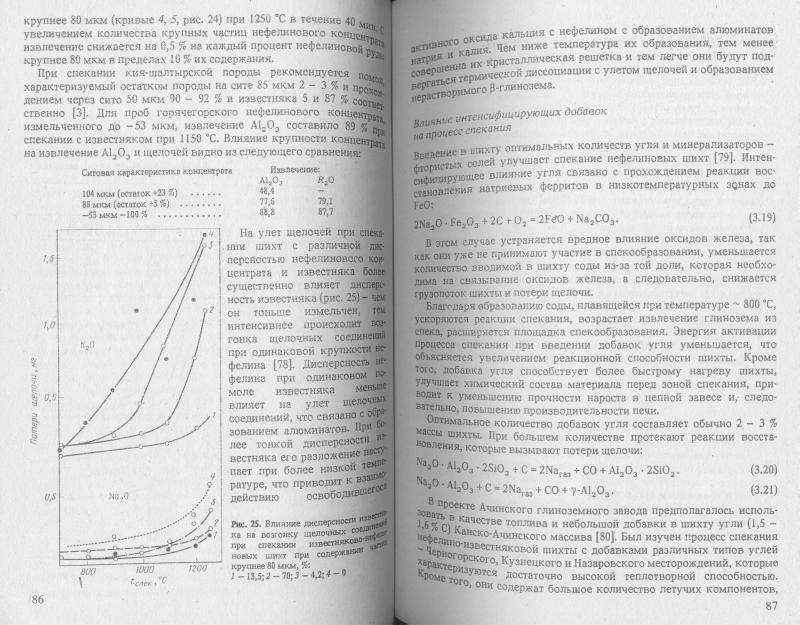
Химизм процесса спекания бокситовых и нефелиновых шихт.

Нефелиновую шихту спекают при 1250—1300° С. Для обеспечения полноты образования алюмината и феррита натрия и двухкальциевого силиката через твердофазные реакции необходим очень тонкий помол исходных сырьевых материалов. Скорость взаимодействия между двумя порошками лимитируется диффузионным переносом и может быть выражена в общем виде уравнением
где у — толщина реакционного слоя при нагревании в течение времени т; D — коэффициент диффузии; х—процент превращения; К—константа скорости реакции (диффузии).
Нагреваясь до 1000—1100° С, исходные смеси для спекания превращаются в основном в смесь оксидов CaO, Al2O3, SiO2, Fe2O3 и др. Это означает, что образование желаемых соединений при спекании происходит в результате взаимодействий между Na2СО3 и Al2O3, Fe2O3, между CaO и SiO2, ТiO2 и т. д. Сода (поташ) активно взаимодействует с Аl2О3 и Fe2О3 при температуре выше 1000°С с образованием алюминатов и ферритов натрия (калия) и твердых растворов алюмоферритов, состав которых зависит от дозировки соды.
При молярном соотношении Na2O:(Аl2О3 + Fe2О3) = 1,0 образуются мета-алюминат натрия NaAlO2, метаферрит натрия NaFeO2 и твердый раствор алюмо-феррита Na(Al,Fe)O2(Na2O·Al(Fe)2O3. Если в смеси содержится не более 15— 20% Fe2О3 от массы Аl2О3, то весь оксид железа практически входит в состав алюмо-феррита; избыток соды остается в спеке свободным. При молярном соотношении Na2O:(Аl2О3 + Fe2О3) < 1 наряду с указанными соединениями, образуется твердый раствор алюмоферрита Na2O-ll(Аl,Fе)2O3, называемый β-глиноземом, который при выщелачивании остается практически неразложенным, и с ним будут связаны потери глинозема и щелочи.
Несколько силикатов кальция различной основности образует CaO с SiO2, однако в условиях спекания (низкая температура и непродолжительное время) образуется только ортосиликат 2СаО·SiO2 при любом соотношении CaO:SiO2. В присутствии Na2O двухкальциевый силикат находится в спеках в виде β-модификации, а без Na2O (для бесщелочных шихт) — γ-модификации. Переход при 675°С β→γ сопровождается саморассыпанием продукта в тонкий порошок.
Примеси алюминиевого сырья связываются при спекании либо с Na2O (сульфат и др.), либо с CaO.
Таким образом, для получения в спеке хорошо растворимого алюмината натрия и гидролизуемого в водных растворах феррита натрия, а также очень малорастворимого ортосиликата кальция необходимо при спекании нефелинов соблюдать в шихте следующие молярные соотношения:
R2O:(Аl2O3 + Fe2O3) = 1,00 ± 0,02,
CaO : SiO2 =2,00 ± 0,03,
где R — Na. Такая шихта называется насыщенной, и она обеспечивает максимальное извлечение Аl2О3 и Na2O при выщелачивании спеков. Иногда для маложелезистого сырья (нефелинов) применяют ненасыщенную шихту, т. е. щелочь дозируют только на соединение с Аl2О3.
Ионы в кристалле, расположенные в непосредственном соседстве со «слабыми» местами, более подвижны, чем ионы в частях кристалла, приближающихся по структуре к идеальным, поэтому способны к перемещениям и взаимодействиям при наименьшей энергии активации. При нагревании в кристалле ускоряется самодиффузия запас внутренней энергии уменьшается и постепенно исправляется дефекты в кристалле. При нагревании однородного кристаллического порошка оживленный обмен частицами между различными кристаллами приводит к сцеплению кристаллов, а затем к поглощению мелких кристалликов к более крупными. Так как температура плавления вещества определяется степенью прочности связи элементарных частиц в кристалле, существует зависимость между температурами спекания и любого вещества. Чем выше температура плавления вещества, тем больший нагрев нужен для спекания его порошка. Температура спекания повышается с усложнением строения кристаллической решётки вещества.
У силикатов и органических соединений более сложное строение кристаллической решетки и более прочные связи в кристаллах, поэтому спекание их возможно лишь при температурах, близких к точкам плавления.
Сначала в твердофазной реакции могут принимать участие только атомы, расположенные на поверхности соприкасающихся веществ; для продолжения реакции нужна взаимная диффузия атомов (ионов) через образовавшийся слой продукта реакции. Полиморфные превращения сопровождаются более или менее существенным перемещением частиц в кристалле, поэтому твердые вещества при температурах полиморфных превращений лучше спекаются и скорее взаимодействуют с кристаллами других веществ. Если же точки полиморфного превращения веществ лежат выше температуры начала спекания, то такие вещества не влияют на спекание и на взаимодействие их с другими веществами.
Твердофазным реакциям способствует тонкое измельчение исходных веществ, поскольку от этого возрастает их удельная поверхность, а с ней - поверхностная энергия и чисто точек соприкосновения разнородных веществ. Вот почему для спекания на заводах всегда тонко измельчают все составные части шихты.
Уплотнение смеси твердых реагентов, как и измельчение зерен, ускоряет реакцию, особенно если смесь перед спрессовыванием смочить какой-либо жидкостью, в том числе и летучей. Жидкость в данном случае действует как смазка и способствует лучшему уплотнению и соприкосновению зерен. По тем же причинам для твердофазных реакций важно не только предварительное тщательное перемешивание исходных веществ, но и во время реакции, в особенности если оно сопровождается растиранием продуктов реакции. При перемешивани
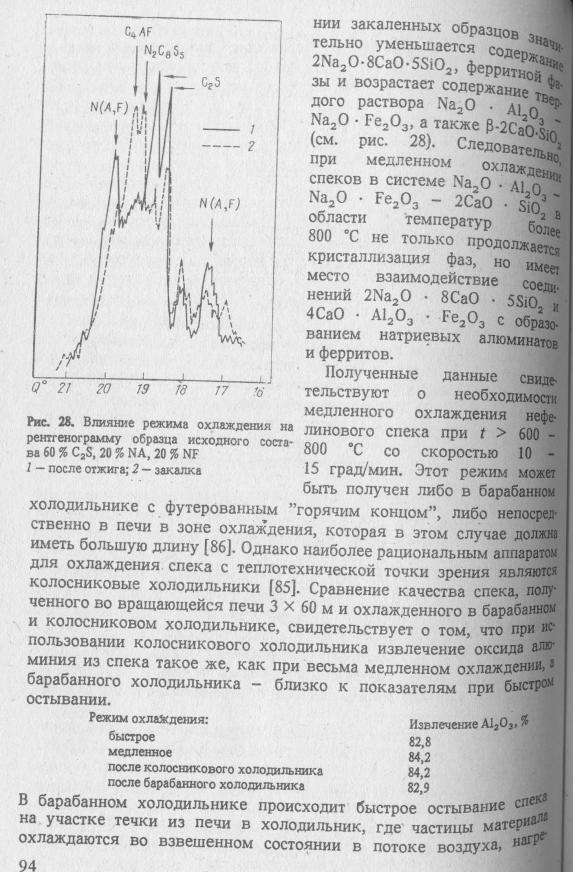
Влияние технологического режима спекания на физико-химические свойства спеков.
продуктов реакции. При перемешивани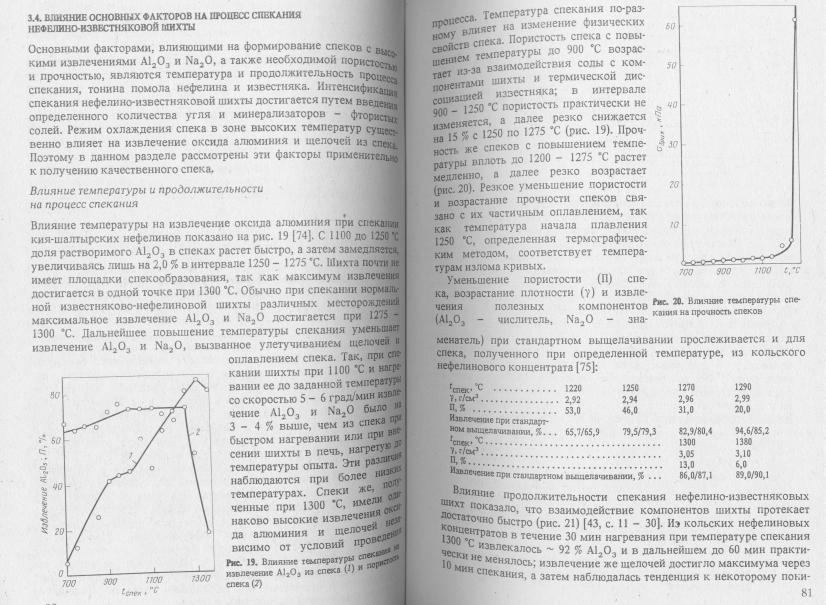



 1
1
 3
3
 .
.

13 |
|
|
|
Регенерация глинозема из известкового шлама после второй стадии обескремнивания алюминатных растворов.
Механизм спекания глиноземсодержащих шихт.
См. в билете 3 вопрос 3.
Аппаратура для карбонизации алюминатных растворов.
Основным типом применяемых в настоящее время карбонизаторов является цилиндроконический аппарат с аэролифтным перемешиванием.
Карбонизатор представляет собой бак цилиндрической формы с конусным днищем. Для подвода и равномерного распределения печных газов предусматриваются две кольцевые камеры с барботерами колпачкового типа, погруженные под небольшим слоем раствора. По другому варианту газ подается и распределяется через одну кольцевую камеру с барботирующим устройством, состоящим из трех провальных колосниковых решеток, расположенных на расстоянии 200 мм друг от друга. Карбонизатор снабжен аэролифтом для воздушного перемешивания, паровой трубой для нагрева раствора и воздушной – для взмучивания осадка в нижней части бака. Карбонизаторы могут работать периодически и не прерывно. В последнем случае необходимо предусмотреть в каждом карбонизаторе дополнительные аэролифты для перекачивания пульпы или сливные пороги с течками для передачи пульпы из одного бака в другой, а из последнего - в сборный бак или сгуститель.
|
|
|
14 |




