
- •1Основные понятия коллоидной химии; классификация, основные особенности, количественные характеристики дисперсных систем.
- •2. Диспергационные методы получения дисперсных систем
- •3. Конденсационные методы получения дисперсных систем
- •5Первый и второй законы Фика, диффузия, движущая сила диффузии, связь коэффициента диффузии с размерами частиц.
- •6. Гипсометрический закон Лапласа, диффузионно-седиментационное равновесие. Кривая седиментации для монодисперсных и полидисперсных систем.
- •7. Строение двойного электрического слоя (фи-потенциал и дзета-потенциал), теория Квинке-Гельмгольца-Перрена, теория Гуи-Чепмена, теория Штерна, строение мицеллы.
- •9 Закон Бугера-Ламберта-Бера, оптические свойства коллоидных растворов, оптические методы анализа дисперсности.
- •10. Работа когезии. Связь поверхностной энергии с взаимодействиями между молекулами (атомами, ионами), правило Трутона, уравнение Дюпре. .
- •12. Закон Лапласа: общая форма, частные случаи, капиллярное поднятие жидкости, уравнение Жюрена.
- •13 Закон Томсона (Кельвина), зависимость давления насыщенного пара от кривизны поверхности жидкости, капиллярная конденсация.
- •14. Закон Гиббса-Оствальда-Фрейндлиха, влияние дисперсности на растворимость твердых частиц, процессы изотермической перегонки в дисперсных системах.
- •15. Лиофильные коллоидные системы, методы получения. Самопроизвольное диспергирование макрофаз: критерий самопроизвольного диспергирования (по Ребиндеру-Щукину, примеры).
- •17 Солюбилизация
- •18. Термодинамика мицеллообразования, диаграмма фазовых состояний, точка Крафта, жидкокристаллические системы.
- •19. Образование и строение обратных мицелл
- •Классификация
- •Свойства
- •21 Термопреципитация
- •22. Фотофорез
- •23. Термофорез.
- •25 Быстрая и медленная коагуляция.
- •26. Концентрационная и нейтрализационная коагуляция
- •27. Изотермическая перегонка.
- •29 Эффект Марангони
- •30. Тиксотропия.
- •31. Флотация.
- •33. Правило Банкрофта
- •34. Правило Дюкло-Траубе
- •35. Правило Шульца-Гарди.
- •37. Теория длфо.
- •38. Слои Шиллера
- •39. Тактоиды
- •41. Кольца и слои Лизеганга
- •42. Пептизация.
- •43. Флокуляция
- •45. Адагуляция.
- •46. Аддитивность коагуляции.
- •47. Антагонизм коагуляции
- •49. Коагуляционные структуры
- •50. Структуры с фазовыми контактами
- •51. Синерезис.
- •53. Кристаллизационные структуры
- •54. Когезия.
- •55. Адгезия
- •57. Смачивание.
- •58. Капиллярное давление
- •59. Закон Ньютона (трение)
- •61. Застудневание
- •62.Ползучесть
- •63. Вязкость коллоидных растворов. Зависимость вязкости раствора от концентрации взвешенных частиц (уравнение Эйнштейна)
- •Аномалии вязкости
- •65. Как образуется снежинка
- •66. Хемосорбция и каталитическая сорбция, сходства и отличия, привести примеры
- •67. Почему “химические дожди” выпадают недалеко от источника загрязнения?
- •69. Абсорция.
- •70. Хемосорбция.
- •71. Каталитическая сорбция
- •73. В чём сходство и различие газовой и жидкой дисперсионных сред?
- •74. Почему туман в вечернее время распространяется в приземном слое, не оседая на поверхность?
- •75. Почему снег выпадает иногда в виде “крупы”?
- •77. Адсорбция и адагуляция, сходства и отличия, привести примеры
- •Количественные характеристики дисперсных систем
- •Классификация дисперсных систем по размеру частиц дисперсной фазы
- •Классификация дисперсных систем по фракционному составу частиц дисперсной фазы
- •Классификация дисперсных систем по концентрации частиц
- •Классификация дисперсных систем по взаимодействию дисперсной фазы с дисперсной средой
- •Классификация дисперсных систем по характеру распределения фаз
- •Классификация дисперсных систем по агрегатному состоянию
- •Классификация дисперсных частиц по размерам
- •Классификация дисперсных частиц по форме
- •Классификация дисперсных частиц по строению
- •Классификация дисперсных частиц по химическому составу
- •Размерные эффекты, наблюдаемые в дисперсных системах
- •Тд свойства дисперсных частиц
- •Механические свойства дисперсных частиц
- •Магнитные свойства дисперсных частиц
- •Каталитические свойства дисперсных частиц
- •Энергетическое и силовое определение поверхностного натяжения
- •Факторы, влияющие на поверхностное натяжение
- •Дисперсная и полярная составляющие поверхностного натяжения
- •Метод избыточных величин Гиббса
- •Капиллярное давление
- •Закон Лапласа
- •Смачивание
- •Закон Юнга
- •Несмачивание, полное смачивание, гидрофильность, гидрофобность.
- •Правило Антонова
- •Эффект Марангони
- •Зависимость смачивания от свойств твёрдой поверхности
- •Смачивание нанокаплями
- •Адгезия, когезия, уравнение Дюпре
- •Закон Кельвина
- •Закон Гиббса-Оствальда
- •Изотермическая перегонка
- •Капиллярная конденсация
- •Закон Жюрена
- •Закон Пуазейля
- •Измерение поверхностного натяжения методом капиллярного подъёма
- •Измерение поверхностного натяжения методом сидящей капли
- •Измерение поверхностного натяжения методом максимального давления
- •Измерение поверхностного натяжения методом пластинки Вильгельми
- •Измерение поверхностного натяжения методом вращающейся капли
- •Измерение поверхностной энергии твёрдых тел
- •Адсорбция пав из растворов на поверхности твёрдых тел
- •Химическое модифицирование твёрдых тел
- •Классификация пав по растворимости
- •Классификация пав по диссоциации в воде
- •Классификация пав по способу образования мицелл и происхождению
- •Классификация пав по фх воздействию на поверхность раздела между фазами
- •Гидрофильно-липофильный баланс
- •Критический параметр упаковки
- •Механизмы образования электрического заряда на поверхности твёрдых тел и жидкостей в дисперсных системах
- •Строение дэс
- •Влияние электролитов на дэс
- •Электрофорез
- •Электроосмос
- •Потенциал течения
- •Потенциал оседания
- •Электрокапиллярные явления (электрокапиллярная кривая, закон Липпмана)
12. Закон Лапласа: общая форма, частные случаи, капиллярное поднятие жидкости, уравнение Жюрена.
Вследствие избыточной пов-й энергии подвешенная жидкость в условии невесомости приобретает сферическую форму. С уменьшением кол-ва жидкости роль силы тяжести снижается, т.к. она уменьшается пропорц-но кубу, а пов-ть квадрату радиуса тела, т.е. увеличивается удельная пов-ть . С появлением кривизны пов-ти тела радиусом r возникает дополнительное внутреннее давление дельта Р .Его можно представить как равнодейств. силу пов-го натяжения ,сходящихся в одной точке. Равнодейсв. направлена перпендикулярно пов-ти в центр кривизны.
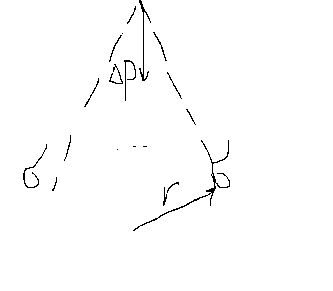
Эта сила рассчитана на ед площади и представляет собой доп-е давление:
 Где
Δ Р - разность давлений внутри тела
с изогнутой и плоской пов-ти.
Где
Δ Р - разность давлений внутри тела
с изогнутой и плоской пов-ти.
 -
кривизна поверхности. Чем больше σ, тем
влияние кривизны значительное для
сферической формы.
-
кривизна поверхности. Чем больше σ, тем
влияние кривизны значительное для
сферической формы.
Для
цилиндрической пов-ти длиной L
и радиусом r
имеем:
 Тогда:
Тогда:

для
пов-ти неправильной формы используется
представление средней кривизны, опред.
по уравнению: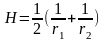 Где
1/r1
и 1/r2
-кривизна главных нормальных сечений
1 и 2.
Где
1/r1
и 1/r2
-кривизна главных нормальных сечений
1 и 2.
Тогда: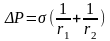 - это и есть уравнение Лапласа.
- это и есть уравнение Лапласа.
Капиллярное явление наблюдается в сосудах, содержащих жидкость у которых расстояние между стенками соизмеримо с радиусом кривизны пов-ти жидкости. Поведение ж-ти в капиллярных сосудах зависит от того, смачивает или нет жидкость стенки сосуда. При смачивании наблюдается поднятие уровня в капилляре за счет растяжения ж-ти, а при не смачивании наоборот- опускание в рез-те сжатия. При равновесии Лапласовское давление = гидростатическому
 Где
ρ - плотность жидкости, ρ0
-
плотность газовой фазы, g-
ускорение свободного падения, r-радиус
мениска, h
- высота столба
Где
ρ - плотность жидкости, ρ0
-
плотность газовой фазы, g-
ускорение свободного падения, r-радиус
мениска, h
- высота столба
 -
Уравнение
Жюрена.
-
Уравнение
Жюрена.
Где
 .
.
Следует помнить, что капиллярное явление имеет место только на границе трех фаз: твердое тело – газ – жидкость.
13 Закон Томсона (Кельвина), зависимость давления насыщенного пара от кривизны поверхности жидкости, капиллярная конденсация.
Закон Кельвина (Томпсона) определяет зависимость давления насыщенного пара от кривизны жидкости.
pr≈ p0*[1+2σVm/(rRT)]
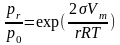 или
приближённо
или
приближённо ,
т.е.
,
т.е.
 .
Необходимо отметить, что для вогнутой
поверхности давление насыщенного пара
будет меньше, чем над плоской поверхностью,
поэтому закон Кельвина примет вид:
p0/pr=exp[2σVm/(rRT)].
.
Необходимо отметить, что для вогнутой
поверхности давление насыщенного пара
будет меньше, чем над плоской поверхностью,
поэтому закон Кельвина примет вид:
p0/pr=exp[2σVm/(rRT)].
pr (*индекс –r) – равновесное давление насыщенного пара, p0 – давление насыщенного пара, σ – поверхностное натяжение капли, r – радиус капли, R – газовая постоянная, Vm – молярный объем жидкости, Т – температура. Из закона Томсона видно, что равновесное давление пара для капель жидкости тем выше, чем меньше радиус капель. Закон Томсона в приближённом виде применим практически во всех случаях, за исключением капель размерами, приближающимися к молекулярным.
Явление капиллярной конденсации состоит в том, что конденсация пара в тонких капиллярных порах твёрдых адсорбентов происходят при давлении меньших, чем давление насыщенного пара над плоской поверхностью жидкости (при условии смачивания конденсатом поверхности адсорбента). В соответствии с законом Томсона (Кельвина) чем меньше поры адсорбента, тем при меньшем давлении происходит конденсация.
Примеры: Капиллярная конденсация увеличивает поглощение (сорбцию) паров пористыми телами, в особенности вблизи точки насыщения паров. Капиллярная конденсация используется в промышленности для улавливания жидкостей тонкопористыми телами (сорбентами): при рекуперации (возвращение в производство) летучих растворителей в технологических процессах; для анализа геометрии порогового пространства сорбента и др. Большую роль капиллярная конденсация играет также в процессах сушки, удержания влаги почвами, строительными и др. пористыми материалами.
Отрицательное капиллярное давление может удерживать вместе смачиваемые жидкостью частицы, обеспечивая прочность таких структур. В случае несвязных пористых тел возможна их объемная деформация под действием капиллярных сил- так называемая капиллярная контракция. Капиллярная конденсация может быть причиной прилипания частиц пыли к твердым поверхностям, разрушения пористых тел при замораживании сконденсированной жидкости в порах. Для уменьшения эффекта капиллярной конденсации используют лиофобизацию поверхности пористых тел.
