
- •Неорганическая химия
- •1. Важнейшие классы неорганических соединений: оксиды, гидроксиды, кислоты, соли.
- •2. Закон сохранения материи.
- •3. Основные типы комплексных соединений (к.С.). Поведение к.С. В водных растворах. Константа нестойкости.
- •4. Номенклатура комплексных соединений. Координационное число.
- •5. Амфотерные гидроксиды
- •6. Комплексные соединения. Комплексообразователь, лиганды.
- •7. Гидролиз солей, образованных слабым основанием и сильным кислотой. Степень и константа гидролиза.
- •8. Растворение твердых веществ. Из каких слагаемых состоит теплота растворения твердого вещества в жидкости?
- •9. Типы окислительно-восстановительных реакций.
- •10. Закон постоянства состава. Дальтониды, бертоллиды.
- •11. Кристаллизация разбавленных и концентрированных растворов. Кристаллогидраты.
- •12. Ионообменные реакции. Произведение растворимости.
- •13. Закон кратных отношений.
- •14. Электрохимическая диссоциация воды. Ионное произведение воды. Водородный показатель.
- •15. Отношение металлов к соляной и серной кислотам (разбавленной и концентрированной).
- •17. Закон эквивалентов. Определение эквивалентов простых и сложных веществ.
- •18. Способы выражения концентрации раствора: молярная, нормальная, титр.
- •19. Квантово-механическая теория строения атома. Уравнение Луи де Бройля. Принцип неопределенности Гейзенберга.
- •20. Окислительно-восстановительные свойства перманганата калия.
- •22. Гидролиз солей, образованных слабым основанием и слабой кислотой.
- •23. Слабые электролиты. Степень диссоциации. Константа диссоциации.
- •24. Отношение металлов к азотной кислоте.
- •26. Электронная структура атомов. S-, p-, d-, f- электронные семейства атомов.
- •27. Растворимость. Растворение газов, жидкостей и твердых тел. Физико-химическая теория растворов.
- •28. Заполнение атомных орбиталей в атомах с возрастанием порядкового номера элемента (правило Клечковского).
- •29. Давление пара над жидкостью. Первый закон Рауля.
- •30. Ядерная модель строения атома. Атомные ядра, их состав. Изотопы, изобары.
- •31. Растворы сильных электролитов.
- •32. Квантовые числа: главное, орбитальное, магнитное, спиновое.
- •33. Общее понятие о растворах. Способы выражения концентрации раствора: моляльность, массовая доя, титр.
- •34. Гидролиз солей, образованных сильным основанием и слабой кислотой.
- •35. Осмос. Осмотическое давление.
- •36. Сильные электролиты.
- •37. Квантовая теория света Планка. Теория строения атома Бора.
- •38. Вода. Физические и химические свойства воды.
- •39. Закон эквивалентов. Химический эквивалент. Определение эквивалента кислоты, основания и соли.
- •40. Второй закон Рауля.
13. Закон кратных отношений.
Закон кратных отношений: «Если два элемента образуют друг с другом несколько химических соединений, то массы одного из элементов, приходящиеся в этих соединениях на одну и ту же массу другого, относятся между собой как небольшие целые числа».
14. Электрохимическая диссоциация воды. Ионное произведение воды. Водородный показатель.
Изучение очищенной от примесей воды показало, что она обладает электропроводностью, повышающейся с ростом температуры. Это можно объяснить небольшой самодиссоциацией воды на ионы водорода и гидроксид-ионы:
![]()
По величине электрической проводимости чистой воды можно вычислить концентрацию ионов гидроксония Н3О+ и гидроксид-ионов в воде. При 25ºС она равна 10‾7 моль/л.
Константа диссоциации воды может быть вычислена по уравнению
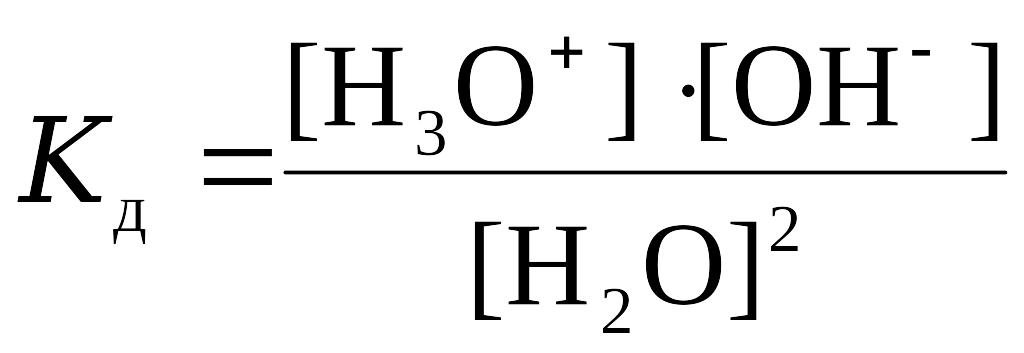 ,
,
Перепишем это уравнение следующим образом:
![]()
Поскольку степень диссоциации воды очень мала, то концентрация недиссоциированных молекул Н2О в воде равна общей концентрации воды, т.е. 55,55 моль/л (1 л содержит 1000 г воды, т.е. 1000/18 = 55,55 моль).
Полученное уравнение показывает, что для воды и разбавленных водных растворов при неизменной температуре произведение концентраций ионов гидроксония и гидроксид-ионов есть величина постоянная. Она называется ионным произведением воды.
В соответствии теорией электролитической диссоциации ионы Н+ являются носителями кислотных свойств, а ионы ОНˉ - носителями основных свойств. Поэтому раствор будет нейтральным, когда
![]() ;
;
кислым, когда
![]() ;
;
и щелочным, когда
![]()
Для характеристики кислотности (щелочности) среды введен специальный параметр – водородный показатель, или pH. Водородным показателем, или pH, называется взятый с обратным знаком десятичный логарифм концентрации водородных ионов в растворе:
![]()
Из ионного произведения следует:
![]()
![]()
![]()
рН + рОН = 14.
Таким образом, зная рОН, можно легко рассчитать рН, и наоборот, по известному значению рН легко определяется рОН.
15. Отношение металлов к соляной и серной кислотам (разбавленной и концентрированной).
Соляная кислота – это техническое название хлороводородной кислоты. Получают ее путем растворения в воде газообразного хлороводорода – HCl. Ввиду невысокой его растворимости в воде, концентрация соляной кислоты при обычных условиях не превышает 38%. Поэтому независимо от концентрации соляной кислоты процесс диссоциации ее молекул в водном растворе протекает активно:
HCl
![]() H+
+ Cl-
H+
+ Cl-
Образующиеся в этом процессе ионы водорода H+ выполняют роль окислителя, окисляя металлы, расположенные в ряду активности левее водорода. Взаимодействие протекает по схеме:
Me
+ HCl
![]() соль
+ H2↑
соль
+ H2↑
Соляная кислота является слабым окислителем, поэтому металлы с переменной валентностью окисляются ей до низших положительных степеней окисления:
Fe0 → Fe2+
Co0 → Co2+
Ni0 → Ni2+
Cr0 → Cr2+
Mn0 → Mn2+ и др.
Соляная кислота пассивирует свинец (Pb). Пассивация свинца обусловлена образованием на его поверхности трудно растворимого в воде хлорида свинца (II), который защищает металл от дальнейшего воздействия кислоты:
Pb + 2 HCl → PbCl2↓ + H2↑
Серная кислота (H2SO4)
В промышленности получают серную кислоту очень высокой концентрации (до 98).
Разбавленная серная кислота
В разбавленном водном растворе серной кислоты большинство ее молекул диссоциируют:
H2SO4 H+ + HSO4-
HSO4- H+ + SO42-
Образующиеся ионы Н+ выполняют функцию окислителя. Как и соляная кислота, разбавленный раствор серной кислоты взаимодействует только с металлами активными и средней активности (расположенными в ряду активности до водорода).
Химическая реакция протекает по схеме:
Ме + H2SO4(разб.) → соль + H2↑
Металлы с переменной валентностью окисляются разбавленным раствором серной кислоты до низших положительных степеней окисления:
Fe0 → Fe2+
Co0 → Co2+
Ni0 → Ni2+
Cr0 → Cr2+
Mn0 → Mn2+ и др.
Свинец (Pb) не растворяется в серной кислоте (если ее концентрация ниже 80%), так как образующаяся соль PbSO4 нерастворима и создает на поверхности металла защитную пленку.
Концентрированная серная кислота
В концентрированном растворе серной кислоты (выше 68%) большинство молекул находятся в недиссоциированном состоянии, поэтому функцию окислителя выполняет сера, находящаяся в высшей степени окисления (S+6). Концентрированная H2SO4 окисляет все металлы, стандартный электродный потенциал которых меньше потенциала окислителя – сульфат-иона SO42-. В связи с этим, с концентрированной серной кислотой реагируют и некоторые малоактивные металлы.
Процесс взаимодействия металлов с концентрированной серной кислотой в большинстве случаев протекает по схеме:
Me + H2SO4 (конц.) соль + вода + продукт восстановления H2SO4
Практика показала, что при взаимодействии металла с концентрированной серной кислотой выделяется смесь продуктов восстановления, состоящая из H2S, S и SO2. Взаимодействие металлов различной активности с концентрированной серной кислотой можно представить схемой:

Алюминий (Al) и железо (Fe) не реагируют с холодной концентрированной H2SO4, покрываясь плотными оксидными пленками, однако при нагревании реакция протекает.
Ag, Au, Ru, Os, Rh, Ir, Pt не реагируют с серной кислотой.
Концентрированная серная кислота является сильным окислителем, поэтому при взаимодействии с ней металлов, обладающих переменной валентностью, последние окисляются до более высоких степеней окисления, чем в случае с разбавленным раствором кислоты:
Fe0 → Fe3+,
Cr0 → Cr3+,
Mn0 → Mn4+,
Sn0 → Sn4+
Свинец (Pb) окисляется до двухвалентного состояния с образованием растворимого гидросульфата свинца Pb(HSO4)2.
16. Факторы, влияющие на окислительно-восстановительные процессы. Расстановка коэффициентов в окислительно-восстановительных реакциях.
Природа, концентрация, температура, катализаторы
Метод электронного баланса, основанный на учете изменения степеней окисления и принципе электронейтральности молекулы, является универсальным. Его обычно используют для составления уравнений окислительно-восстановительных реакций, протекающих между газами, твердыми веществами и в расплавах.
Последовательность операций, согласно этому методу, такая:
1) Записывают формулы реагентов и продуктов реакции в молекулярном виде:
![]()
2) Определяют степени окисления атомов, меняющих ее в процессе реакции:
![]()
3) По изменению степеней окисления устанавливают число электронов, отдаваемых восстановителем, и число электронов, принимаемых окислителем, и составляют электронный баланс с учетом принципа равенства числа отдаваемых и принимаемых электронов:
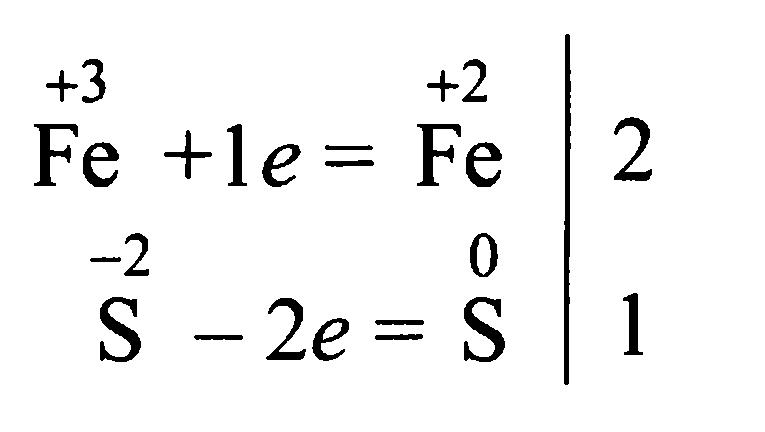
4) Множители электронного баланса записывают в уравнение окислительно-восстановительной реакции как основные стехиометрические коэффициенты:
![]()
5) подбирают стехиометрические коэффициенты остальных участников реакции:
![]()
При составлении уравнений следует учитывать, что окислитель (или восстановитель) может расходоваться не только в основной окислительно-восстановительной реакции, но и при связывании образующихся продуктов реакции, т.е. выступать в роли среды и солеобразователя.
