
- •Лекция №1
- •Предмет органической химии
- •Эмпирические, молекулярные и структурные формулы. Изомерия.
- •Классификация органических веществ.
- •Важнейшие функциональные производные органических веществ
- •Номенклатура органических веществ
- •Лекция № 2
- •Виды химических связей
- •Ковалентная связь
- •Образование молекулярных орбиталей из ао (лкао мо)
- •Электронная конфигурация и гибридизация углерода в органических соединениях
- •Полярность и поляризуемость связей
- •Лекция № 3
- •Классификация органических реакций: по характеру превращения
- •По типу разрыва связи в исходной молекуле
- •Энергетические аспекты химических реакций
- •Механизмы органических реакций
- •Постулат Дж. Хэммонда
- •Лекция № 4
- •Равновесные реакции
- •Кинетический и термодинамический контроль
- •Кислотно-основные свойства органических соединений
- •Кислоты и основания по Брёнстеду-Лоури
- •Кислоты и основания по Льюису
- •Лекция № 5 Углеводороды Алканы
- •Алканы (насыщенные ациклические соединения, парафины)
- •Изомерия, номенклатура
- •Конформационная изомерия
- •Номенклатура
- •Лекция № 6 Углеводороды
- •Химические свойства алканов
- •Механизм реакции галогенирования алканов
- •Лекция № 7 Углеводороды
- •Природные источники и методы получения алканов
- •Получение алканов. Лабораторные и промышленные методы синтеза
- •Лекция № 8 Углеводороды
- •Алкены (олефины, этиленовые углеводороды)
- •Получение алкенов
- •Дегидрогалогенирование алкилгалогенидов
- •Дегидратация спиртов
- •Дегалогенирование дигалогенопроизводных
- •Парциальное (частичное) гидрирование алкинов
- •Лекция № 9 Углеводороды
- •Химические свойства алкенов
- •Присоединение галогенов
- •Присоединение галогеноводородов
- •Лекция № 10 Углеводороды
- •Радикальное присоединение к алкенам
- •Гидратация алкенов
- •Образование галогенгидринов
- •Окисление алкенов
- •Образование эпоксидов
- •Окислительное расщепление двойной связи
- •Озонолиз (реакция Гарриеса)
- •Гидроксилирование алкенов (реакция Вагнера)
- •Лекция № 11 Углеводороды
- •Реакции замещения в алкильных группах алкенов
- •Полимеризация алкенов
Лекция № 4
Равновесные реакции, константа равновесия, кинетический и термодинамический контроль. Механизм реакции и пути его установления. Принцип микроскопической обратимости, постулат Хэммонда.
Кислоты и основания в органической химии (теории Бренстеда-Лоури и Льюиса). Сопряженные кислоты и основания. Кислотно-основные равновесия. Константа кислотности (рКа), константа основности (рКb). Влияние заместителей на кислотность и основность органических соединений.
Равновесные реакции
Особенность многих органических реакций состоит в том, что они равновесные.
aA + bB = dD + fF
Скорость прямой реакции: Vпр = KпрCAaCBb
Скорость обратной реакции: Vоб = KобCDdCFf
Когда скорости прямой и обратной реакции равны, наступает равновесие:
Vпр = Vоб
KпрCAaCBb = KобCDdCFf
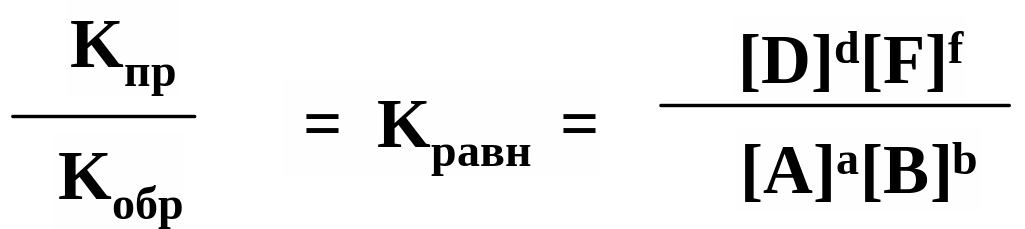
Кроме того, константу равновесия можно выразить через свободную энергию:
G = -RTlnKравн
Важно: при наступлении состояния равновесия реакции не прекращаются. Одновременно протекают прямая и обратная реакция, но из-за постоянства концентраций исходных веществ и продуктов, кажется, что все процессы остановились. Просто скорости прямой и обратной реакции равны!
Если Vпр > Vобр, то в равновесном состоянии концентрации продуктов будут выше концентраций исходных веществ. Равновесие сдвинуто вправо. При Vпр < Vобр равновесие смещено влево, в сторону исходных веществ. Если в первом случае не удается выделить исходные соединения, считают, что реакция полностью прошла. Во втором случае, если не удается обнаружить продукты, реакция не идет.
Кинетический и термодинамический контроль
В ряде случаев в результате протекания параллельных реакций в реакционной массе могут образовываться два продукта (C и D), один из которых превращается в другой либо непосредственно (по реакции 3) (рис 4.1а), либо в результате обратимости первой реакции (рис. 4.1б). Какой из продуктов является основным, очень часто зависит от температурных условий проведения превращения.
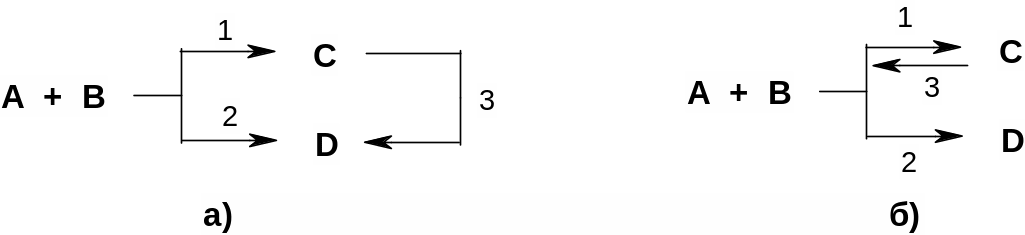
Рис. 4.1. Схемы конкурентных реакций
Энергетическая диаграмма процессов, изображенных на рис. 4.1а, показывает, что образование продукта С происходит быстрее, т.к. ЕаС этой реакции заметно меньше, чем ЕаD (рис. 4.2). При низкой температуре, когда энергия реагирующих молекул невелика, основное направление реакции – образование соединения С. Этот процесс контролируется скоростью и называется кинетически контролируемой реакцией, а соединение С – продуктом кинетического контроля.
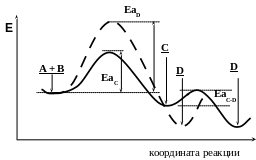
Рис. 4.2. Кинетический и термодинамический контроль
(последовательное превращение)
Образование соединения D требует большей энергии, поэтому при низкой температуре оно – побочный продукт. Однако продукт D термодинамически более устойчив, чем С. Поэтому с ростом температуры проведения реакции, когда большее число молекул способно перебраться через высокий энергетический барьер, в реакционной массе наблюдается преобладание продукта D. Процесс образования соединения D контролируется энергетическими факторами и называется термодинамически контролируемой реакцией. Соединение D – продукт термодинамического контроля.
Соединение С образуется быстро. Его стабильность относительно низка, а энергия активации превращения С в D (ЕаС-D) невелика. При проведении реакции при повышенной температуре (т.е. в условиях термодинамического контроля) происходит превращение соединения С в более энергетически выгодный продукт Д.
На рис. 4.3 показаны энергетические профили реакций кинетического (образование С) и термодинамического (образование D) контроля для обратимых превращений.. Причины особенностей протекания реакций аналогичны изложенным выше.
Е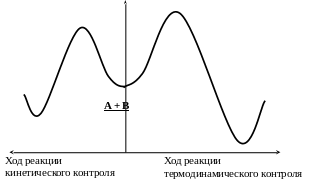


C
EaD
EaD
D


Рис. 4.3. Кинетический и термодинамический контроль (обратимое превращение)
Отличается только превращение продукта кинетического контроля С в продукт термодинамического контроля D. При повышенной температуре происходит превращение соединения С в исходные вещества A и B. Процесс протекает быстро, т.к. энергия активации этого процесса незначительна. Превращение D в исходные продукты протекает значительно труднее, и он накапливается в реакционной смеси.
Образование продуктов кинетического и термодинамического контроля – классический случай протекания органических реакций. Конкретные реакции будут рассмотрены в соответствующих разделах (см., например, химические свойства 1,3-алкадиенов, лекция № 15).
