
- •Лекция №1
- •Предмет органической химии
- •Эмпирические, молекулярные и структурные формулы. Изомерия.
- •Классификация органических веществ.
- •Важнейшие функциональные производные органических веществ
- •Номенклатура органических веществ
- •Лекция № 2
- •Виды химических связей
- •Ковалентная связь
- •Образование молекулярных орбиталей из ао (лкао мо)
- •Электронная конфигурация и гибридизация углерода в органических соединениях
- •Полярность и поляризуемость связей
- •Лекция № 3
- •Классификация органических реакций: по характеру превращения
- •По типу разрыва связи в исходной молекуле
- •Энергетические аспекты химических реакций
- •Механизмы органических реакций
- •Постулат Дж. Хэммонда
- •Лекция № 4
- •Равновесные реакции
- •Кинетический и термодинамический контроль
- •Кислотно-основные свойства органических соединений
- •Кислоты и основания по Брёнстеду-Лоури
- •Кислоты и основания по Льюису
- •Лекция № 5 Углеводороды Алканы
- •Алканы (насыщенные ациклические соединения, парафины)
- •Изомерия, номенклатура
- •Конформационная изомерия
- •Номенклатура
- •Лекция № 6 Углеводороды
- •Химические свойства алканов
- •Механизм реакции галогенирования алканов
- •Лекция № 7 Углеводороды
- •Природные источники и методы получения алканов
- •Получение алканов. Лабораторные и промышленные методы синтеза
- •Лекция № 8 Углеводороды
- •Алкены (олефины, этиленовые углеводороды)
- •Получение алкенов
- •Дегидрогалогенирование алкилгалогенидов
- •Дегидратация спиртов
- •Дегалогенирование дигалогенопроизводных
- •Парциальное (частичное) гидрирование алкинов
- •Лекция № 9 Углеводороды
- •Химические свойства алкенов
- •Присоединение галогенов
- •Присоединение галогеноводородов
- •Лекция № 10 Углеводороды
- •Радикальное присоединение к алкенам
- •Гидратация алкенов
- •Образование галогенгидринов
- •Окисление алкенов
- •Образование эпоксидов
- •Окислительное расщепление двойной связи
- •Озонолиз (реакция Гарриеса)
- •Гидроксилирование алкенов (реакция Вагнера)
- •Лекция № 11 Углеводороды
- •Реакции замещения в алкильных группах алкенов
- •Полимеризация алкенов
Лекция № 11 Углеводороды
Алкены. Реакции радикального замещения (аллильное галогенирование). Полимеризация олефинов и ее разновидности (цепная, ступенчатая, катионная, анионная, радикальная). Стереоспецифическая полимеризация. Полиэтилен, полипропилен.
Реакции замещения в алкильных группах алкенов
Наличие алкильных групп в молекулах алкенов предполагает их способность участвовать в реакциях свободнорадикального замещения. Классической реакцией такого типа является галогенирование. Алканы реагируют с галогенами в газовой фазе при высокой температуре или освещении. Алкены присоединяют галогены в темноте, при низкой температуре и в жидкой фазе. Такие различия в условиях проведения реакции могут быть использованы для подбора условий, позволяющих проводить ионное присоединение или свободнорадикальное замещение.
При высокой температуре (> 300oС) пропилен вступает в реакцию с хлором с образованием аллилхлорида.

sp3-Гибридизованный атом углерода, находящийся по соседству с углеродом двойной связи, называется аллильным. Замещение водорода у аллильного атома – аллильное замещение. Эта реакция - общая для всех алкенов. Аллильное бромирование обычно приводят с использованием N-бромсукцинимида.
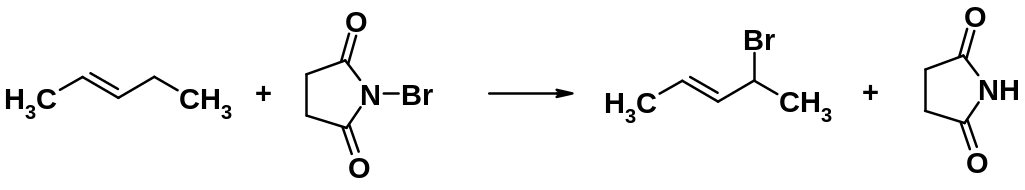
N-Бромсукцинимид создает постоянную низкую концентрацию атомов брома в реакционной смеси, что благоприятствует течению свободнорадикального замещения.
Следует отметить, что аллильный радикал легче образуется и обладает меньшей энергией, чем алкильные радикалы (причины таких свойств будут рассмотрены в других разделах). Как было показано в разделе алканы, свободнорадикальное замещение протекает через образование наиболее стабильного свободного радикала. Это объясняет региоселективность реакции аллильного замещения.
Полимеризация алкенов
Одной из наиболее важных реакций органических соединений, содержащих двойные углерод-углеродные связи, является реакция полимеризации. В настоящее время высокомолекулярные соединения (ВМС, полимеры) проникли во все области человеческой деятельности.
Полимером называют макромолекулу, построенную из большого числа повторяющихся звеньев (фрагментов) низкомолекулярного вещества - мономера. ВМС, состоящее из одинаковых фрагментов, называют гомополимером (чаще просто полимером), построенное из различных фрагментов – гетерополимером (чаще – сополимером).
Полимеризация – процесс получения ВМС, при котором молекулы полимера образуются за счет последовательного присоединения мономера к растущей цепи макромолекулы. Если в процессе участвуют два и более мономера, такую реакцию обычно называют сополимеризацией.
Следует отличать реакции полимеризации от реакций поликонденсации. В полимеризации все атомы мономера входят в молекулу ВМС. В поликонденсации также образуются ВМС, но на каждую образующуюся между молекулами мономера связь выделяется молекула низкомолекулярного вещества (вода, аммиак или галогеноводород).
Простейший пример полимеризации:

В этой реакции мономером является простейший алкен – этилен. Концевые группировки полимерной цепи отличаются от всех остальных, но их количество и влияние на свойства макромолекулы очень мало. Индекс n - степень полимеризации - указывает число мономерных звеньев в молекуле полимера Название полимера образуется добавлением к названию мономера приставки поли-. В приведенном выше примере, мономером является этилен, а продуктом полимеризации – полиэтилен.
Реакции полимеризации подразделяют на два типа – ступенчатую и цепную. Ступенчатая протекает таким образом, что образующиеся на каждой стадии олигомеры могут быть выделены. Как правило, таким способом получают ди-, три- и тетрамеры. Ступенчатая полимеризация значительно меньше распространена, чем цепная.
Цепная полимеризация сразу приводит к образованию высокомолекулярного соединения. В ходе этого процесса невозможно выделение олигомерных продуктов. Этот тип полимеризации очень распространен, в нем выделяют четыре механизма протекания. Механизм цепной полимеризации зависит от того, каким инициатором пользуются для начала реакции. Различают свободнорадикальную (часто – радикальную), катионную, анионную и координационную полимеризации (последняя будет рассмотрена в разделе «Диены»). Как у всех цепных процессов, в реакции полимеризации выделяют стадии: инициирования, роста и обрыва цепи.
Радикальная полимеризация
В качестве инициаторов используют вещества, способные в условиях реакции (нагревание или фотолиз) образовывать свободные радикалы. Чаще всего используют органические пероксиды.
Реакция начинается с образования свободных радикалов. Радикал взаимодействует с алкеном, образуя алкильный радикал, который присоединяется к следующей молекуле алкена и т.д. Этот процесс продолжается до стадии обрыва цепи, которая может произойти разными способами, например, путем рекомбинации двух свободных алкильных радикалов.
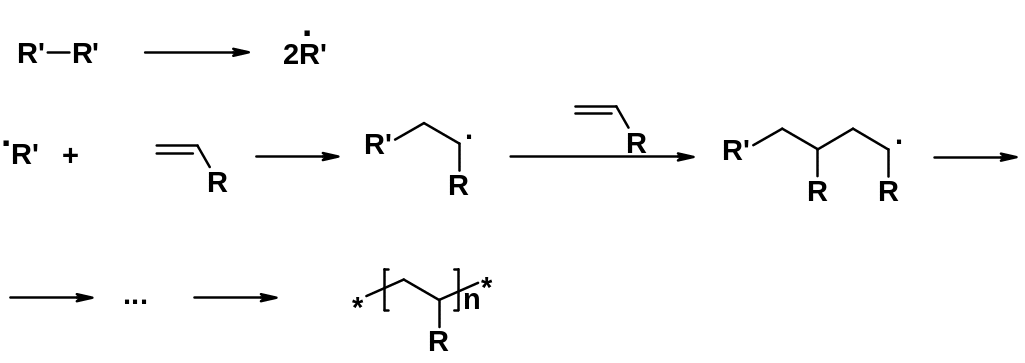
Так как даже следы некоторых веществ могут ингибировать цепной процесс, необходимо использовать очень чистые мономеры. Поэтому мономеры для полимеризации - одни из наиболее чистых органических веществ, производимых в больших масштабах в промышленности.
Чаще всего в радикальной полимеризации используются мономеры, у которых образующийся алкильный радикал стабилизирован за счет электронного влияния заместителей. Хорошим примером такого мономера является стирол.

Катионная полимеризация.
Этот тип полимеризации характерен для алкенов с терминальной двойной связью и двумя донорными группировками, образующими при взаимодействии с электрофилами стабильные третичные катионы. Реакция протекает по цепному ионному механизму под действием минеральных кислот или кислот Льюиса.
Классическим примером катионной полимеризации является получение полиизобутилена, изученное еще А.М. Бутлеровым.
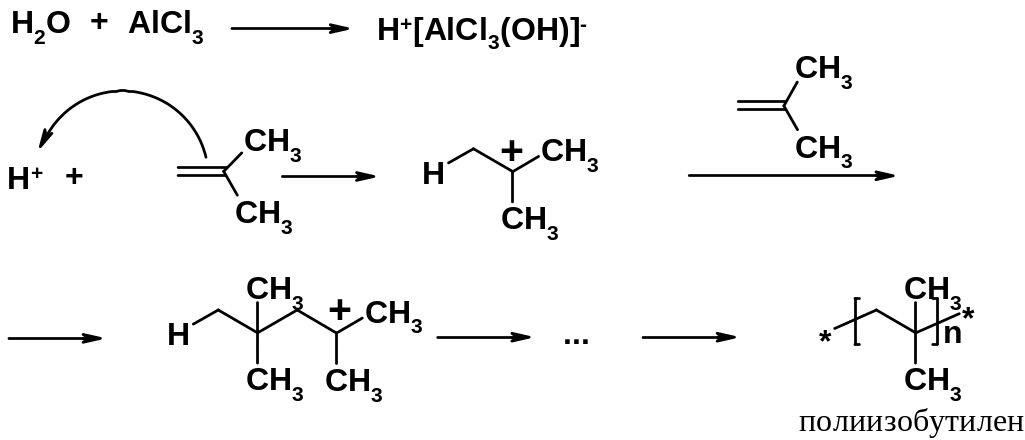
Анионная полимеризация
В этом варианте реакцию инициируют анионные реагенты (NH2-, RO-, металлорганические соединения). Следует помнить, что для этиленовых углеводородов характерны реакции электрофильного присоединения. В случае анионной полимеризации инициатор – нуклеофил. Поэтому взаимодействовать с нуклеофильным инициатором могут только алкены, несущие электроноакцепторные заместители, снижающие электронную плотность -связи.
Классический пример анионной полимеризации – получение полиакрилонитрила.
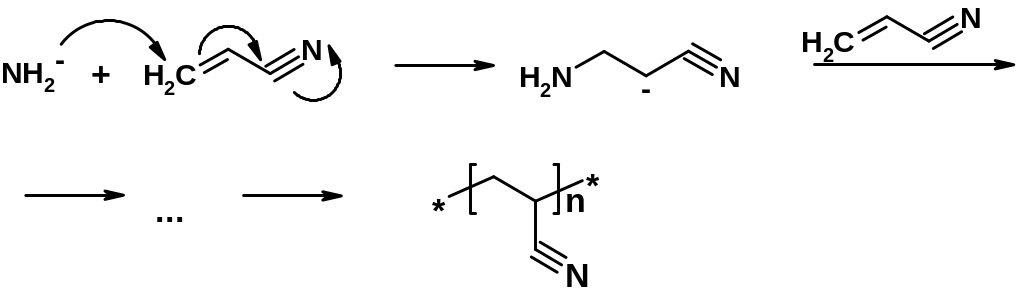
Физико-химические и механические свойства полимеров обусловлены химическим строением, степенью полимеризации, расположением структурных звеньев в пространстве. Чем ближе друг к другу расположены полимерные цепи, тем сильнее Ван-дер-Ваальсово взаимодействие.
Рассмотрим строение полипропилена. Если основная полимерная цепь расположена в плоскости изображения, то метильные группы могут быть расположены тремя способами:
беспорядочно;
по одну сторону от плоскости основной цепи;
попеременно по одну и другую сторону основной цепи.
Соответственно различают:
атактический;
изотактический;
синдиотактический полимеры.
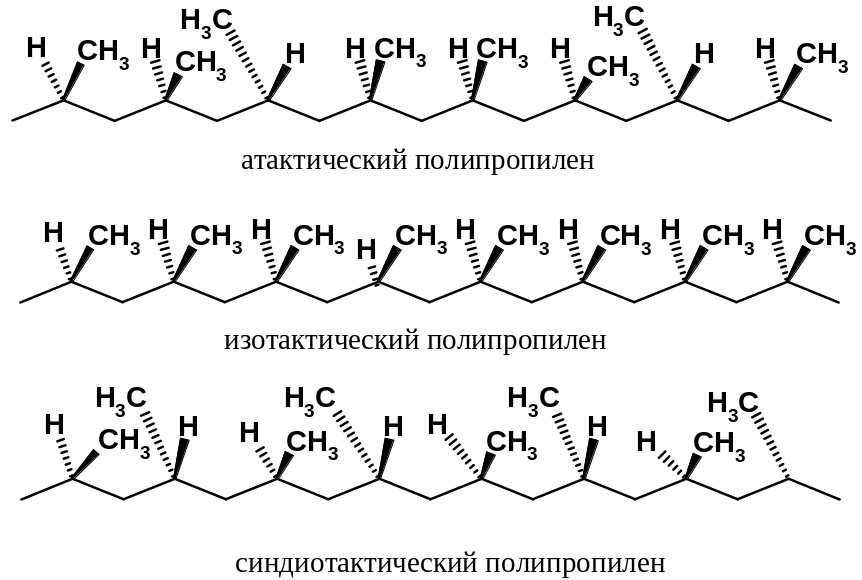
Названия от греческого taktikos – упорядоченный, Isos – равный, одинаковый, Sin – вместе, dio – два.
В атактическом полипропилене из-за беспорядочного расположения заместителей цепи находятся далеко друг от друга. Полимер аморфный, мягкий (Тпл. 80о), получают радикальной полимеризацией. В изотактическом полипропилене цепи могут располагаться намного ближе друг к другу. Полимер кристаллический, намного более прочный. Его Тпл. около 170о, что позволяет производить из него различные медицинские приборы, т.к. его можно легко стерилизовать (Тпл. значительно выше 100о).
Аналогичная ситуация и в случаях получения других ВМС (полистирола, полиметилметакрилата, синтетического каучука и др.).
Стереонаправленный синтез полимеров возможен в результате координационной полимеризации (К.Циглер, Дж. Натта) и будет рассмотрен в разделе алкадиены.
