
- •Лекция №1
- •Предмет органической химии
- •Эмпирические, молекулярные и структурные формулы. Изомерия.
- •Классификация органических веществ.
- •Важнейшие функциональные производные органических веществ
- •Номенклатура органических веществ
- •Лекция № 2
- •Виды химических связей
- •Ковалентная связь
- •Образование молекулярных орбиталей из ао (лкао мо)
- •Электронная конфигурация и гибридизация углерода в органических соединениях
- •Полярность и поляризуемость связей
- •Лекция № 3
- •Классификация органических реакций: по характеру превращения
- •По типу разрыва связи в исходной молекуле
- •Энергетические аспекты химических реакций
- •Механизмы органических реакций
- •Постулат Дж. Хэммонда
- •Лекция № 4
- •Равновесные реакции
- •Кинетический и термодинамический контроль
- •Кислотно-основные свойства органических соединений
- •Кислоты и основания по Брёнстеду-Лоури
- •Кислоты и основания по Льюису
- •Лекция № 5 Углеводороды Алканы
- •Алканы (насыщенные ациклические соединения, парафины)
- •Изомерия, номенклатура
- •Конформационная изомерия
- •Номенклатура
- •Лекция № 6 Углеводороды
- •Химические свойства алканов
- •Механизм реакции галогенирования алканов
- •Лекция № 7 Углеводороды
- •Природные источники и методы получения алканов
- •Получение алканов. Лабораторные и промышленные методы синтеза
- •Лекция № 8 Углеводороды
- •Алкены (олефины, этиленовые углеводороды)
- •Получение алкенов
- •Дегидрогалогенирование алкилгалогенидов
- •Дегидратация спиртов
- •Дегалогенирование дигалогенопроизводных
- •Парциальное (частичное) гидрирование алкинов
- •Лекция № 9 Углеводороды
- •Химические свойства алкенов
- •Присоединение галогенов
- •Присоединение галогеноводородов
- •Лекция № 10 Углеводороды
- •Радикальное присоединение к алкенам
- •Гидратация алкенов
- •Образование галогенгидринов
- •Окисление алкенов
- •Образование эпоксидов
- •Окислительное расщепление двойной связи
- •Озонолиз (реакция Гарриеса)
- •Гидроксилирование алкенов (реакция Вагнера)
- •Лекция № 11 Углеводороды
- •Реакции замещения в алкильных группах алкенов
- •Полимеризация алкенов
Присоединение галогеноводородов
Алкены легко реагируют с галогеноводородами (кроме HF), образуя соответствующие галогенопроизводные алканов.
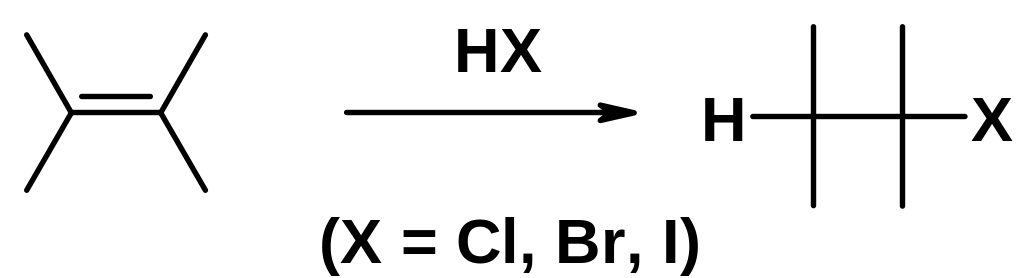
В случае взаимодействия галогеноводорода с несимметричным алкеном возникает вопрос региоориентации реакции, т.е. к какому атому углерода двойной связи присоединяется галоген, а какому - водород.
Например, присоединение бромистого водорода к пропилену может привести к 1-бромпропану или к 2-бромпорпану, либо к смеси этих продуктов. В эксперименте установлено, что преимущественно образуется 2-бромпропан с незначительной примесью 1-изомера.
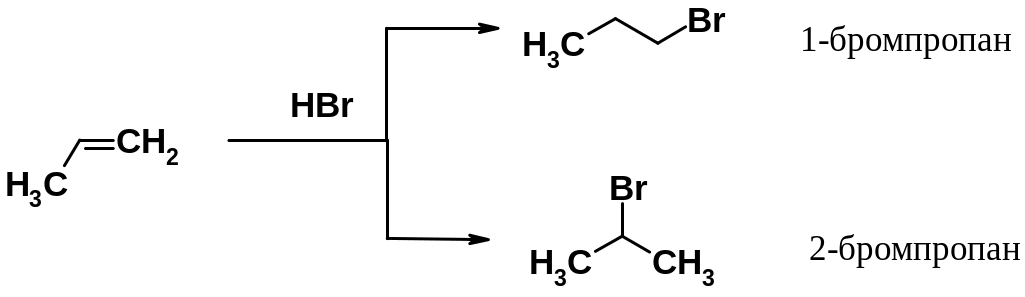
Еще в 1869 г. В. Марковников (Казанский университет) на основе большого числа экспериментальных фактов сформулировал эмпирическое правило:
“Реагент HX присоединяется к несимметричному олефину так, чтобы водород присоединился к наиболее гидрогенизованному (наименее замещенному), а X – к наименее гидрогенизованному (наиболее замещенному) атому углерода двойной связи”.
Таким образом, образование 2-бромпропана происходит в соответствии с правилом Марковникова.
В соответствии с изложенным выше общим механизмом, реакция начинается с атаки электрофильной частицы. В бромистом водороде электрофилом может быть только протон (Н+).
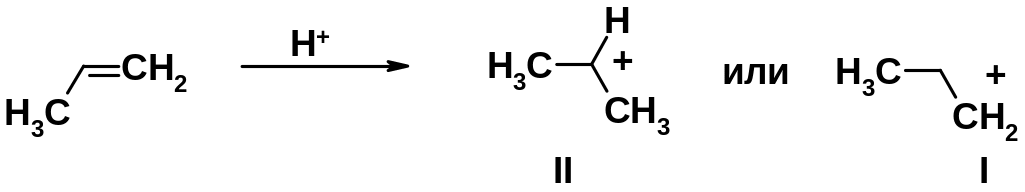
Присоединение протона к двойной связи может теоретически привести к одному из двух карбониевых катионов: первичному (I) или вторичному (II). На практике основной процесс – образование катиона II. Для объяснения этого факта рассмотрим ключевую стадию реакции – присоединение протона.
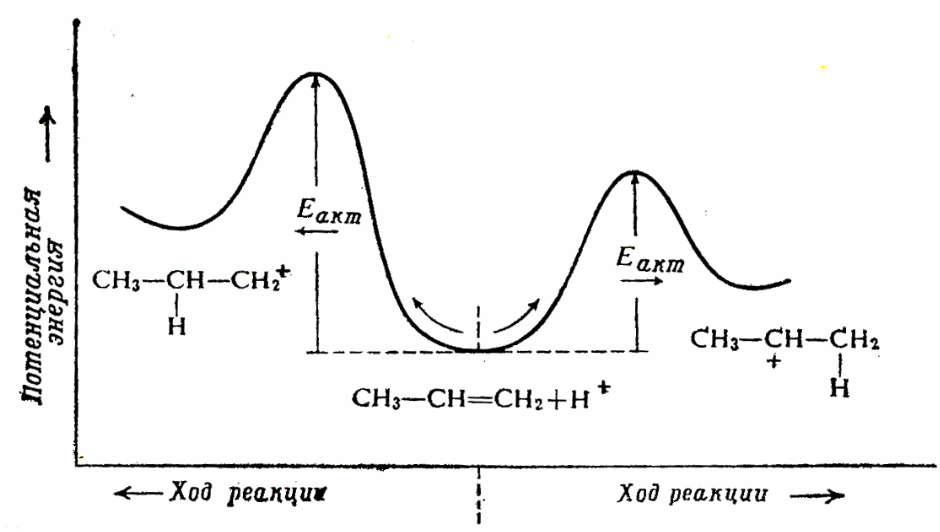
Рис. 9.1. Строение и устойчивость карбокатионов
В общем случае реакция определяется самым энергетически затратным местом на энергетической кривой. В реакции AE это – переходное состояние, возникающее в ходе присоединения протона. Переходное состояние не может быть зарегистрировано какими-либо физическими методами. Но для оценки его строения можно использовать постулат Хэмонда.
В реакциях присоединения к алкенам переходное состояние ближе по энергии к промежуточному продукту (карбокатиону) и, следовательно, структурные факторы, стабилизирующие (понижающие энергию) промежуточный продукт, будут стабилизировать и активированный комплекс.
Рассмотрим, как строение карбониевых катионов влияет на их устойчивость. В зависимости от строения вступающего в реакцию присоединения алкена могут образовываться первичные, вторичные и третичные карбокатионы.
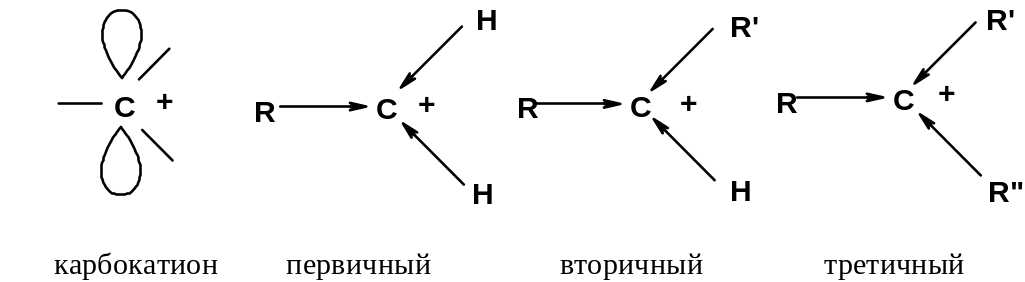
В карбокатионе положительно заряженный атом углерода находится в sp2-гибридном состоянии. Алкильные группы обладают большим положительным индуктивным эффектом по сравнению с атомом водорода. Донорный эффект заместителей, связанных с положительно заряженным углеродом, приводит к увеличению электронной плотности на карбокатионном центре и понижению его энергии. Увеличение числа алкильных групп у карбокатионного центра повышает его стабильность. Устойчивость карбокатионов растет в ряду метильный < первичный < вторичный < третичный.
Образование вторичного карбокатиона II происходит с меньшей энергией активации и большей скоростью, чем первичного карбокатиона I. Это объясняет тот факт, что именно карбокатион II является интермедиатом в рассматриваемой реакции.
Вторая стадия реакции – взаимодействие карбокатиона II с анионом брома – протекает очень быстро и приводит к образованию 2-бромпропана.

Общее правило: электрофильное присоединение к двойной углерод-углеродной связи протекает через образование наиболее стабильного карбокатиона.
«Правило Марковникова» совпадает с современным объяснением региоселективности присоединения несимметричных реагентов к несимметричным алкенам. Но Марковников сформулировал свое правило для объяснения протекания реакций присоединения галогеноводородных кислот исключительно к этиленовым углеводородам. Наличие в молекуле алкена акцепторных группировок приводит к протеканию реакции против правила Марковникова (в редакции автора), но в соответствии с современной трактовкой.

В этом примере вторичный карбокатион менее устойчив, чем первичный, т.к. акцепторная группировка находится рядом с заряженным атомом углерода и дополнительно понижает на нем электронную плотность. В случае первичного карбокатиона акцепторная группа и заряженный атом углерода разделены двумя простыми связями. Поскольку индуктивный эффект проявляется на близких расстояниях, первичный карбокатион будет более стабилен.
Поэтому и в рассматриваемом случае присоединение НХ будет протекать через образование наиболее стабильного – первичного - карбокатиона.
