
- •1. Что такое нефть? Распределение природных горючих ископаемых в земной коре. Топливно-энергетический комплексы рф и мира. Крупнейшие нефте-, газодобывающие и перерабатывающие компании мира и рф.
- •Крупнейшие нпз мира в период 2000-2001 гг.
- •2. Основные теории происхождения нефти: неорганическая, органическая и космическая Происхождение нефти
- •Групповой состав нефти
- •Гетероатомные соединения нефти
- •4. Основные типы классификации нефтей: химическая, технологическая и другие. Классификация нефтей
- •5. Природный и попутный нефтяной газы, химический состав. Что такое газовый фактор? природный газ
- •1. Плотности (нефть, конденсат, н/п).
- •Молекулярная масса
- •Давление насыщенных паров
- •Аппарат для определения давления насыщенных паров нефтепродуктов
- •Критические параметры
- •Критические параметры веществ
- •4. Вязкость
- •7. Оптические свойства нефти и н/п.: цвет, коэффициент преломления, оптическая активность и методы их определения.
- •Коэффициент преломления (рефракции)
- •Зависимость показателя преломления углеводородов от молекулярной массы
- •Оптическая активность
- •8. Температура вспышки, воспламенения и самовоспламенения.
- •Температура вспышки, воспламенения и самовоспламенения
- •Температура воспламенения и самовоспламения
- •Низкотемпературные свойства н/п
- •7.1 Температура помутнения
- •7.2. Температура начала кристаллизации
- •Температура застывания
- •10. Применение ик-спектроскопии к изучению нефти и н/п и газов: основы ик-спектроскопии. Применение ик-спектроcкопии к изучению нефти, нефтепродуктов и газов
- •I. Основы метода ик-спектроскопии
- •2. Расшифровка ик-спектров поглощения
- •Приборы для метода ик-спектроскопии
- •Классификация методов хроматографии
- •12. Основные виды хроматографии: жидкостно-адсорбционная, газо-адсорбционная, жидкостно-жидкостная и газожидкостная хроматографии.
- •2. Детектор по теплоте сгорания (термохимический)
- •3. Пламенно-ионизационный детектор (дип).
- •4. Аргоновый детектор Ловелока.
- •5. Электронно-захватный детектор (эзд)
- •6. Детектор по плотности газов (денситометр или плотномер)
- •Пламенно-фотометрический детектор (пфд).
- •14. Классификация хроматографов.
- •15. Основные хроматографические характеристики: время удерживания и удерживаемый объем, высота и ширина пика, площадь пика и способы их определения
- •Применение газовой хроматографии для исследования углеводородных систем
- •Основные хроматографические характеристики
- •Время удерживания и удерживаемый объем
- •16. Исправленное время удерживания, удерживаемый объем.
- •Влияние скорости газа-носителя на эффективность колонки
- •18. Качественный и количественный хроматографический анализы. Способы идентификации компонентов сложных смесей. Качественный и количественный хроматографический анализы
- •Абсолютная калибровка
- •Содержание компонента, %
- •Внутренняя стандартизация
- •Метод нормализации площадей
- •Классификация установок первичной перегонки нефти
- •Продукты первичной перегонки нефти
- •Комбинированная установка первичной переработки нефти
- •Производительностью 6 млн т/год сернистой нефти:
- •21. Изомеризация пента-гексановой фракции. Катализаторы и схема установки изомеризации пентан-гексановой фракции, основные реакции углеводородов.
- •Переработка природных углеводородных газов
- •1. Изомеризация пентан-гексановой фракции
- •2. Получение мтбэ
- •22. Процессы очистки нефти и н/п: защелачивание основные реакции очистки н/п, демеркаптанизация, процесс «Мерокс», основные реакции очистки н/п.
- •Защелачивание
- •Демеркаптанизация
- •23. Процесс гидроочистки н/п, основные катализаторы, реакции гидрогенолиза гетероатомных соединений, технологические показатели процессов гидроочистка
- •24. Принципиальная схема процессов гидроочистки н/п: бензиновых, керосиновых и дизельных и вакуумных дистиллятов Технологические показатели процессов.
- •Топлива марки рт
- •Го дизельных топлив.
- •Го вакуумных дистиллятов.
- •Каталитический риформинг бензина
- •Каталитический риформинг на получение бензина
- •Каталитический риформинг на получение ароматических углеводородов
- •27. Пиролиз углеводородного сырья, основные реакции пиролиза: реакции изомеризации, замещения, присоединения, рекомбинации, диспропорционирования, цепные реакции. Пиролиз углеводородного сырья
- •28. Технологическая схема установки пиролиза углеводородных фракций. Схема производства эп-300. Основные продукты пиролиза. Пиролиз нефтяного сырья
- •Технологическая схема производства этилена
- •30. Принципиальные схемы процесса и основные технологические показатели. Продукты кк и их использование. Катализаторы процесса кк
- •(Установка rсс):
Приборы для метода ик-спектроскопии
Измерение ИК-спектров поглощения производят при помощи специальных одно- или двухлучевых спектрофотометров. Разница между двумя типами приборов заключается в следующем: при работе на однолучевом приборе для получения спектра поглощения исследуемого соединения необходимо снять кривую излучения источника, пропущенного через кювету с исследуемым веществом и отдельно через кювету, затем необходимо найти отношение координат двух кривых в каждой точке. Следовательно, работа на однолучевом приборе требует большой обработки полученных спектров. При работе на двухлучевом приборе спектр поглощения получается непосредственно в координатах частота - процент пропускания.
Основные узлы обоих типов приборов - источник излучения, монохроматор, приемник излучения и измерительная часть. Рассмотрим кратко особенности этих узлов. В качестве источников излучения в ИК-спектроскопии в основном используется штифт Нернста и силитовый стержень-глобар. Штифт Нернста - это стержень сечением 1,5-2 мм и длиной 30 мм, состоящий из смеси окислов циркония, тория, церия и др. Этот источник дает интенсивное избирательное излучение в средней ИК- области (от 5 до 16 мк). Другой источник - силитовый стержень - глобар длиной 10 см изготовляется из карбида кремния. Дает интенсивное излучение в области больше 16 мк, а в близкой и средней области интенсивность излучения меньше, чем у штифта Нернста.
Для фокусировки лучей в оптической системе ИК-спектрофотометров используются только зеркала, а не линзы. Это объясняется невозможностью изготовления универсальной линзы, пригодной для всех участков в широкой области спектра.
Для диспергирования ИК-лучей обычно применяют призмы, а в некоторых приборах для решения определенных задач - дифракционные решетки. Призмы изготовляются из прозрачных для ИК-лучей монокристаллов галоидных солей щелочных и щелочноземельных элементов (LiF, КВг, NaС1). Кроме того, в области от границы видимого спектра до 4000 см-1 используются призмы из стекла, а до 3400 см-1 - из кварца.
В качестве приемников излучения в инфракрасной спектроскопии в основном применяются два типа тепловых индикаторов: термоэлементы и болометры. Первые представляют собой несколько последовательно соединенных термопар, иногда называемых термостолбиками. В основе их действия лежит явление термоэлектричества. Спаи термопар расположены так, что одни из них (например, четные) подвергаются действию излучения источника, а другие (нечетные) находятся при постоянной температуре. При этом возникает термоэлектродвижущая сила, величина которой зависит от интенсивности падающего излучения.
Болометр - прибор для измерения энергии излучения. Термочувствительные элементы болометров обычно изготовляют из тонких слоев полупроводника (или металлов, диэлектриков), толщиной в несколько микрон или долей микрона.
Под действием падающего излучения в приемниках возникает постоянный ток низкого напряжения, которое может быть измерено с помощью гальванометра чувствительностью 10-8 – 10-9 в. Но применение такого прибора крайне неудобно. Поэтому в современных приборах возникающий в приемниках излучения ток усиливается, затем поступает на потенциометр самописца, перо которого выписывает спектральную кривую пропускания.
Более подробное описание узлов спектрофотометров и принципов их действия приведено во всех инструкциях, прилагаемых к выпускаемым приборам.
Наиболее совершенным двухлучевым спектрофотометром изготовляемым серийно отечественной оптико-механической промышленностью, является прибор ИКС-14А, предназначенный для регистрации спектров поглощения в области от 0,75 до 25 мк. Этот диапазон перекрывается четырьмя призмами: из стекла, фтористого лития, хлористого натрия и бромистого калия. Источник излучения - глобар, приемник -болометр, смена призм - ручная.
Приготовление образцов. Кюветы и оптические, материалы для спектральных исследований
Успешное применение метода ИК-спектроокопии при исследованиях твердых и жидких систем во многом зависит от качества твердых образцов, которые должны иметь достаточно большую удельную поверхность и хорошее пропускание. Последнее зависит от размера частиц, показано, что при диаметре частиц меньше чем длина волны ИК-лучей в тонком слое возможно получить спектр поглощения хорошего качества. Обычно это достигается, если диаметр частиц не превосходит 5 мк. Но, как правило, простым механическим размалыванием очень трудно получить частицы оптимального размера. В настоящее время для приготовления образцов, пригодных для ИК-спектроскопии существует несколько методов.
Метод прессования образца с инертным носителем можно подразделить на два варианта: I) метод совместного- прессования с КВr; 2) метод нанесения твердого вещества на инертную подложку и прессования полученной смеси в таблетки.
В первом случае тонко измельченные порошки твердого тела и оптически чистого КBr - предварительно просеянного через сито 250-300 меш и высушенного при 120-130° С в течение 48 ч прессуются под большим давлением (до 10 т/см2) в прозрачные диски. Для одной пластинки диаметром 20 мм необходимо ориентировочно 150-300 мг КВг и 1-5 мг твердого вещества. Последний может быть приготовлен по методу седиментации.
Этот метод в последнее время критикуют некоторые исследователи, доказывающие, что в системе КBr – твердое вещество возможна химическая реакция между компонентами.
Более широко распространен второй метод приготовления твердого вещества для спектральных опытов, сущность которого заключается в следующем. Порошкообразный кремнезем (аэросил) или γ-Al2O3, имеющие большую удельную поверхность (300-400 м2 /г), смешивают с твердым веществом, затем полученный сухой порошок размалывают в определенную навеску (обычно 15-30 мг на 1 см2 геометрической поверхности образца), прессуют под определенным давлением в таблетки. Последние загружают в вакуумную кювету, в которой производят соответствующие обработки (разложение, восстановление, окисление, откачка). Как правило, хорошее пропускание достигается, если вес твердого вещества в таблетке не превышает 10 % от веса взятого носителя.
Необходимо однако отметить, что γ-Al2O3 является химически довольно активным веществом, способным адсорбировать на своей поверхности реагирующие вещества, полосы поглощения которых могут быть ошибочно отнесены к частотам колебания поверхностных соединений, образующихся на твердом веществе. Кроме того, окись алюминия может также влиять на адсорбционные свойства самого твердого вещества. Поэтому прежде чем применять γ-Al2O3 в качестве носителя, нужно убедиться в его индиферентности к остальным компонентам изучаемой системы.
Аэросил является химически более инертным соединением, однако имеет собственные интенсивные полосы поглощения, которые исключают спектральную область ниже 1400 см-1 из исследования. Кроме того, следует иметь в виду, что аэросил в больших количествах адсорбирует воду и некоторые другие соединения, полосы поглощения которых должны быть учтены при расшифровке спектра.
Для получения спектров поглощения образцы загружают в вакуумную кювету, позволяющую вести откачку, термическую обработку образца. В настоящее время известны кюветы самой различной конструкции. При ее выборе исследователь должен исходить из конкретных условий и задач эксперимента.
Общее требование, предъявляемое к спектральной кювете и к сочлененной с ней вакуумной установке, заключается в обеспечении стерильных условий для опытов, т.е. в исключении возможности попадания паров посторонних веществ на катализатор, в результате чего в спектре могут появиться так называемые паразитические полосы поглощения, не имеющие никакого отношения к изучаемому процессу (пары вакуумной смазки со шлифов, кранов, масло из насосов и др.). Поэтому желательно иметь цельноспаянные установки, или вместо обычных вакуумных кранов применять металлические вентили, затворы и др.
Весьма ответственным этапом и сложной операцией является выбор и способ крепления оптически прозрачных пластинок – «окошеек» к вакуумным кюветам. При этом также следует исходить ив конкретных условий эксперимента. Пластинки из КВг и NaС1 пропускают в широком спектральном диапазоне, поэтому они являются наиболее универсальными и часто применяемыми, однако из-за большой растворимости в воде и склонности к помутнению они крайне неудобны и в случае присутствия паров воды или других агрессивных веществ не применимы.
LiF и СаF2 значительно меньше растворяются в воде, поэтому им можно отдать предпочтение, если изучаемые частоты находятся в пределах пропускания этих пластинок.
Менее распространенными материалами, но обладающими некоторыми преимуществами, являются пластинки из монокристаллов бромистого таллия- йодистого таллия (KRS-5), бромистого таллия - хлористого таллия (KRS-6) и кремния. Они пропускают в широком спектральном диапазоне и плохо или вовсе не растворяются в воде. Кроме того, пластинка из кремния может быть спаяна с кюветой (из стекла пирекс), и поэтому позволяет записывать спектры при повышенных температурах без охлаждения места соединения окошка с кюветой. Недостатки этих пластинок - их высокая стоимость и меньшая величина пропускания 50-60%.
Обычно пластинки прикрепляют к кювете при помощи различных клеев, замазок или смол ( БФ, суперцемент, эпоксидная и глифталевые смолы, пицеин и др.), обеспечивающих вакуумноплотное присоединение окошек. Следует однако иметь в виду, что некоторые из этих материалов имеют довольно высокую упругость пара (например, пицеин), который может адсорбироваться на твердых веществах, приводя к появлению паразитических полос поглощения.
В заключение нужно отметить, что в настоящее время универсальных правил для получения хорошего ИК-спектра жидких и твердых веществ, смесей, систем нет. Все экспериментальные условия: выбор методики получения и концентрации жидких и твердых веществ, давления и продолжительности прессования таблеток подбираются эмпирическим путем.
11. Применение хроматографии для исследования углеводородных систем. Классификация методов хроматографии: адсорбционная, распределительная, осадочная хроматография
Применение газовой хроматографии для исследования углеводородных систем
Впервые идею хроматографического метода высказал русский ученый-ботаник Михаил Семенович Цвет в использовании для разделения веществ их различную степень адсорбироваться на адсорбенте (избирательная адсорбция).
В 1903 г. М. С. Цвет опубликовал в трудах Варшавского общества естествоиспытателей статью, в которой сформулировал принцип нового метода и наглядно показал возможность отделения зеленой части хлорофилловых пигментов листьев (хлорофиллинов) от желтой (ксанто-филлинов) и от оранжевой (каротина) с помощью адсорбентов. В более поздних работах М. С. Цвет значительно усовершенствовал свой метод и дал ему необходимое теоретическое и экспериментальное обоснование. Однако не всем исследователям удавалось воспроизвести опыты М. С. Цвета при его жизни и вскоре этот метод был предан забвению.
О его методе вспомнили через 27 лет после его открытия немецкие биохимики Кун, Ледерер и Винтерштейн, которые в 1930 г. успешно разделили каротин на отдельные изомеры, предсказанные Цветом. С этого времени хроматография стала развиваться в самых разнообразных направлениях и со временем приобрела характер самостоятельной научно-технической дисциплины, претерпев, таким образом, второе рождение.
Хроматографический метод, как показывает его название, предназначался для исследования окрашенных веществ. Однако уже на заре развития метода М. С. Цвет высказал предположение, что его метод применим не только к окрашенным, но и к бесцветным веществам. Но первоначально применению хроматографии для разделения бесцветных веществ мешало отсутствие приборов, с помощью которых можно было бы контролировать в ходе опыта процесс разделения,— детекторов.
В настоящее время разработаны детекторы, позволяющие анализировать самые разнообразные соединения. В простейшем варианте метода Цвета исследуемый раствор окрашенных веществ фильтруют под небольшим разрежением, создаваемым водоструйным насосом, через стеклянную колонку, заполненную бесцветным адсорбентом, затем проявляют хроматограмму чистым растворителем. При правильно поставленном эксперименте вдоль колонки появляется ряд окрашенных поперечных полос, содержащих разделенные компоненты исследуемой смеси.
Проведение хроматографического опыта в таком простейшем варианте видно из рис. 1.
Современная хроматографическая установка включает разделительную колонку, термостат, детектор, блоки управления и другие вспомогательные приспособления.
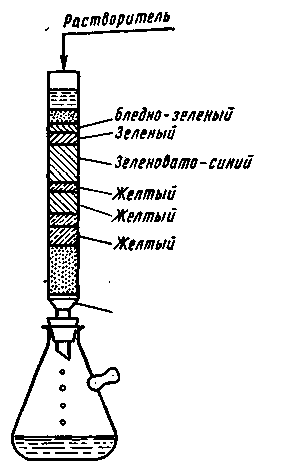
Рис. 1. Хроматограмма хлорофилловых пигментов по М.С. Цвету
Начиная с 1931 г. число публикаций, посвященных применению хроматографии, с каждым годом увеличивалось, прежде всего в биохимии. Это можно объяснить тем, что биохимикам чаще приходится исследовать термически неустойчивые биологически активные материалы и хроматография здесь оказалась наиболее эффективным методом исследования их состава.
Кроме того, все работы М. С. Цвета были опубликованы в биологической литературе, вследствие чего химикам его метод долгое время оставался неизвестным. Кроме хлорофилловых пигментов этим методом были успешно разделены и выделены в чистом виде другие биологически активные вещества: витамины, ферменты, гормоны, энзимы, аминокислоты, алкалоиды.
Применение хроматографии в органической, неорганической и аналитической химии началось значительно позднее, чем в биологии. Первые публикации, посвященные применению метода Цвета в неорганическом анализе, относятся к 1937 г. и принадлежат Швабу и его сотрудникам. В этих работах приведена методика качественного анализа смесей некоторых катионов и анионов на стеклянной колонке с оксидом алюминия, причем техника проведения анализа почти не отличается от той, которую применял Цвет.
Значительные успехи в разделении и анализе неорганических веществ были достигнуты в 50-х годах, когда в практику хроматографии были введены в качестве адсорбентов ионообменные смолы. Стимулом к этому послужила задача изучения токсичности радиоактивных продуктов расщепления урана и плутония при атомном взрыве и в атомном реакторе. Такими продуктами являются соединения редкоземельных элементов с примесью их радиоактивных изотопов. Применение хроматографии на ионообменных смолах в качестве адсорбентов позволило выделить почти все эти продукты и подробно изучить биологическую активность и другие физико-химические свойства каждого продукта в отдельности, что сыграло большую роль в развитии атомной и ядерной техники.
Кроме ионообменной хроматографии, для разделения и анализа катионов и анионов советские ученые Е. Н. Гапон и Т. Б. Гапон в 1948 г. предложили осадочную хроматографию. В этом варианте метода Цвета формирование хроматограмм обусловлено не различием адсорбируемости или коэффициентов распределения, а процессом образования осадков и различием в их растворимости. Это и вызывает разделение тех ионов, которые вошли в состав осадков при реакции с реактивом-осадителем, нанесенным на сорбент хроматографической колонки или на фильтровальную бумагу.
Хроматографический анализ органических веществ развивался попутно с хроматографией неорганических веществ. В 1935— 1936 гг. появились первые сообщения об успешном применении метода Цвета в анализе синтетических красителей. Из жидкофазных вариантов хроматографии наиболее широкое применение в органической и биологической химии получила бумажная хроматография.
Это тонкий микрометод, позволяющий разделять смеси нескольких десятков компонентов на полоске пористой бумаги, которая выполняет роль хроматографической колонки. Хроматограмма получается в виде пятен, окраска которых соответствует природной окраске разделяемых компонентов смеси. При анализе бесцветных веществ пятна проявляют, опрыскивая бумагу реактивом, образующим с разделяемыми компонентами окрашенные соединения. Например, при определении аминокислотного состава белков после их гидролиза бумагу опрыскивают раствором нингидрина, в результате чего на поверхности бумаги появляются пятна розового цвета, соответствующие индивидуальным аминокислотам. Если разделяемые бесцветные вещества обладают способностью к флуоресценции, бумагу облучают ультрафиолетовыми лучами (кварцевой или ртутной лампой) и тогда хроматограмма становится видимой. Этот случай можно наблюдать при разделении смеси антрахинонов, пятна которых в ультрафиолетовом свете ртутной лампы окрашены в сине-фиолетовый цвет.
Аналогичная картина разделения веществ (в основном органического происхождения) получается на стеклянной пластинке, покрытой слоем мелкодисперсного сорбента (оксида алюминия, силикагеля, целлюлозы, крахмала и др.). Это так называемая тонкослойная хроматография, получившая за последние годы широкое применение в химии и особенно в биохимии благодаря значительно большей скорости выполнения анализа по сравнению с бумажной хроматографией. Кроме того, методом тонкослойной хроматографии можно разделять примерно на порядок большие количества смесей без существенного ухудшения качества разделения. Это преимущество позволяет применять тонкослойную хроматографию как препаративный метод выделения индивидуальных продуктов из сложной смеси в чистом виде. Несмотря на широкие возможности применения, жидкофазная хроматография ни в колоночном, ни в бумажном, ни в тонкослойном варианте не могла удовлетворить требования быстро развивающейся (в отмеченный период) науки и промышленности.
Химическая промышленность синтетических материалов и пластмасс, использующая в качестве сырья в основном смеси природных газов, требовала эффективных методов анализа. Старые химические методы анализа ни в коей мере не могли решить эту задачу, что и послужило толчком к развитию газовой хроматографии, получившей широкое применение в контроле производства и научных исследованиях, особенно в нефтехимии. Однако и жидкофазная хроматография, особенно колоночная молекулярная, не потеряла своего значения. За последние годы наблюдается ее возрождение благодаря значительным успехам в области хроматографического приборостроения. Созданы совершенные жидкофазные хроматографы с высокочувствительными детекторами и автоматической записью хроматограммы, аналогично тому, как это происходит при анализе смесей на газовых хроматографах.
В настоящее время высокоэффективная, высокоскоростная жидкостная хроматография широко применяется для анализа малолетучих высокомолекулярных и нетермостабильных соединений. Это возрожденный открытый М. С. Цветом вариант молекулярной жидкостной хроматографии, модернизированный путем использования новых высокоэффективных сорбентов, высоких давлений на входе в колонку, высоких скоростей элюента и автоматического детектирования.
Лекция 7
