
- •8 Глав 57 параграфов. 16ти нет Физика Введение. Дуализм света. Опыт Боте.
- •Глава 1. Действие света. §1 Фотоны.
- •§2 Фотоэффект.
- •1. Основные особенности фотоэффекта.
- •2. Объяснение фотоэффекта с точки зрения волновой и квантовой теорий.
- •3. Селективный, внутренний, вентильный фотоэффект.
- •§3 Применение фотоэффекта.
- •§4 Давление света.
- •§5 Явление Комптона – рассеяние рентгеновского кванта на «свободном» электроне.
- •1. Физическая сущность
- •2. Элементарная теория комптоновского эффекта
- •3. Выводы
- •2. Квантовая гипотеза. Формула Планка.
- •3. Следствие из формул Планка.
- •2. Строение атома.
- •§2 Модель Томпсона.
- •§3 Опыты Резерфорда.
- •§4 Энергия электрона в атоме.
- •Глава 3. Теория Бора. §1 Несостоятельность классической модели атома.
- •§2 Постулаты Бора. (1913)
- •§3 Опыты Франка и Герца. (1913)
- •§4 Теория атома водорода и водородоподобных ионов по Бору.
- •1.Эксперементальные факты, объясняемые теорией Бора:
- •§2 Экспериментальное подтверждение гипотезы де Бройля. Опыты Дэвисона и Джермера. 1927-1923.
- •§3 Общие свойства волн. Волновой пакет.
- •§4 Свойства волн де Бройля.
- •4)Дисперсия волн де Бройля
- •5)Волны де Бройля и второй постулат Бора. (правило квантования орбит)
- •§5 Соотношение неопределенностей Гейзенберга.
- •1)Разрыв однозначных связей между p и X в квантовой механике
- •§6 Волны де Бройля и волновая функция.
- •§7 Вероятностное толкование волн де Бройля.
- •§8 Вероятность нахождения мкч.Нахождение средних значений функции от координат. (роль ψ –фунукции в квантовой механике)
- •Глава 5. Уравнение Шредингера. §1 Особенности волнового уравнения для микрочастицы.
- •§2 Общий вид уравнения Шредингера от времени.
- •§3 Уравнение Шредингера для стационарных состояний.
- •§4 Уравнение Шредингера для n частиц
- •§5 Анализ решений уравнений Шредингера
- •1.Сравнение с обычным волновым уравнением:
- •2.Начальные и граничные условия
- •3. Стандартные естественные условия
- •4. Собственные значения и собственные функции
- •Глава 6. Применение квантовой механики. §1 Движение мкч в свободном пространстве.
- •1.Уравнение Шредингера и его решение
- •2.Собственные функции оператора энергии
- •3. Собственные значения энергии
- •§2 Движение мкч в потенциальном ящике.
- •§3 Отражение и прохождение мкч через Потенциальный барьер.
- •2.Уравнение Шредингера и его решение
- •3.Микро и макро частицы на грани 2х сред
- •4.Определение коэффициента отражения r и коэффициента прозрачности d
- •5.Частные случаи
- •§4 Прохождение микрочастицы через потенциальный барьер конечной ширины. Туннельный эффект.
- •§5 Микрочастица в потенциальной яме конечной глубины.
- •§6 Квантово-механический осциллятор
- •1.Гармонический осциллятор
- •2.Классический гармонический осциллятор
- •3.Квантово-механический осциллятор
- •§7 Квантово-механическая модель атома.
- •1.Качественное рассмотрение
- •2. Уравнение шредингера для электрона в атоме водорода
- •3.Квантовые числа
- •4.Спектр атома водорода. Правило отбора.
- •5.Сферич. Симметрич. Случай. (1s сост)
- •6. Местонахождение электрона в атоме в 1s состоянии
- •§8 Магнитные свойства и спин электрона.
- •Глава 6. Применение квантовой механики. §1 Принцип Паули (1925).
- •§2 Распределение электронов в сложных атомах по оболочкам. Таблица Менделеева.
- •§3 Спектр сложных атомов.
- •1.Рентгеновские спектры.
- •2.Тормозное рентгеновское излучение (белое)
- •Глава 7. Элементы квантовой статистики. Проводимость металлов. §1 Понятие о квантовой статистике.
- •§3 Динамика электрона в кристаллической решетке. Эффективная масса электрона.
- •II з. Ньютона
3.Квантовые числа
1)Главное квантовое число n=1,2,3…
E = - (1/n2) (k2me4/2ћ2)
2) Орбитальное квантовое число l=0,1,2,…,(n-1)
Характ. Орбит. Момент.
L=sqr(l(l+1)) ћ, L=[r,P] (вект), p=mV(вект)
3) магнитное квантовое число me= 0, +-1,+-2,…,+-l
Lz = me ћ
Состояние электрона в атоме
Таблица:
n l me сост
1 0 0 1S
2 0|1 0|-1 0 1 2S|2p
3 0|1|2 0|-1 0 1|-2 -1 0 1 2 3S|3p|3d
При одном и том же n может быть несколько состояний. Состояние электрона с одинаковой энергией называются вырожденными.
Кратность вырождения N
n, l – n значений m=(2n+1)
N=∑(от эль до n-1)(2l + 1) = 1+3+5…
N=(1+2n-2+1)n/2=n2
4.Спектр атома водорода. Правило отбора.
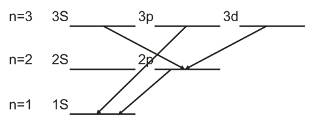
∆l = +-1
∆me = 0,+-1
Правило отбора отражает закон сохранения импульса.
Серия лаймана (n,p --- 1S), n=2,3…
Серия Бальмира (nS --- 2p), (nd---2p), n=3,4
5.Сферич. Симметрич. Случай. (1s сост)
(1/r2)( ∂/∂r)(r2∂ ψ /∂r) + (1/r2Sinθ)(Sinθ∂ ψ /∂θ) + ( 1/r2Sinθ)( ∂2 ψ /∂ φ 2) + (2m /ħ2)(E + ke2/r) ψ =0
ψ (r,θ,φ)
∂ ψ /∂ θ = 0 ∂ ψ /∂ φ = 0
(1/r2)( ∂/∂r)(r2∂ ψ /∂r) + (2m /ħ2)(E + ke2/r) ψ =0
(1/r2) 2r ( ∂ ψ /∂r) (1/r2) r2∂ 2ψ /∂r2 + (2m /ħ2)(E + ke2/r) ψ =0
∂ 2ψ /∂r2 + (2/r) ( ∂ ψ /∂r) + (2m /ħ2)(E + ke2/r) ψ =0
ψ = e -ar
∂ ψ /∂r = -a ψ
∂ 2ψ /∂r2 = a2 ψ
a2 ψ – (2a ψ/r) + (2m /ħ2)(E + ke2/r) ψ =0
a2 – (2a /r) + (2m /ħ2)(E + ke2/r) =0
(a2 + 2mE /ħ2) + (2/r)( kme2/ћ2 -a) =0
kme2/ћ2 -a =0
a = kme2/ћ2 a=1/r
ψ = e -2/r
a2 + 2mE /ħ2 =0
E= - ħ2a2/2m = - ħ2k2m2e4/2mћ4 = - k2m2e4/2ћ2
6. Местонахождение электрона в атоме в 1s состоянии
ψ = Ae -r/r1 A – нормирующий множитель
(интеграл от 0 до бескон.)( A2e -2r/r1)dV = (интеграл от 0 до бескон.)( A2e -2r/r14Pir2)dr = 1
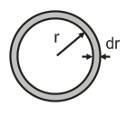
dV=4Pir2dr
4Pi A2(интеграл от 0 до бескон.)( r2 e -2r/r1) = 1
A2 Pir13=1
A = sqr (1/ Pir13)
ψ = e -r/r1/ sqr ( Pir13)
dW = | ψ 2|dV
dW = (e -2r/r1/ ( Pir13)) 4Pir2dr – вероятность обнаружить электрон в dr
Радиальная плотность вероятности:
ρ(r) = dW/dr = (1/ Pir13) (e -2r/r1) 4Pir2
r стремится к 0, ρ(r) стремится к 0
r стремится к бесконечности, ρ(r) стремится к 0
∂ ρ(r) /∂ r = 0
(4/ r13)((-2/ r1) (e -2r/r1)r2 + 2r(e -2r/r1))=0
(4/ r13)( 2 r e -2r/r1)(1 – r/r1) = 0
1 – r/r1 = 0
r = r1 – максимальный радиус плотности вероятности
Сравнение с теорией Бора
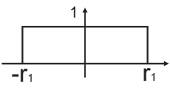
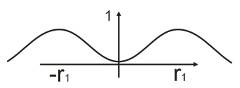
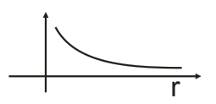
ψ = e -r/r1/ sqr ( Pir13)
§8 Магнитные свойства и спин электрона.
Энергетические уровни электрона в атоме расщепляются изза того, что электрон имеет магнитный момент.
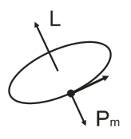
L = [r, mV] – момент импульса
Pm = JS
Pm / L = l/2m
В квант механике
L= sqr(l(l+1)) ħ
L=n ħ по Бору
(l/2m) ħ sqr(l(l+1))
----------
Pm = - eL/2m (вект) – орбитальным магнитный момент
e/2m – гиромагнитное отношение
по квантово-механической модели:
L = sqr(l(l+1)) ħ – закон квантования магнитных моментов
Pm = sqr(l(l+1))μб
μб = e ħ /2m – минимальная порция магнитного момента в природе
Запустили в состояние 1S => L=0
Если L=0 атомы прошли и с МП(магнитное поле?) не взаимодействовали. НО
Опыты Штерна и Германа
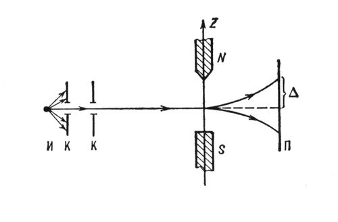
F = μ (∂B/∂x)Cosα
Cosα = (μ, B) (вект)
1S n=1 l=0 me=0 Pm=0
Опыт состоял в следующем: пучок атомов серебра пропускали через сильно неоднородное магнитное поле, создаваемое мощным постоянным магнитом. При прохождении атомов через это поле, в силу обладания ими магнитных моментов, на них действовала зависящая от проекции спина на направление магнитного поля сила, отклонявшая летящие между магнитами атомы от их первоначального направления движения. Причём, если предположить, что магнитные моменты атомов ориентированы хаотично (непрерывно), то тогда на расположенной далее по направлению движения атомов пластинке должна была проявиться размытая полоса. Однако вместо этого на пластинке образовались две достаточно чёткие узкие полосы, что свидетельствовало в пользу того, что магнитные моменты атомов пучка принимали лишь два определённых значения, что подтверждало предположение квантово-механической теории о квантовании магнитного момента атомов.
Гипотеза об электронном спине
У электрона есть собственный магнитный момент
Ls – спиновый механический момент (момент импульса)
Pms – спиновый магнитный момент
1925 Гаудсмит и Уленберг (1я теория. не прошла.)
S=1/2 ms = +-1/2
Ls = sqr(S(S+1)) ħ Ls = sqr(3) ħ /2
S – спиновое квантовое число
|Pms| = e Ls / m = (e ħ / m) sqr(S(S+1)) = sqr3 μб
Проекция на выбранное направление z:
Pmsz = e Lsz / m = e sqr3 ms ħ / m 2 = +- μб
Lsz = ms ħ
Электрон движется по орбите. У него будто маленькая магнитная стрелочка.
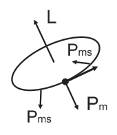
Объяснение расщепления спектральных линий:
Без учета спина:
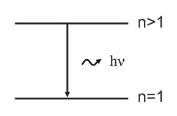
С учетом спина:
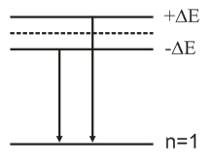
Уровень расщепляется, линии носят дублетный характер
Тонкая структура линий.
