
- •Москва медицина 1998 Издание рекомендовано для перевода академиком рамн
- •Майкл Ферранте
- •Значимость проблемы послеоперационной боли
- •Распространенность проблемы по данным исследований
- •Распространенность проблемы по хирургическим данным
- •Боль, обусловленная хирургическим вмешательством (в порядке снижения интенсивности)1 Операции на желудке
- •Сопоставление разных методов аналгезии (международное исследование)
- •Региональная анестезия/аналгезия и легочные осложнения
- •Региональная анестезия/аналгезия и заболевания в послеоперационном периоде
- •Аналгезия, контролируемая пациентом
- •Премедикация и техника анестезии
- •Факторы, обусловливающие неадекватный контроль послеоперационной боли
- •Недостаток рутинной количественной оценки
- •Побочное действие анальгетиков
- •Индивидуальные различия реакции на анальгетики
- •Направления и пути решения
- •Периферическая нервная система Основы анатомии
- •Микроскопическое строение
- •Трансдукция Характеристика ноцицепторов
- •Категории ноцицепторов
- •Миелинизированные ноцицепторы
- •Немиелинизированные ноцицепторы
- •Роль ноцицепторов в перцепции боли
- •Сенсибилизация и гиперсенсибилизация
- •Биохимические субстраты
- •Трансдукция в глубоких соматических тканях
- •Суставы
- •Трансдукция в висцеральных органах
- •Резюме по вопросам трансдукции
- •Центральная нервная система
- •Ультраструктура спинного мозга
- •Ультраструктура головного мозга
- •Главные структуры ствола мозга
- •Таламус
- •Трансмиссия Первичные афферентные волокна в заднем корешке
- •Первичные афферентные волокна в спинном мозге
- •Терминалы первичных афферентов
- •Нейротрансмиттеры первичных аффекторов
- •Трансмиссионные клетки в спинном мозге Анатомия
- •Центральная гиперсенсибилизация, или нервное перевозбуждение
- •Восходящие ноцицептивные проводящие пути
- •Спиноталамический путь (стп)
- •Вентральный спиноталамический путь
- •Спинно-ретикулярный путь (срп)
- •Спинно-мезэнцефалический путь (смп)
- •Дорсальный столб постсинаптической спинно-медуллярной системы
- •Проприоспинальная мультисинаптическая восходящая система
- •Ростральные центры Ретикулярная формация
- •Таламус
- •Гипоталамус и лимбическая система
- •Кора мозга
- •Резюме по вопросам трансмиссии
- •Модуляция
- •Аналгезия, возникающая при стимуляции
- •Аналгезия, обеспечиваемая опиоидами
- •Анатомия нисходящей модулирующей системы Средний мозг
- •Продолговатый мозг
- •Кора и промежуточный мозг
- •Нейротрансмиттеры нисходящих проводящих путей Норадреналин
- •Серотонин
- •Эндогенные опиоиды
- •Резюме по вопросам модуляции
- •Пути контроля теории боли
- •Периферический отдел автономной нервной системы
- •Ганглии и сплетения периферического отдела автономной нервной системы
- •Эндокринные
- •Обменные
- •Обмен липидов
- •Стрессовые гормоны - это еще не результаты (некоторые предостережения)
- •Заключение
- •Структуры, расположенные в позвоночном канале Спинной мозг
- •Кровоснабжение позвоночного канала Артерии
- •Методы, вызывающие боль Турникетный болевой тест
- •Побочные действия
- •Гастропатия
- •Нспвп и преодоление боли в послеоперационном периоде
- •Опиоиды
- •Соотношение структуры и активности
- •Фармакодинамика Эндогенные опиоидныс пептиды
- •Опиоидные рецепторы
- •Классификация типов рецепторов и их предполагаемое действие
- •Связывание рецепторов и их реакция: истинная активность
- •Пути поступления препаратов
- •Проникновение к рецепторам
- •Фармакология Действие на центральную нервную систему
- •Гипнотическое действие опиоидов (в порядке снижения активности)
- •Метадон
- •Меперидин
- •Алкалоиды Морфин
- •Синтетические опиоиды Леворфанол (лево-дроморан)
- •Метадон (дольфин)
- •Смешанные агонист-антагонисты Налбуфин (нубаин)
- •Частичные агонисты Бупренорфин (бупренекс)
- •Пероральные антагонисты Налтрексон
- •Заключение
- •Список литературы
- •Соотношение рКд к процентному содержанию основных форм и время развития 50% проводникового блока в изолированном нерве
- •Факторы, влияющие на анестезиологическую активность
- •Дозировка
- •Добавки
- •Беременность
- •Фармакокинетика
- •Абсорбция
- •Распределение
- •Метаболизм и выведение
- •Токсичность
- •Общая токсичность
- •Токсичность для центральной нервной системы
- •Токсичность для сердечно-сосудистой системы
- •Различные системные эффекты
- •Аллергические реакции
- •Местное токсическое воздействие
- •Осложнения региональной анестезии
- •Эпидуральная анестезия
- •Уровень блокады
- •Доза препарата
- •Особенности локального анестетика
- •Дополнительное введение вазоконстрикторов
- •Волемическое состояние, объем циркулирующей крови
- •Спинальная анестезия
- •Препараты для локальной анестезии Препараты из группы аминоэфиров Кокаин
- •Прокаин (новокаин)
- •Хлоропрокаин
- •Тетракаин
- •Препараты из группы аминоамидов Лидокаин
- •Мепивакаин
- •Прилокаин
- •Бупивакаин
- •Этидокаин
- •Другие препараты Дибукаин
- •Бензокаин
- •Заключение
- •Список литературы
- •Внутривенная аналгезия, контролируемая пациентом Определение методов акп и параметры дозировок
- •Инфузионная технология акп
- •Характеристика прибора
- •Факторы, относящиеся к оценке акп-инфузоров
- •Безопасность
- •Неблагоприятные реакции и побочное действие
- •Проблемы, связанные с работой приборов (механические проблемы)
- •Взаимодействие прибора и пользователя
- •Образец (парадигма) акп
- •Непрерывная инфузионная аналгезия для преодоления острой боли
- •Индивидуализация требований аналгезии
- •Вопросы фармакокинетики
- •Факторы фармакодинамики
- •Психологические факторы
- •Подкожная аналгезия, контролируемая пациентом
- •Эпидуральная аналгезия, контролируемая пациентом
- •Заключение
- •Список литературы
- •Клиническое использование эпидурального введения опиоидов Механизм действия
- •Значение растворимости в липидах
- •Опиоиды; обычно используемые для эпидурального введения
- •Клиническая характеристика эпидуральных опиоидов (после однократной инъекции)
- •Наступление аналгезии
- •Продолжительность аналгезии
- •Ростральная миграция в цсж
- •Место инъекции
- •Интермитткрующие инъекции или продолжительные инфузии?
- •Опиоиды, обычно используемые для эпидуральных инфузий 1
- •Клиническая практика госпиталя Brigham и женского госпиталя
- •Показания к применению
- •Субарахноидальное введение опиоидов в клинике
- •Побочное действие спинальных опиоидов
- •Угнетение дыхания
- •Тошнота
- •Задержка мочи
- •Активация латентной герпетической инфекции
- •Угнетение функции желудочно-кишечного тракта
- •Неврологические эффекты
- •Мониторинг
- •Заключение
- •Список литературы
- •Балансированная аналгезия
- •Эпидуральное введение локальных анестетиков
- •Влияние эпидуральной блокады на сердечно-сосудистую систему
- •Интермиттирующие инъекции
- •Продолжительные инфузии
- •Тахифилаксия
- •Общие сведения
- •Механизм тахифилаксии
- •Гипотетические механизмы тахифилаксии при эпидуральном введении локальных анестетиков
- •Клинические особенности эпидуральной анестезии при комбинации локальных анестетиков и опиоидов Синергизм аналгезии
- •Клинические особенности совместного назначения локальных анестетиков и опиоидов
- •Угнетение тахифилаксии
- •Угнетение центральной гиперсенсибилизации: концепция преимущественной аналгезии
- •Угнетение ноцицептивной трансмиссии: афферентный «барраж»
- •Продолжительность действия
- •Клинические исследования
- •Совместное эпидуральное применение локальных анестетиков и опиоидов
- •Эпидуральные инфузии локальных анестетиков и опиоидов: клиническая практика госпиталя -brigham и женского госпиталя
- •Комбинации локальных анестетиков и опиоидов для эпидуральной инфузии
- •Приготовление некоторых растворов для эпидурального введения
- •Выявление нарушений
- •Обычные проблемы, возникающие при проведении эпидуральной аналгезии
- •Осложнения и побочное действие
- •Заключение
- •Список литературы
- •Анатомия
- •Механизм действия
- •Методика Паховый параваскулярный метод
- •Противопоказания
- •Применение в клинике
- •Заключение
- •Список литературы
- •Анатомия
- •Симпатическая иннервация верхней конечности
- •Методика
- •Процедура Подмышечный подход
- •Межскаленный подход
- •Подключичный периваскулярный доступ
- •Подключичный (инфраклавикулярный) доступ
- •Выбор локального анестетика и его дозировка
- •Применение в клинике
- •Осложнения
- •Токсическое действие локальных анестетиков
- •Повреждение нерва
- •Заключение
- •Список литературы
- •Анатомия
- •Механизм действия
- •Методика Положение пациента и ориентиры
- •Выполнение процедуры
- •Возможные технические трудности
- •Варианты методики
- •Выбор локального анестетика и его дозировка
- •Интервалы между повторными введениями
- •Применение в клинике
- •Осложнения Недостаточная аналгезия
- •Пневмоторакс
- •Повреждение сосудов
- •Токсическое действие локального анестетика
- •Повреждение нерва
- •Заключение
- •Список литературы
- •Анатомия
- •Механизм аналгезии
- •Методика
- •Положение пациента и ориентиры
- •Выполнение процедуры
- •Выбор локального анестетика и его дозировка Концентрация бупивакаина
- •Объем вводимого раствора
- •Другие локальные анестетики
- •Адреналин
- •Интервалы между повторными введениями Интермиттирующие инъекции
- •Длительные внутриплевральные инфузий
- •Применение в клинике
- •Протокол по интермиттирующей дозировке препарата в случае установки внутриплеврального катетера
- •Применение в клинике внутриплевральной региональной аналгезии
- •Причины неэффективности внутриплевральной региональной аналгезии после операции торакотомии
- •Осложнения
- •Пневмоторакс
- •Токсическое действие локального анестетика
- •Противопоказания
- •Заключение
- •Список литературы
- •Анатомия
- •Механизм действия
- •Методика Положение пациента и ориентиры
- •Выполнение
- •Варианты методики
- •Выбор локального анестетика и интервалы между повторными введениями
- •Применение в клинике
- •Сообщения об аналгезии при использовании паравертебральной невральной блокады в грудном отделе
- •Осложнения
- •Список литературы
- •Анатомия
- •Методика
- •Мониторинг и подготовка
- •Положение пациента и ориентиры
- •Выполнение процедуры
- •Околосрединный подход
- •Подход по средней линии
- •Контроль проникновения в эпидуральное пространство
- •Потеря сопротивления
- •«Висящая капля»
- •Ощущение прокола желтой связки
- •Легкость введения катетера
- •Физиологические реакции
- •Выбор анальгетиков и их дозировка
- •Влияние эпидуральной аналгезии локальными анестетиками в грудном отделе на сердечно-сосудистую систему Снижение артериального давления
- •Ориентировочные дозы препаратов при торакальной эпидуральной аналгезии
- •Сегментарное распределение симпатической иннервации в грудопоясничном отделе
- •Потребность миокарда в кислороде
- •Применение в клинике
- •Осложнения Прокол твердой мозговой оболочки
- •Прокол вены
- •Парестезия
- •Задержка мочи
- •Тошнота
- •Седация
- •Гипотензия
- •Противопоказания Инфекция
- •Снижение сердечного резерва
- •Заключение
- •Список литературы
- •Система свертывания крови и ее физиологическая оценка
- •Эпидуральная гематома
- •Клинические признаки и патофизиология
- •Эпидуральная гематома после субарахноидальной пункции
- •Эпидуральная гематома после эпидуральной анестезии
- •Клинические сообщения, демонстрирующие безопасность региональной анестезии у больных, применявших антикоагулянты
- •Региональная анестезия/аналгезия у больного в состоянии антикоагуляции: ориентиры для критического решительного анализа
- •Спинальное введение опиоидов перед кардиопульмональным шунтированием
- •Предоперационная оценка
- •Подкожное введение гепарина («мини-дозы»)
- •Нестероидные противовоспалительные препараты
- •Ведение больного в операционном и послеоперационном периодах
- •Сроки сохранения факторов свертывания в плазме
- •Послеоперационный мониторинг
- •Заключение
- •Список литературы
- •Историческая справка
- •Механизм действия
- •Технические аспекты
- •Продолжительность импульса
- •Постоянный поток или постоянный вольтаж
- •Форма волн
- •Частотность
- •Амплитуда
- •Установка электродов и множественные каналы стимуляции
- •Электроды
- •Сроки стимуляции
- •Побочное действие
- •Противопоказания
- •Эффективность чэсн в послеоперационном периоде: обзор литературы Методологические аспекты
- •Абдоминальная хирургия
- •Предварительные клинические исследования по чэсн
- •Ортопедические операции
- •Акушерские операции
- •Операции на сердце и на органах грудной клетки
- •Состояние после ампутации
- •Ориентировочные показания по использованию чэсн в послеоперационном периоде
- •Пациенты, у которых ожидается улучшение от чэсн
- •Рекомендуемая установка электродов и параметры стимулирования при проведении чэсн
- •Заключение
- •Список литературы
- •Психосоциальный контекст послеоперационной боли
- •Анальгетические вмешательства нехимиотерапевтического характера
- •Обучение
- •Введение в транс
- •Погружение в транс
- •Гипнотическая работа
- •Завершение
- •Релаксационная реакция
- •Достижение релаксационной реакции
- •Заключение
- •Список литературы
- •Предоперационные факторы и подготовка
- •Оценка степени выраженности боли Боль у ребенка, не умеющего говорить
- •Оценка степени боли
- •Терапевтические возможности преодоления послеоперационной боли в педиатрии
- •Системные анальгетики Анальгетики неопиоидного типа
- •Послеоперационные режимы назначения морфина методом акп
- •Опиоиды
- •Режимы дозировок в педиатрии при региональной анестезии/аналгезии
- •Пути введения Энтеральная аналгезия
- •Внутримышечное введение
- •Интермиттирующее внутривенное введение опиоидов
- •Продолжительное внутривенное введение опиоидов
- •Аналгезия, контролируемая пациентом (акп)
- •Региональная анестезия/аналгезия
- •Каудальный блок
- •Эпидуральная аналгезия в поясничном и грудном отделах
- •Блокада подвздошно-пахового и подвздошно-подчревного нервов
- •Блокада дорсального нерва полового члена
- •Блокада бедренного и бокового кожного нервов бедра
- •Блокада отсека подвздошной фасции
- •Внутриплевральная региональная аналгезия
- •Инфильтрационная аналгезия операционной раны
- •Заключение
- •Список литературы
- •Послеродовое разрешение физиологической адаптации периода беременности
- •Физиологическая адаптация во время беременности
- •Анальгетические возможности Внутримышечное введение опиоидов
- •Внутривенное введение опиоидов
- •Эпидуральное введение опиоидов
- •Режимы дозировки эпидурально и суб-арахноидально вводимых опиоидов для аналгезии после кесарева сечения
- •Меперидин
- •Фентанил
- •Суфентанил
- •Буторфанол
- •Бупренорфин
- •Сочетанное применение препаратов
- •Субарахноидальное введение опиоидов
- •Фентанил
- •Суфентанил
- •Эпидуральное введение клофелина
- •Аналгезия опиоидами и грудное вскармливание
- •Выбор аналгезии после кесарева сечения
- •Список литературы
- •Аналгезия после некоторых ортопедических операций Артропластика и протезирование тазобедренного сустава
- •Влияние региональной анестезии на показатели смертности после операции артропластики тазобедренного сустава
- •Аналгезия, контролируемая пациентом (акп)
- •Субарахноидальное введение опиоидов
- •Эпидуральное введение опиоидов и локальных анестетиков
- •Субарахноидальное введение опиоидов при артропластике и протезировании коленного и тазобедренного суставов
- •Операции со вскрытием коленного сустава
- •Общее назначение опиоидов
- •Субарахноидальное введение опиоидов
- •Эпидуральное введение опиоидов
- •Эпидуральное введение локального анестетика
- •Комбинированная аналгезия
- •Невральная блокада поясничного сплетения
- •Клиническая практика госпиталя Brigham и женского госпиталя
- •Артроскопия коленного сустава Внутрисуставное введение бупивакаина
- •Внутрисуставное введение морфина
- •Артропластика плечевого сустава Аналгезия, контролируемая пациентом (акп)
- •Блокада плечевого сплетения
- •Эпидуральная анестезия/аналгезия в области шеи
- •Ампутация
- •Открытое вправление и внутренняя фиксация переломов лодыжки
- •Невральная блокада седалищного нерва в подколенной области
- •Заключение
- •Список литературы
- •Физиологические нарушения после операций на грудной полости
- •Причины нарушений функции дыхания после торакотомии
- •Методы аналгезии Парентеральное введение опиоидов
- •Межреберная невральная блокада
- •Внутриплевральная региональная аналгезия
- •Паравертебральная невральная блокада
- •Криоаналгезия
- •Чрескожная электростимуляция нерва
- •Субарахноидальное введение опиоидов
- •Эпидуралыюе введение локальных анестетиков и опиоидов Введение локальных анестетиков
- •Введение опиоидов
- •Установка эпидурального катетера в грудном или поясничном отделе
- •Комбинированное применение локальных анестетиков и опиоидов
- •Влияние на дыхание
- •Порядок ведения торакальной эпидуральной аналгезии после торакотомии
- •Порядок ведения торакальной эпидуральной аналгезии комбинацией локального анестетика и опиоида
- •Рекомендации по дозировке препаратов при торакальной эпидуральной аналгезии
- •Особые проблемы аналгезии после торакотомии
- •Заключение
- •Список литературы
- •Патофизиология послеоперационной абдоминальной боли
- •Кожная соматическая боль
- •Сенсибилизация ноцицепторов
- •Глубокая соматическая боль
- •Висцеральная боль Трансдукция
- •Трансмиссия
- •Иррадиирующая боль
- •Предполагаемые механизмы иррадиирующей боли
- •Последовательные рефлекторные реакции
- •Кортикальные реакции
- •Физиологические нарушения после операций на брюшной полости Нарушения функции легких
- •Осложнения со стороны желудочно-кишечного тракта
- •Тромбоэмболия
- •Аналгезия при некоторых вмешательствах на брюшной полости
- •Операции на верхнем отделе брюшной полости Нестероидные противовоспалительные препараты
- •Аналгезия, контролируемая пациентом
- •Межреберная невральная блокада
- •Внутриплевральная региональная аналгезия
- •Влияние внутриплевральной региональной аналгезии (впа) в сочетании с обычным введением опиоидов на обезболивание и на легочную функцию после операции холецистэктомии
- •Субарахноидальное введение опиоидов
- •Эпидуральное введение локальных анестетиков и опиоидов
- •Операции на нижнем отделе брюшной полости
- •Аппендэктомия
- •Операции на толстом кишечнике
- •Влияние эпидуральной анестезии/аналгезии на двигательную активность желудочно-кишечного тракта
- •Опорожнение желудка и подвижность тонкого кишечника
- •Моторика толстого кишечника
- •Заключение
- •Список литературы
- •Два мнения: аналгезия против диагностики
- •Физиологические нарушения, связанные с травмой
- •Возможности аналгезии Парентеральное назначение анальгетиков
- •Региональная анестезия/аналгезия
- •Подкожная инфильтрационная анестезия
- •Инфильтрационная анестезия
- •Фоновая блокада
- •Периферическая невральная блокада
- •Блокада сплетения
- •Внутриплевральная региональная аналгезия
- •Эпидуральная аналгезия
- •Субарахноидальная аналгезия
- •Травмы головы
- •Травмы грудной клетки
- •Повреждения скелета
- •Заключение
- •Список литературы
- •Коммуникация
- •Врачебный вклад
- •Концепция «глобального гонорара»
- •Администрация Департамент управления
- •Администрация госпиталей
- •Приобретение оборудования
- •Маркетинг
- •Заключение
- •Список литературы
- •Формирование эффективно работающих бригад по устранению боли: общий и женский госпиталь brigham
- •Группа задач, связанных с акп
- •Распределение препаратов
- •Участие медицинских сестер в переориентировке целей
- •Объекты проведения целевых усилии
- •Альтернативные методы контроля боли
- •Поза, позиционная установка
- •Сон, релаксация
- •Тошнота, рвота
- •Устранение боли дополнительное руководство по аналгезии, контролируемой пациентом
- •Общая информация:
- •Критерии акп Предлагаемые критерии акп совместно с лечением
- •Аналгезия, контролируемая пациентом
- •Общие указания Обучение пациента/родственников
- •Сестринский департамент госпиталя Протокол анестезии, контролируемой пациентом Реабилитационное отделение
- •Сестринский департамент госпиталя Соображения в случаях неадекватности аналгезии
- •Сестринский департамент госпиталя Инструкция по титрованию и введению «спасительной» дозы при акп-плюс
- •Сестринский департамент госпиталя Инструкция по титрованию и по введению «спасительной» дозы при акп-плюс
- •Список литературы
- •Персональный фактор
- •Анестезиолог
- •Сестринская помощь
- •Фармакологическая служба
- •Приготовление некоторых растворов для эпидурального введения
- •Оборудование
- •Основные требования, предъявляемые к эпиду-ральным инфузионным системам
- •Простота и легкость в обращении
- •Ограничитель скорости потока
- •Четкость в идентификации прибора (обозначение)
- •Вход для инъекций
- •Безопасность
- •Портативность
- •Мониторы
- •Процедуры, проводимые службой острой боли
- •Документация
- •Рабочий документ службы по борьбе с острой болью Служба лечения боли bwh отделение анестезиологии
- •Типичный лист стандартных назначений для пациента, получающего акп Общий и женский госпиталь Brigham Учебный филиал медицинского университета Гарварда
- •Проблемы, стоящие перед службой острой боли
- •Проблемы, стоящие перед соб
- •Список литературы
- •Молекулярная фармакология
- •Нейроэндокринная система
- •Сердечно-сосудистая система
- •Дыхательная система
- •Пищеварительная система
- •Центральная нервная система
- •Механизм аналгезии
- •Клинические исследования аналгезии Общее назначение
- •Эпидуральное назначение
- •Субарахноидальное введение
- •Заключение
- •Список литературы
- •Послеоперационная боль
- •101000, Москва, Петроверигский пер., 6/8
- •143200, Г. Можайск, ул. Мира, 93.
Кровоснабжение позвоночного канала Артерии
Кровоснабжение спинного мозга, его корешков и мозговых оболочек осуществляется передней спинномозговой артерией и двумя задними спинномозговыми артериями. Первая из указанных артерий спускается по передней срединной борозде на передней поверхности спинного мозга (рис. 5-9) и заканчивается артериолами на уровне терминальных волокон. Она образуется из разных источников. Верхняя часть передней спинномозговой артерии формируется при слиянии конечных ветвей позвоночных артерий и анастомозов от ветвей щитовидно-шейной и реберно-шейной артерий. Эта система обеспечивает артериальное кровоснабжение спинного мозга до уровня TIV. Передняя спинномозговая артерия среднегрудного отдела образуется межреберными артериями, отходящими от аорты на уровне TIV-TIX. Нижележащие участки спинного мозга питаются единственным сосудом (a. radicularis magna, артерия Адамкевича). Эта артерия отходит от аорты на участке от TIX до LII. Передняя спинномозговая артерия обеспечивает кровью всю переднюю часть спинного мозга или почти 2/3 его объема (см. рис. 5-9).
Задние спинномозговые артерии отходят от задних нижних ветвей мозжечковых артерий и опускаются по задней поверхности спинного мозга. Эти артерии располагаются чуть медиальное соответствующих задних корешков, они обеспечивают артериальной кровью 1/3 объема спинного мозга. Весьма значительные анатомические вариации в прохождении передней спинномозговой артерии имеют большое клиническое значение. Между отдельными участками спинного мозга не всегда имеются достаточные анастомозы, поэтому в определенных зонах спинного мозга, снабжаемой единственной артерией (артерия Адамкевича), может развиться ишемия. Сегментарные артерии обеспечивают спинной мозг с обеих сторон, тем не менее в терминальных зонах может присутствовать всего одна концевая артерия с какой-либо из сторон. Нарушение кровотока в ней ведет к ишемии и к развитию синдрома передней спинномозговой артерии, характеризующегося ослаблением двигательной способности при сохранении чувствительности.
Игла, введенная в эпидуральное пространство косым доступом при проколе желтой связки, может травмировать область дуральной манжетки, где в позвоночный канал входят «питающие» ветви спинномозговых артерий. Они могут быть повреждены при выполнении спинальной анестезии/аналгезии. Однако современные достижения техники эпидуральной анестезии сводят к минимуму число осложнений типа синдрома передней спинномозговой артерии.
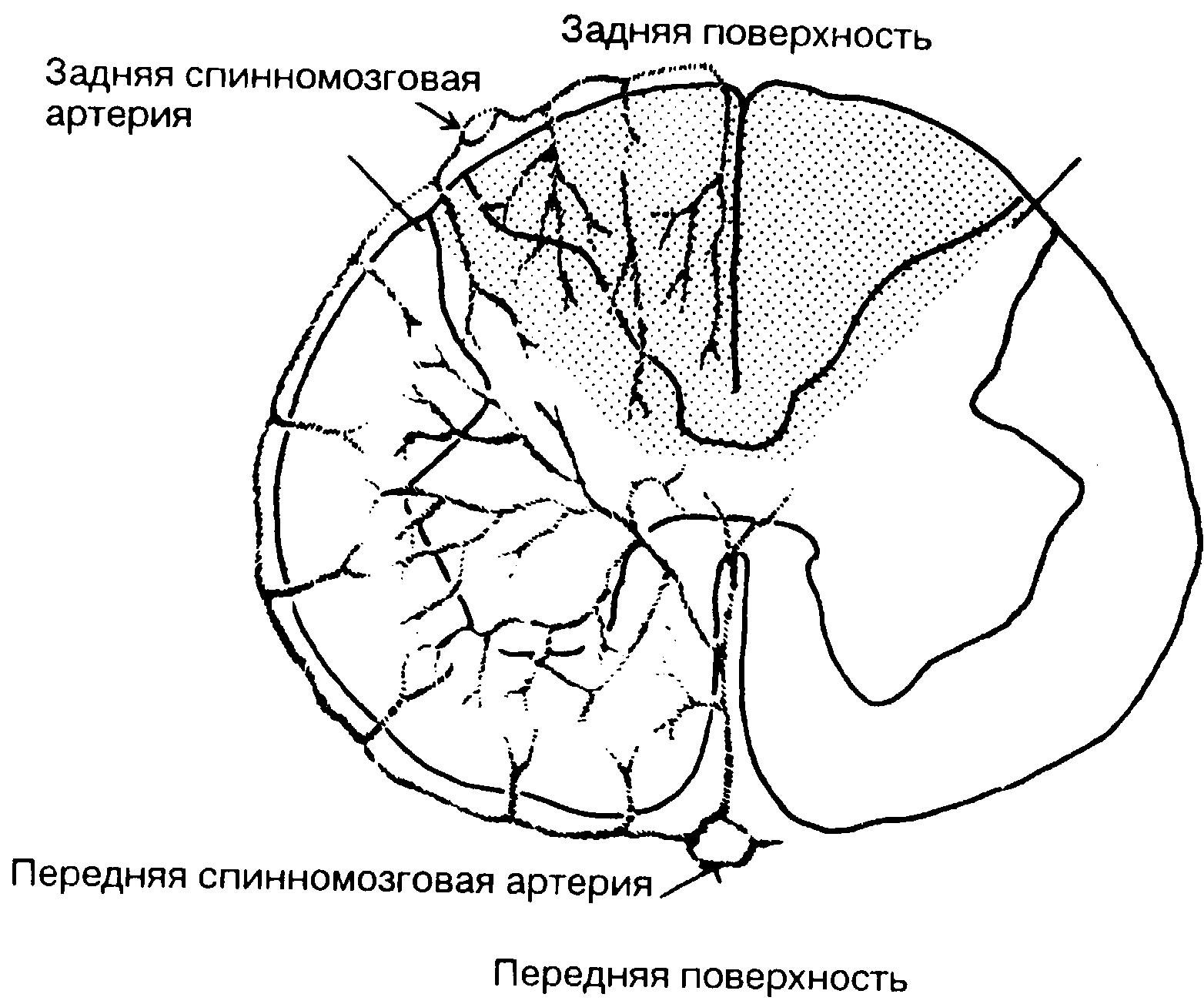
Рис. 5-9. Артериальное обеспечение спинного мозга.
Передняя спинномозговая артерия снабжает передние 2/3 спинного мозга. Ишемия в системе этой артерии вызывает двигательные нарушения.
Вены
Сложная система эпидуральных венозных сплетений окружает дуральный мешок на всем его протяжении в позвоночном канале. Через венозные сплетения дренируется кровь от спинного мозга, от структур позвоночного канала и в небольшом количестве отводится ЦСЖ, поступающая через арахноидальные грануляции. В верхнем отделе эпидуральные венозные сплетения соединяются с мозговыми венозными синусами. Кровь от самого спинного мозга оттекает через систему непарной и полунепарной вен. В нижних отделах кровь из эпидуральных венозных сплетений попадает в систему нижней полой вены через крестцовые и тазовые венозные сплетения.
Список литературы
1. Covino ВС. Scott DB: Handbook of Epidural Anaesthesia and Analgesia. Grune & Stratton, Orlando. FL, 1985
2. Kutz J, Renck H: Handbook ofThoraco-abdominal Nerve Block. Grune & Siratton, Orlando, FL, 1987
3. Scott DB: Techniques of Regional Anaesthesia. Appleton & Lange/Mediglobc, Norwalk, CT, 1989
Клиническое измерение боли
Роберт H. Джеймисон (Robert N. Jamison)
Характеристика боли и ее измерение привлекают все большее внимание. Боль остается субъективным ощущением, тем не менее ее количественная оценка приобретает возрастающее значение. Первоначально попытки измерить боль фокусировались только на колебаниях ее интенсивности. Как известно, ощущение боли у человека отражает сложный комплекс физиологических и патофизиологических процессов, конечным результатом которых и являются качественные особенности боли.
К сожалению, проблема измерения боли все еще находится в зародышевом состоянии, отсутствует даже единая теоретическая база для этого. В общем существуют две основные модели возникновения боли:
1) медицинская модель, по которой боль рассматривается как патология или следствие повреждения;
2) поведенческая модель, по которой боль представляет собой ощущение, регулируемое сознанием, поведением и персональными предрасполагающими факторами.
Первая из этих моделей более традиционна и основана на объективных данных патологии. Поведенческая модель ориентирована на субъективные факторы, например на предшествующий опыт и воспитание. Эти фундаментальные различия характеризуют некоторые из типичных затруднений, возникающих при попытках точно оценить боль.
Важно остановиться на некоторых трудностях, присущих измерению боли. Так как боль - это субъективное ощущение, каждый человек воспринимает ее по-своему. В количественной оценке боли обнаружены непреодолимые индивидуальные различия. Например, одни пациенты никогда не оценят свои боли в 10 баллов (по шкале от 0 до 10), пока они не достигнут такой степени, что больные почти начнут терять сознание. Другие пациенты, наоборот, оценивают боль в 10 баллов, хотя при этом остаются спокойными и расслабленными. Следовательно, все цифровые системы оценки боли имеют пределы надежности. Если пациент характеризует боль как «10-балльную», то говорить о дальнейшем нарастании боли уже нельзя.
Сравнивать болевые ощущения очень сложно из-за большого числа индивидуальных различий. Больные по-разному сообщают о локализации, характере и продолжительности своих болей. Кроме того, само восприятие боли в данный момент зависит от предшествующего опыта больного в этом отношении. На индивидуальное восприятие боли влияют демографические факторы, пол, возраст, этнические особенности. Сведения, сообщаемые пациентом о своих болях, изменяются в зависимости от проводимого лечения, от нарушений сна и от аффектации. Так, в состоянии депрессии и возбуждения пациенты склонны преувеличивать свои боли.
Все эти факторы проливают свет на трудности, свойственные оценке интенсивности болей у человека. Однако, несмотря на эти ограничения, разработано и применяется много методов клинической оценки боли. В данной главе приведен обзор мекоторых из них, кратко описаны их преимущества и недостатки.
САМООЦЕНКА ВЫРАЖЕННОСТИ БОЛИ
Самым обычным методом количественной характеристики боли является ее оценка самим пациентом. Он может использовать множество слов и определений, чтобы описать интенсивность своих болей. Некоторые системы учета основаны на фиксации различных признаков боли, но большинство принимают во внимание лишь один из них.
Наиболее простой способ характеризовать боль - это спросить пациента, имеются ли у него боли (да/нет). Этот действительно простейший метод не дает представления о интенсивности боли. Одна из первых схем систематизации боли была предложена Melzack и Torgerson [1]. В ней предусматривалось пять разных определений степени болевых ощущений - от «легкой» до «мучительной». Однако эту шкалу критиковали, так как она недостаточно отражала ощущения больного. Некоторые из методов измерения боли были признаны более реальными и значимыми по сравнению с другими.
Цифровая рейтинговая (оценочная) шкала
Цифровая рейтинговая шкала используется для определения интенсивности боли. Впервые применили ее Budzynski и сотр. [2] и Melzack [3]. Пациентам предлагали оценить свои болевые ощущения цифрами от 0 (нет болей) до величины максимальной ее интенсивности (до 10 или 100). Эта методика позволяла оценивать динамику болевых ощущений, была проста в употреблении и более демонстративна, чем другие способы измерения боли [4]. Пациенты легко обучались применению этой схемы, особенно когда цифровые обозначения связывались с определенной интенсивностью болей. Шкала быстро усваивалась, была наглядной и удобной в заполнении. Из разных в цифровом масштабе значений шкалы наиболее распространенной стала шкала из 11 пунктов (от 0 до 10). Можно рекомендовать также более детальную шкалу с большим числом цифр, позволяющую подробнее характеризовать вариабильность болевых ощущений.
Некоторые клиницисты предлагали своим пациентам оценивать боли ежечасно все время лечения. Подобная периодическая оценка обеспечивает информацию о динамике боли, что не удается получить при однократном определении ее интенсивности. Сопоставляя предыдущие и последующие показатели болевых ощущений, можно судить об эффективности проводимого лечения. Однако частые измерения требуют сотрудничества со стороны пациента, что иногда становится серьезной проблемой. Более того, настороженность больного в отношении восприятия боли, сопряженная с ее мониторингом, может привести к усилению раздражительности, ощущению недостатка внимания, чувству заброшенности, беспомощности [5]. Это особенно нежелательно, если боли постоянные или даже усиливающиеся. Следовательно, частые измерения боли могут привести к неточности в ее оценке и к преувеличению болевых ощущений.
Несмотря на указанные недостатки, цифровая система оценки боли часто довольно успешно используется в клинических условиях. Возможно, она является наиболее доступным методом при обслуживании большого числа пациентов, страдающих от болей в послеоперационном периоде.
Было высказано предположение, что пациенты, проводящие мониторинг собственных болевых ощущений, могут испытывать чувство усиливающегося контроля [7]. Уже сам по себе факт мониторинга они воспринимают как активное вмешательство [8]. Однако последние исследования подтвердили, что ежечасный контроль интенсивности болей потенциально полезен в клинике [5]. Пациенты, не справлявшиеся с продолжительной оценкой своих болей, обычно были склонны к эмоциональным нарушениям. Это обстоятельство удавалось объяснить, выдвинув предположение, что пациенты, предварительно настроенные на контроль за своими болями, чувствуют себя более защищенными. В то же время больные, не справляющиеся с регистрацией болей, либо же пациенты со стабильно удерживающимися болями, не проходящими при лечении, чувствуют себя заброшенными. Выдвинуто предположение, что эти ощущения усиливают состояние возбуждения. Последнее само по себе способно усилить перцепцию боли.
Визуальная аналоговая шкала
Визуальная аналоговая шкала (ВАШ) - это прямая линия длиной 10 см, концы которой соответствуют крайним степеням интенсивности боли («нет боли» на одном конце, «мучительная нестерпимая боль» - на другом) (рис. 6-1). Линия может быть как горизонтальной, так и вертикальной [9]. Пациенту предлагают сделать на этой линии отметку, соответствующую интенсивности испытываемых им в данный момент болей. Расстояние между концом линии («нет болей») и сделанной больным отметкой измеряют в сантиметрах и округляют. Помощь в оценке боли могут оказать пояснения, вписанные вдоль линии (например, «слабые, умеренные, тяжелые»). Различные вариации ВАШ называют графической рейтинговой шкалой [10]. Пациенты склонны группировать свои ответы в местах подобных подписей, поэтому графическая рейтинговая шкала считается менее точной.
Перед тем как пациент начнет пользоваться ВАШ (или любой другой оценочной шкалой), врач или производящий исследование должен все подробно объяснить пациенту.

Рис. 6-1. Визуальная аналоговая шкала, используемая для измерения интенсивности боли.
Применение ВАШ имеет следующие преимущества:
1) метод позволяет определить действительную интенсивность болей (проведенные исследования выявили хорошую корреляцию между данными ВАШ и другими методами измерения силы болей) [11];
2) большинство пациентов, даже дети (в возрасте 5 лет и старше) легко усваивают и правильно используют ВАШ [12];
3) использование ВАШ позволяет изучить распределение рейтинга [13];
4) результаты исследований воспроизводимы во времени [9];
5) более адекватная оценка эффекта лечения по сравнению со словесной характеристикой боли [14].
ВАШ успешно использовали во многих исследованиях при изучении эффективности терапии.
Однако ВАШ имеет и определенные недостатки по сравнению с другими методиками. Во-первых, пациенты могут весьма произвольно ставить отметки на шкале. Часто подобные отметки не отражают действительности и не соответствуют устным оценкам болей, даваемым самими больными. Во-вторых, расстояние до сделанной отметки должно быть измерено, что требует времени и точности, возможны также ошибки при измерении. В-третьих, ВАШ трудно объяснить пожилым пациентам, не улавливающим связи между линией и положением своей отметки на ней [15]. Наконец, фотокопирование иногда приводит к искажению линии, что отражается на измерении. Поэтому ВАШ не считают оптимальным методом измерения интенсивности боли у взрослых и у пожилых больных, но рекомендуют как успешный у детей [10].
Словесная рейтинговая шкала
Словесная рейтинговая шкала представляет собой другой способ оценки вариантов и интенсивности болей. Эта шкала выглядит как список слов, из которых пациент выбирает наиболее точно отражающие его боль («жгучие, режущие, судорожные боли»). Пациенты также обычно используют многообразные описания при объяснении степени дискомфорта. Поэтому словесная рейтинговая шкала одинаково нужна как работникам медицинских учреждений, так и пациентам.
Словесная рейтинговая шкала, как и линейная цифровая шкала, облегчает оценку степени боли. В литературе описаны разные типы словесной рейтинговой шкалы, в том числе состоящие из 4 пунктов [16, 17], 5 [18, 19], 6 [3], 12 [20] и даже из 15 пунктов [21]. Слова обычно выстраивают в ряды по степени нарастания тяжести боли и последовательно нумеруют от меньшей тяжести к большей (рис. 6-2).
Использование словесной рейтинговой шкалы имеет ряд преимуществ. Ее легко применять, просто ставить отметки, она адекватно отражает состояние пациента и эффективность проводимой терапии. Данные словесной шкалы хорошо совмещаются с результатами других измерений интенсивности боли, но слабо отражают персональные факторы, влияющие на боль [22]. Эта шкала хорошо отражает имеющиеся изменения. Клинические исследования продемонстрировали четкие сдвиги в чувствительности и в аффективном рейтинге боли после нейрохирургических вмешательств и/или медикаментозного лечения [23, 24].
Аа. |
Аб. |
Ав. |
1. Нет болей |
1. Нет болей |
1. Нет болей |
2. Слабые |
2. Слабые |
2. Слабые |
3. Умеренные |
3. Умеренные |
3. Дискомфорт |
4. Тяжелые |
4.Тяжелые |
4. Мучительные |
|
5. Очень тяжелые |
5. Ужасные |
|
|
6. Непереносимые |
Б. |
В. |
1. Незаметные |
1. Нет болей |
2. Едва заметные |
2. Крайне слабые |
3. Очень слабые |
3. Едва заметные |
4. Слабые |
4. Очень слабые |
5. Легкие |
5. Слабые |
6. Умеренные |
6. Легкие |
7. Сильные |
7. Умеренные |
8. Интенсивные |
8. Беспокоящие |
9. Очень сильные |
9. Сильные |
10. Тяжелые |
10. Интенсивные |
11. Очень интенсивные |
11. Очень сильные |
12. Непереносимые |
12. Крайне интенсивные |
|
13. Особо интенсивные |
|
14. Непереносимые |
|
15. Мучительные |
Рис. 6-2. Примеры словесных рейтинговых шкал, применяемых для оценки интенсивности боли.
Боль остается индивидуальным ощущением, поэтому именно словесный рейтинг лучше всего отражает многообразную природу боли. В настоящее время словесная рейтинговая шкала является наиболее популярным методом измерения болевых ощущений.
К сожалению, у словесной рейтинговой шкалы имеются и недостатки. Чаще всего она спланирована в расчете на нарастание силы боли. Подобная аранжировка объясняется тем, что шкала вырабатывалась на лицах, подвергавшихся болевым воздействиям в условиях эксперимента, а не на пациентах со спонтанно возникающими болями. Между тем распределение боли по степени тяжести при остром их возникновении и при хроническом персистировании различно. Для преодоления подобного затруднения исследователи предлагали пациентам самим составить подробный ряд обозначений выраженности боли. Такой прием известен как перекрестно-модальный подход [10]. Этот метод позволяет индивидуализировать болевую характеристику, но требует значительного времени. Кроме того, при таком подходе не соблюдаются равные интервалы между соседними характеристиками силы болей, что снижает точность подобной шкалы [25].
Другая трудность при работе со словесной шкалой заключается в особой ее подверженности небольшим колебаниям чувствительности и в тенденции больных изменять показания под влиянием аффекта. Исследования показали, что сенсорные, аффективные и оценочные описания боли в значительной степени зависят от степени возбуждения пациента [26].
Сам диагноз заболевания может оказать влияние на показатели словесной шкалы. Например, пациенты со злокачественными процессами склонны уменьшать свои болевые ощущения и делать более эмоциональные записи по сравнению с пациентами, страдающими от болей иного происхождения [27]. Остаются спорные положения относительно правильной формулировки болей, соответствующих диагнозу заболевания. Fordyce [28] и др. предполагали, что словесная формулировка боли зависит от многих факторов, а не только от основной патологии. Пациенты с хроническими болями используют более одного слова для описания своих болевых ощущений (в том числе «жгучие, ноющие, пульсирующие, стреляющие») (табл. 6-1). Этот признак указывает на более выраженные эмоциональные сдвиги и вероятность безуспешного лечения [29].
Таблица 6-1. Список словесных характеристик боли
1. Пронизывающие (острые) |
8. Жалящие |
2. Колющие |
9. Сдавливающие |
3. Стреляющие |
10. Онемение |
4. Жгучие |
11. Зудящие |
5. Ноющие |
12. Покалывание |
6. Схваткообразные |
13. Отсутствие болей |
7. Пульсирующие |
|
В настоящее время нет оснований считать, что ВАШ более чувствительна и лучше отражает лечебный эффект, чем словесная рейтинговая шкала [30]. Оба метода приемлемы для количественной характеристики болей в условиях клиники.
Болевая анкета McGill
Melzack и Torgerson [1] распределили слова, описывающие качественные особенности боли, на три основных класса: сенсорные, аффективные и оценивающие слова. Из этого списка McGill и составил свою болевую анкету. Она состоит из 20 подклассов, оценивающих интенсивность боли по шкале от 0 («нет боли») до 5 («мучительные боли»). Анкета предусматривает три типа измерений:
1) индекс интенсивности боли;
2) число выбранных слов;
3) общую интенсивность по шкале боли.
Анкета достаточно объективно отражает степень и истинный характер субъективных болей [31]. Сокращенные варианты анкеты опубликованы [32]. Кроме того, с ее помощью можно измерять различные аспекты болевых ощущений, изменения в результате проведенного лечения и облегчать дифференциальную диагностику.
Существуют определенные ограничения в пользовании болевой анкетой McGill. Во-первых, в анкете есть термины, понятные не всем больным (например, дергающие, скребущие). Поэтому некоторым пациентам приходится объяснять значение подобных слов. Во-вторых, три приведенные в анкете шкалы в значительной степени коррелируют между собой. Поэтому одно и то же измерение может попадать в разные разделы шкалы [33]. Наконец, могут возникать сомнения по поводу стабильности и содержания подклассов [10]. Несмотря на эти ограничения, болевая анкета используется в клинических исследованиях уже многие годы и представляет собой вполне подходящий метод субъективного измерения интенсивности боли.
Схема распределения боли по дерматомам
Схема распределения боли относится к популярным методам ее оценки. Пациенту предлагают указать локализацию и распределение его болевых ощущений на схеме дерматомов. Схема обычно представляет собой условное обозначение контуров человеческого тела спереди и сзади. На некоторых схемах приводится также и косое положение. Пациент должен заштриховать на данной ему карте области, соответствующие локализации болей. Некоторые клиницисты используют разные цвета, чтобы отобразить оттенки чувствительности (красный - боль, синий - онемение).
Опубликовано множество методов, основанных на подобных отметках. Margolis и сотр. [34] разделили карту дерматомов на 45 отдельных областей (рис. 6-3). С помощью прозрачного пластмассового шаблона можно было оценивать каждую схему, обозначая отдельные заштрихованные зоны, где пациент ощущает боли как «1», незаштрихованные - как «0». Полученная сумма означала число пораженных зон. Toomey и сотр. [35] выделили на карте дерматомов 32 области и пользовались ана логичным методом оценки. Эффективность подобной методики подтверждена многочисленными наблюдениями [34, 36, 37].
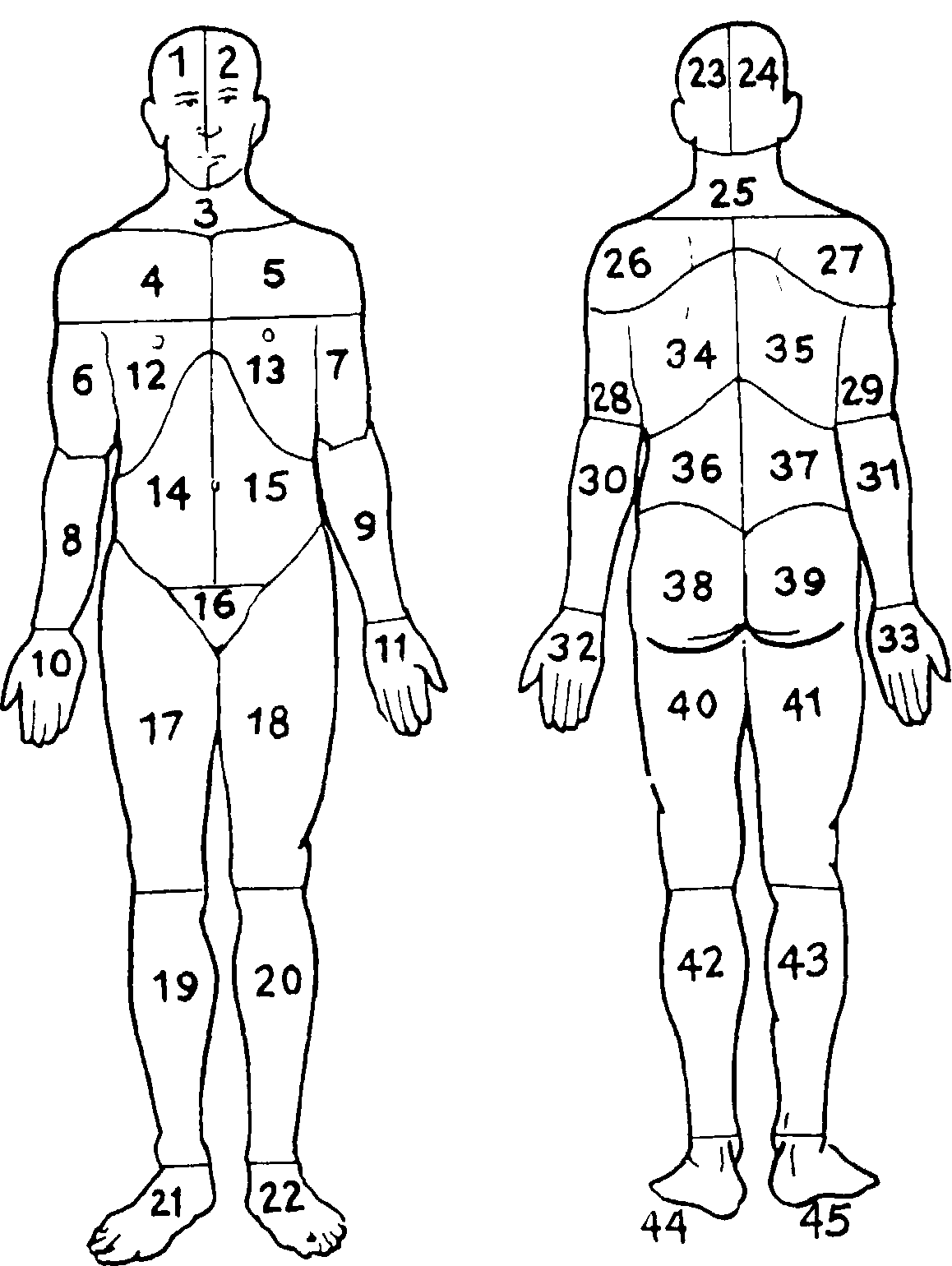
Рис. 6-3. Изображение дерматомов (локализация боли).
Разрабатывались и другие оценочные схемы, где основное внимание уделялось обычному или аномальному распределению болей. Выделены следующие критерии:
1) несоответствие схематического изображения словесному описанию болей;
2) распространение или преувеличение зоны болей;
3) эмоциональное преувеличение (например, длительные записи, обширные описания);
4) заштрихованные участки быстро меняют свои очертания и расположение.
Margolis [38] отметил, что при поражениях опорно-двигательного аппарата больные часто изображают на схеме парестезию, не укладывающуюся в анатомические рамки. Он отвергал мнение, что схема, не укладывающаяся в строгие анатомические рамки, может представлять собой так называемое функциональное перекрытие. По данным других исследователей, имеется весьма слабая корреляция между аномальными схемами отображения боли и психопатологией [39].
Болевые схемы просты, удобны в работе, их легко оценивать. Они могут быть полезны, в частности, при диагностике некоторых заболеваний, сопровождающихся болями, а также при выборе места операционного разреза.
Применение болевых схем имеет определенные ограничения:
1) больные могут искажать и фальсифицировать схемы;
2) некоторым пациентам приходится давать детальные разъяснения;
3) пожилые больные испытывают затруднения при рассматривании схем, при их точной заштриховке и при описании своих болей;
4) графическое отображение болей зависит от состояния пациента и от длительности заболевания.
Эти схемы никогда не следует применять для оценки психического статуса пациента, а только как составную часть описательной оценки болевых ощущений.
