
- •Оснащение химической лаборатории
- •Химические реактивы
- •Химическая посуда
- •Лабораторное оборудование
- •2. Основные приемы и методы работы
- •2.1. Измельчение и перемешивание
- •2.2. Нагревание и охлаждение
- •2.3. Фильтрование и центрифугирование
- •2.4. Высушивание
- •2.5. Концентрирование растворов
- •3. Разделение и очистка веществ
- •3.1. Кристаллизация
- •3.2. Экстракция
- •3.3. Перегонка
- •4. Экспериментальные работы по разделению, очистке органических веществ
- •4.1. Определение температуры плавления кристаллических органических соединений
- •4.2. Разделение смеси веществ методом перегонки
- •4.3. Возгонка (сублимация)
- •4.4. Очистка органического вещества перекристаллизацией.
- •5. Экспериментальные работы по получению некоторых органических соединений
- •5.1. Оформление отчета по синтезу органических соединений
- •Образец записи в рабочем журнале
- •Синтез бензойной кислоты
- •5.3. Синтез бензимидазола
- •5.4. Синтез метилоранжа
- •5.5. Синтез сульфаниловой кислоты
- •5.6. Синтез уксусноэтилового эфира
- •5.7. Синтез изобутилацетата
- •5.8. Синтез уксусноизоамилового эфира
- •5.9. Синтез хинизарина
- •5.10. Синтез n- нитрозофенола
- •5.11. Синтез n - толуолсульфокислоты
- •5.12. Синтез 3-нитрофталевой кислоты
- •5.13. Синтез хромового желтого к
- •5.14. Фенолфталеина
- •5.15. Синтез этилбромида
- •5.16. Синтез 2- бромпропана
- •5.17. Бутилацетат
- •Контрольные вопросы
Образец записи в рабочем журнале
Дата………………………………….Работа №……..
Получение бромистого этила
Основные реакции:
KBr + H2SO4 → KHSO4 + HBr
C2H5OH
+ HBr![]() C2H5Br
+ H2O
C2H5Br
+ H2O
CH3-CH2-OH + HO-SO2-OH CH3-CH2-O-SO2-OH + H2O
CH3-CH2-O-SO2-OH + HBr → CH3-CH2- Br + H2SO4
Побочные реакции:
2HBr + H2SO4 → Br2 + 2 H2O + SO2
CH3-CH2-O-SO2-OH + CH3-CH2-OH → H2SO4 + CH3-CH2-O-CH2-CH3
3. Таблица
Вещество |
Мr |
Тпл, ºС |
Ткип, ºС |
Плотность, d204 |
n20D |
Растворимость |
Примечания |
Этиловый спирт, 95% |
46,07 |
-114,5 |
78,4 |
0,8042 |
1,3614 |
Смешивается с водой, эфиром и др. органическими растворителями |
Пары образуют с воздухом взрывропасные смеси |
Бромистый калий |
119,02 |
730 |
1380 |
2,75 |
- |
Растворяется в воде, глицерине |
- |
Серная кислота, 95,6% |
98,08 |
10,49 (100%-ная) |
338 (частично разлагается) |
1,84 |
- |
Смешивается с водой |
Обугливает орган. вещества, Следует приливать порциями кислоту в воду, но не наоборот |
Бромистый этил |
109 |
-119 |
38,3 |
1,4586 |
1,4211 |
В 100 мл воды при 20 ºС растворяется 0,9 г |
|
Пересчет количеств веществ, необходимых для синтеза:
а) по руководству требуется взять:
Этиловый спирт, 95 %-ный, мл (моль)……………..40 (0,7)
Бромистый калий, г (моль)………………………….30 (0,25)
Серная кислота (d=1,84), мл (моль)………………...33 (0,6)
б) следует взять реактивов из расчета на 0,1 моль бромистого калия:
Этиловый спирт, 95 %-ный, мл ……………………..16
Бромистый калий, г ……..……………………………11,9
Серная кислота (d=1,84), мл …………………………13
Теоретический выход бромистого этила 10,9 г.
Главные этапы синтеза:
а) приготовление реакционной смеси и отгонка бромистого этила;
б) отделение бромистого этила от воды;
в) очистка бромистого этила: удаление этилового эфира и перегонка бромистого этила.
Схемы приборов:
Схема прибора 1 Схема прибора 2
описание хода синтеза (описание операций, наблюдения, объяснения).
выход чистого бромистого этила:
а) 8,7 г; б) 80 % от теоретического количества;
Дата окончания работы………………..
Отзыв и подпись преподавателя…………
Синтез бензойной кислоты
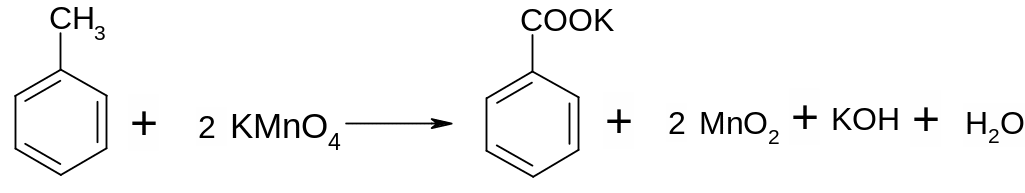

Необходимые реактивы и посуда:
Толуол 3 г
Перманганат калия 10,2 г
Соляная кислота
Круглодонная колба на 250 мл
Водяной холодильник
Стакан
Отсос
Ход работы:
В круглодонной колбе, снабженной обратным холодильником, кипятят в течение 2-3 часов на песчаной бане 3 г толуола и 10,2 г мелкорастертого перманганата калия в 60-80 мл воды. Для равномерного кипения смеси в колбу бросают несколько кусочков пористого кирпича. После окончания реакции реакционную массу охлаждают, выпавшую двуокись марганца отфильтровывают и промывают теплой водой (5 мл)*. Фильтрат подкисляют концентрированной соляной кислотой до кислой реакции по Конго. При этом осаждается бензойная кислота. Осадок отфильтровывают, растворяют в небольшом количестве кипящей воды и медленно охлаждают. Образовавшиеся кристаллы отсасывают на микроотсосе, высушивают между листами фильтровальной бумаги и определяют температуру плавления (120-121 ºС).
* Если реакционная смесь остается окрашенной, обесцвечивания достигают прибавлением 1-1,5 мл спирта или 0,2 г щавелевой кислоты при нагревании. Выпавший при этом осадок вновь отфильтровывают.
