
- •Термодинамиканың негізгі түсініктері мен анықтамалары.
- •Термодинамиканың бірінші заңы, оның анықтамалары мен аналитикалық өрнектері.
- •Гесс заңы , оның термодинамикалық негізделуі.
- •Ішкі энергия және энтальпия, олардың өзара байланысы.
- •9. Әр түрлі температурада химиялық процестің және фазалық ауысулардың жылу эффектілерін есептеу жолдады.
- •10. Идеал газдар қатысымен өтетін әр түрлі процестер үшін термодинамиканың бірінші заңы.
- •11)Термод-ң 2ші заңы.Оның анықтамалары ж/е матем-қ өрнектері. Қайтымды ж/е қайтымсыз процестердің энтропиясының өзгерісі.
- •13) Тұрақты қысым кезде процес жылуының темп-ға тәуелділігін қарастырамыз.
- •14. Әр түрлі температурада химиялық процестің және фазалық ауысулардың жылу эффектілерін есептеу жолдады.
- •15. Идеал газдар қатысымен өтетін әр түрлі процестер үшін термодинамиканың бірінші заңы.
- •20.Қайтымды ж/е қайтымсыз процестердің энтропиясының өзгерісі.
- •21.Энтропияны процесс бағытының критериі (белгісі) ретінде қолдану.
- •23) Идеал газдар қатысымен өтетін әр түрлі процестер энтропиясының өзгерісін есептеу жолдары.
- •24) Заттың абсолютті энтропиясының температураға тәуелділігі.
Термодинамиканың негізгі түсініктері мен анықтамалары.
Термодинамика – температура мен жылудың және жылу мен жұмыстың өзара байланысын зерттейтін ғылым. Термодинамикада зерттелінетін негізгі құбылыстар:
Энергияның бір денеден екінші денеге және бір түрден екінші түрге ауысуы.
Әртүрлі жағдайларда өтетін физикалық және химиялық процестердің энергиялық эффектілері.
Процестің өтуі не өтпеуі, олардың бағыты және шегі.
Термодинамика үшке бөлінеді- жалпы, техникалық және химиялық. Термодинамикада негізгі зерттелетін объект жүйе. Жүйе дегеніміз қоршаған ортаның ойша немесе щыншектермен шектелген бөлігі. Бұл бөлік бір немесе бірнеше денеден тұрады. Егер жүйені құратын денелер бір-бірімен не басқа денелермен энергия немесе зат алмасу арқылы әрекеттессе онда ол термодинамикалық жүйе болып саналады. Термодинамикалық жүйе 3 түрлі болады: ашық – қоршаған ортамен энергия да, зат та алмасу арқылы әрекеттеседі; жабық – қоршаған ортамен тек энергия алмасу арқылы әрекеттеседі; оқшау – қоршаған ортамен зат та, энергия да алмаспайды. Тағы да жүйе гомогенді және гетерогенді болып бөлінеді. Гомогенді жүйе – тек бір фазалы денелерден құралады. Гетерогенді жүйе – кемінде екі фазалы денелерден құралады.
Термодинамика макроскопиялық денелерді қарастырады, яғни кемінде 1020-1025 бөлшектерден тұратын денелер. Ал осы бөлшектер жылудың әсерінен ылғи қозғалыста болады. Термодинамика осы жылу қозғалысын температура арқылы өлшейді. Осыдан термодинамикадығы алғашқы тұжырым шығады: жылу тепе-теғдігінде барлық термодинамикалық денелерде температура бірдей болады. Бұны термодинамиканың нөлдік зағы деп те айтады.
Келесі ұғым Термодинамикалық тепе-теңдік. Жүйе өзіне тән қасиеттерімен, соған сәйкес күймен сипатталады. Егер жүйенің күйі өзгермей тұрақты болсатермодинамикалық тепе-теңдік орнаған болып саналады. Мұндай жағдайда жүйенің барлық бөліктерінде температура, қысым және концентрация бірдей болады.
Жүйенің
қасиеттері мен күйін сипаттайтын
шамаларды параметрлер дейміз. Олар
екіге бөлінеді: интенсивтік және
экстенсивтік. Процесс орындалып,
тепе-тіңдік орнағаннан кейін теңесетін
параметрлерді интенситік не потенциалдар
дейміз. Оларға қысым, температура,
кернеу, химиялық потенциал және т.б.
жатады. Ал тепе-теңдік орнағаннан кейін
қосылатын параметрлерді экстенсивтік
не координаттар дейміз. Оларға масса,
жылу сыйымдылық, заряд ж/е т.б. жатады.
Термодинамика энергияның сақталу
зағына негізделеді. Термодинамикада
қозғалыс энергиямен сипатталады. Ал
осы энергия әрдайым интенсивтік және
экстенсивтік параметрлердің
көбейтіндісімен анықталады. Мысалы
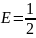 mv2
.
mv2
.
Термодинамиказаңдарын матиматикалық әдістермен өрнектеу үшін дифференциалдық теңдеулер мен дербес туындылар пайдаланылады. Себебі жүйе күйін сипаттайтын параметрлер айнымалышамалар болып саналатындықтан олар бір-бірімен функционалдық байланыста болады. Бұл байланысты дифференциалды қатынастар арқылы аламыз.
