
- •По характеру взаимодействия частиц дисперсной фазы между собой
- •По характеру взаимодействия между фазой и средой
- •Классификация состояния вещества по степени его дисперсности
- •Классификация дс по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •В зависимости от строения углеводородного радикала
- •5. Ненасыщенные и ароматические углеводородные радикалы.
- •1. Природа вещества гидрофобных золей и растворов полимеров.
- •Термодинамические
- •Кинетичекие
- •По происхождению:
- •По типу структуры:
- •II. Физическая конденсация
№ 1. Дисперсные системы, определение, классификация.
Дисперсная система - гетерогенная система, в которой дисперсная фаза раздроблена и распределена в дисперсионной среде.
По характеру взаимодействия частиц дисперсной фазы между собой
Свободнодисперсные — дисперсная фаза подвижна, т.к. представлена отдельными, не связанными между собой частицами, более или менее равномерно распределенными в объеме дисперсионной среды (лиозоли, суспензии, эмульсии, кровь, аэрозоли).
Связнодисперсные — дисперсная фаза практически неподвижна, т.к. образует сплошную структуру, внутри которой заключена дисперсионная среда (лиогели, студни, капиллярные системы, биомембраны, пены, гели).
По характеру взаимодействия между фазой и средой
Лиофобные системы – это системы, получающиеся в результате диспергирования и конденсации с пересыщением (принудительное образование гетерогенной свободнодисперсной системы).
Лиофильные системы – это системы, получающиеся в результате самопроизвольного диспергирования одной из фаз (самопроизвольное образование гетерогенной свободнодисперсной системы).
Классификация состояния вещества по степени его дисперсности
Состояние вещества |
Раздробленность вещества |
Макроскопическое |
Грубодисперсная |
Микроскопическое |
Тонкодисперсная |
Коллоидное или наноструктурированное |
Ультрадисперсная |
Молекулярное, атомное и ионное |
Молекулярная, атомная и ионная |
Классификация дс по агрегатному состоянию дисперсной фазы и дисперсионной среды
Д.ф./Д.ср. |
Примеры |
ж/г |
Туман, облака, аэрозоли жидких лекарств |
т/г |
Дым, пыль, порошки, аэрозоли твердых лекарств |
г/ж |
Пены, газовые эмульсии (мыльная, кислородная пена) |
ж/ж |
Эмульсии (молоко, лекарственные эмульсии) |
т/ж |
Суспензии, золи, взвеси |
г/т |
Твердые пены, хлеб, пемза, силикагель, активированные угли |
ж/т |
Жемчуг, минералы, капиллярные системы, гели |
т/т |
Цветные стекла, минералы, сплавы, самоцветы |
№ 28. Двухосновные карбоновые кислоты
1. Щавелевая НООС-СООН. Соли щ. к. распространены в растениях (кислая калиевая соль обнаружена в щавеле). В тканях организма щ. к. образуется как продукт обмена веществ и вместе с щ. к. пищи выделяется с мочой в виде оксалата кальция. При нарушениях минерального обмена оксалаты участвуют в образовании камней в почках и мочевом пузыре.
2. Малоновая НООС-СН2-СООН. В свободном виде присутствует в листьях бобовых, зелёных частях злаков и зонтичных, плодах лимона. В обмене веществ у растений и животных участвует в форме солей — малонатов. Производное малоновой кислоты — малонилкофермент А — промежуточный продукт в биосинтезе жирных кислот, может декарбоксилироваться с образованием ацетилкофермента А. Малонаты являются ингибиторами клеточного дыхания.
3. Янтарная НООС-(СН2)2СООН. В свободном и связанном виде обнаружена в тканях растений и животных. Соли янтарной кислоты (сукцинаты) промежуточные продукты цикла трикарбоновых кислот. Богатый энергией тиоэфир янтарной кислоты и кофермента А участвует в синтезе органических соединений; образуется в цикле трикарбоновых кислот при окислительном декарбоксилировании кетоглутаровой кислоты. В результате деацилирования сукцинилкофермента А образуются молекулы ГТФ (АТФ).
4. Глутаровая НООС(СН2)3СООН. Кето-производное глутаровой кислоты — α-кетоглутаровая кислота является является одним из промежуточных продуктов цикла Кребса.
5. Фумаровая HOОC-CH=CH-COОH. Эфиры фумаровой кислоты применяют для лечения псориаза. В свободном виде присутствует в высших растениях, некоторых видах грибов, лишайниках. В обмене веществ у животных, растений и микроорганизмов участвует в виде солей — фумаратов — промежуточных продуктов цикла трикарбоновых кислот, биосинтеза аспарагиновой кислоты у растений и микроорганизмов, продуктов окисления тирозина и фенилаланина.
НООС-(СН2)2СООН = HOОC-CH=CH-COОH + Н2
№ 29. Аминоспирты
Аминоспирты – это соединения, в молекуле которых одновременно содержатся амино- и гидроксильная группы. Основными представителями этой группы соединений являются 2-аминоэтанол (коламин) и гидроокись оксиэтилтриметиламмония (холин).
НОСН2СН2NН2 2-аминоэтанол - аминоспирт, входящий в состав фосфолипидов тканей животных (кефалинов); представляет собой производное этилового спирта, в молекуле которого водород метильной группы замещен аминогруппой.
НОСН2СН2N+(СН3)3 холин. Содержанится в яичном желтке, мозге, печени, почках и мышце сердца. Х. обычно относят к витаминам группы В, хотя животные и микроорганизмы способны его синтезировать. Х. входит в состав фосфолипидов (лецитина, сфингомиелина).Из Х. в организме животных синтезируется ацетилхолин — один из важнейших химических переносчиков нервных импульсов. В медицине для лечения заболеваний печени применяют хлорид Х.
№ 30. Аминофенолы
АМИНОФЕНОЛЫ - ароматические соединения, содержащие в молекуле аминогруппу и гидроксильную группу.
Дофами́н — нейромедиатор, вырабатываемый в мозгу людей и животных; гормон, вырабатываемый мозговым веществом надпочечников и другими тканями (почками), но в подкорку мозга из крови этот гормон почти не проникает. Дофамин является биохимическим предшественником норадреналина (и адреналина).
А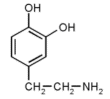 дреналин
- гормон мозгового слоя надпочечников.
Поступая в кровь, А. повышает потребление
кислорода органами и тканями, участвует
в мобилизации гликогена,
расщепление которого приводит к
нарастанию уровня сахара в крови;
стимулирует обмен веществ (белковый,
углеводный, жировой, минеральный),
повышает артериальное давление (главным
образом вследствие сужения мелких
периферических сосудов), учащает и
усиливает сердцебиение, ускоряет ритм
дыхания, замедляет перистальтику кишок
и т. д. При эмоциональных переживаниях,
усиленной мышечной работе, удушье,
охлаждении, понижении уровня сахара в
крови содержание А. в крови резко
повышается.
дреналин
- гормон мозгового слоя надпочечников.
Поступая в кровь, А. повышает потребление
кислорода органами и тканями, участвует
в мобилизации гликогена,
расщепление которого приводит к
нарастанию уровня сахара в крови;
стимулирует обмен веществ (белковый,
углеводный, жировой, минеральный),
повышает артериальное давление (главным
образом вследствие сужения мелких
периферических сосудов), учащает и
усиливает сердцебиение, ускоряет ритм
дыхания, замедляет перистальтику кишок
и т. д. При эмоциональных переживаниях,
усиленной мышечной работе, удушье,
охлаждении, понижении уровня сахара в
крови содержание А. в крови резко
повышается.
Норадреналин - биологически активное вещество из группы катехоламинов. В организме человека и животных Н. образуется частично в клетках мозгового слоя надпочечников. По действию на сердце, кровеносные сосуды, гладкие мышцы, а также на углеводный обмен Н. обладает свойствами гормона и близок к своему N-метильному производному — адреналину. Уровень Н. в крови, органах и выделениях организма позволяет судить о состоянии (тонусе и реактивности) симпатической нервной системы. Н. применяют в медицинской практике при падении кровяного давления, при коллапсе, шоке, кровопотерях и т. д.
№ 31. Аминокислоты
Аминокислоты - гетерофункциональные соединения, содержащие два типа функциональных групп с противоположными свойствами: аминогруппу ( –NН2) и карбоксильную (–СООН). -Аминокислоты являются мономерами пептидов и белков. Общая формула: – R–CH(NH2)–СООН
Классификация по природе радикала:
1. алифатические (15)
2. циклические (5)
- алициклические (пролин)
- ароматические
а) карбоциклические (тирозин и фенилаланин)
б) гетероциклические (гистидин и триптофан)
Аминокислоты, которые синтезируются в организме из продуктов метаболизма, называют заменимыми (глицин, аланин, серин, тирозин, цистеин, пролин, глутаминовая кислота, глутамин, аспарагиновая кислота, аспарагин).
Аминокислоты, которые в организме не синтезируются или синтезируются в очень малых количествах и должны поступать с пищей, называют незаменимыми (валин, лейцин, изолейцин, триптофан, треонин, метионин, гистидин, лизин и аргинин).
№ 32. Кислотно-основные св-ва аминокислот
В водных р-ах -аминокислоты сущ-ют в виде равновесной смеси диполярного иона, катионной и анионной форм:
Положение равновесия зависит от рН среды. Общим для всех -аминокислот является преобладание катионных форм в сильнокислых и анионных – в сильнощелочных средах. Значение рН, при котором суммарный заряд молекулы аминокислоты или белка равен нулю, называется изоэлектрической точкой (ИЭТ), а состояние молекулы – изоэлектрическим состоянием.
Для аминокислот кислого характера ИЭТ - в сильнокислой среде; нейтрального характера – в слабокислой среде;
основного характера – сильнощелочной.
В ИЭТ молекула не перемещается в постоянном электрическом поле ни к катоду, ни к аноду. При рН ниже ИЭТ -аминокислота заряжается положительно. При рН выше ИЭТ -аминокислота заряжается отрицательно.
№ 26. Изменение кислотных свойств в гомологическом ряду карбоновых кислот
В гомологическом ряду карбоновых кислот кислотные свойства уменьшаются от муравьиной кислоты к высшим карбоновым кислотам. Положительный индукционный эффект радикала тем больше, чем длиннее цепь, или чем более она разветвлена. В молекуле карбоновой кислоты такой радикал частично гасит δ+ на атоме углерода карбоксильной группы в соответствии с силой своего влияния. Это уменьшает поляризацию связи О – Н из-за снижения эффекта сопряжения и, как результат, понижает кислотные свойства.
№ 25. Карбоновые кислоты
Карбоновые кислоты - соединения, содержащие карбоксильную функциональную группу.
Классификация:
