
- •Введение
- •Часть I клиническая физиология главных синдромов критических состояний
- •Глава 1
- •Физиологические эффекты гиповолемии
- •Функциональные критерии
- •Глава 2 острая дыхательная недостаточность
- •Функциональные критерии
- •Принципы интенсивной терапии
- •Свертывание крови и фибринолиз
- •Первичная адгезия и агрегация
- •Реакция освобождения и вторичная агрегация
- •Принципы интенсивной терапии
- •Глава 4 гепаторенальный синдром
- •Физиологические механизмы
- •Функциональные критерии
- •Принципы интенсивной терапии
- •Глава 5 острая церебральная недостаточность
- •Физиологические механизмы
- •Функциональные критерии
- •Прогноз неврологического статуса
- •Принципы интенсивной терапии
- •Глава 6 болевой синдром
- •Физиологические механизмы
- •Принципы интенсивной терапии
- •Глава 7 операционный стресс
- •Функциональные критерии
- •Принципы физиологической защиты
- •Глава 8 нарушение метаболизма
- •Пути управления метаболизмом
- •Нарушение осмол яркости и водно-электролитного баланса
- •Часть II клиническая физиология методов интенсивной терапии, анестезии и реанимации
- •Реанимация при остановке сердца и дыхания
- •Г л а в а 11 инфузионная и трансфузионная терапия
- •Инфузия медикаментов
- •Парентеральное питание
- •Методы инфузионной терапии
- •Глава 12 вспомогательное кровообращение
- •Метод контрпульсации
- •Шунтирование желудочков
- •Функциональные эффекты
- •Глава 13 респираторная терапия
- •Оптимизация естественных механизмов дренирования мокроты
- •Глава 14 антигипоксическая терапия (ингаляционная, трансфузионная и медикаментозная)
- •Ингаляционная оксигенотерапия
- •Гипербарическая оксигенация
- •Энтеральная оксигенация
- •Трансфузионая оксигенация
- •Искусственная вентиляция легких
- •Клинико-физиологические аспекты процедуры искусственной вентиляции легких
- •Объективные критерии
- •Глава 16 искусственная миоплегия
- •Миорелаксанты и мышечная система
- •Глава 17 детоксикационная терапия
- •Стимуляция естественной детоксикации
- •Искусственная детоксикация
- •Синдроматическая терапия
- •Глава 18 мониторизация
- •Принципы мониторизации
- •Методы и цели
- •Параметры мониторизации
- •Часть III клинико-физиологический анализ итар в повседневной практике
- •Глава 19 акушерство
- •Амниотическая эмболия
- •Эклампсия
- •Глава 20 неонатология и педиатрия
- •Реанимация новорожденных
- •Бронхиолит
- •Синдром внезапной смерти младенца
- •Глава 21 пульмонология Влияние анестезиологического пособия на дыхание
- •Тромбоэмболия легочной артерии
- •Бронхоастматический статус
- •Отек легких
- •Синдром шокового легкого
- •Глава 22 кардиология
- •Внезапная кардиальная смерть
- •Кардиогенный шок
- •Глава 23 гепатология
- •Острая печеночная недостаточность
- •Нефрология Влияние анестезии на функции почек
- •Острая почечная недостаточность
- •Глава 25 гематология
- •Геморрагический шок
- •Глава 26 неврология и нейрохирургия
- •Эпилептический статус
- •Столбняк
- •Поражение головного мозга
- •Поражение спинного мозга
- •Глава 27 гастроэнтерология
- •Острейший гастроэнтерит
- •Травматология
- •Травматический шок
- •Синдром жировой эмболии
- •Газовая эмболия
- •Глава 29 иммунологические аспекты практики итар
- •Аллергия в практике итар
- •Анафилактический шок
- •Септический шоковый синдром
- •Список литературы
- •Оглавление
- •Часть I. Клиническая физиология главных синдромов критических состояний ..........……………………………………….. 12
- •Глава 1. Нарушение реологии крови и острая гиповолемия .…………….. 12
- •Глава 2. Острая дыхательная недостаточность ...…………………………... 30
- •Глава 11. Инфузионная и трансфузионная терапия ....……………………… 141
- •Глава 21. Пульмонология ...........………………………………………………….. 250
- •Глава 28. Травматология . . . .......………………………………………………….. 341
- •Глава 29. Иммунологические аспекты практики итар ..…………………….. 351
Свертывание крови и фибринолиз
Функции системы крови и ее составной части — системы лимфы— чрезвычайно многообразны. Большинство этих функций связано с транспортной ролью крови и лимфы, которые переносят газы, питательные вещества, гормоны, медиаторы, подлежащие экскреции продукты метаболизма, тепло. Помимо транспортных, кровь и лимфа выполняют собственные, присущие только им функции: защиту организма выработкой иммунных тел или действием клеток и лимфы, буферную роль в поддержании нормального состава воды, электролитов, кислых и щелочных продуктов во всех тканях и средах организма и, наконец, тромбообразование, спасающее организм от кровопотери, или тромболиз, предупреждающий ишемию.
Вопросами свертывания крови медицина занимается более 100 лет. Несмотря на большие успехи, достигнутые в изучении этой проблемы, она еще во многом остается неясной. Заложенная на рубеже прошлого и нынешнего столетия сравнительно простая по сути ферментативная теория Шмидта — Моравица обросла таким обилием нрвых сведений, что разобраться в них полностью — дело будущего. Однако повседневная практика не позволяет реаниматологу ждать достижения абсолютной истины, потому что останавливать или предупреждать тромбозы и коагулопатические кровотечения надо уже сегодня.
Обеспечивая нормальное состояние системы кровообращения, свертывание крови в свою очередь зависит от функционального состояния многих систем организма. На систему свертывания крови влияют объем циркулирующей крови и скорость кровотока, газообмен, состояние эндокринной системы, костного мозга, печени, селезенки, почек, лимфатической системы. Свертывание меняется при изменении реологических свойств крови, кислотно-щелочного состояния, электролитного баланса. Оно, наконец, зависит от функционального состояния собственно свертывающей, антикоагулянтной и фибринолитической систем крови. Поскольку при критическом состоянии меняется функциональное состояние всех перечисленных систем, характер свертывания крови не может не измениться.
Чтобы разобраться в невероятном многообразии факторов, которым приписывают участие в свертывании крови, необходимо заранее договориться о некоторых принципиальных положениях:
1. Существуют специальные системы, поддерживающие жидкое состояние крови, пока не возникнет нужда в местном образовании тромба, необходимого для остановки кровотечения, из поврежденного сосуда. При нормальном течении процесса кровь в остальной части системы кровообращения остается жидкой, а образовавшийся для гемостаза тромб не растворяется фибринолитической системой.
При аномальных условиях возможны три варианта отклонений: а) тромб не образуется и кровотечение не останавливается, б) тромбы образуются везде — и там, где они нужны для гемостаза, и в неповрежденных сосудах, где они вызывают ишемию тканей; в) образовавшийся тромб растворяется и кровотечение возобновляется.
2. Чтобы образовался тромб, необходимо воздействие трех участников этого процесса: сосудистой стенки, форменных элементов крови и плазмы. Каждый участник тромбообразования несет в себе следующие группы веществ: факторы свертывания и фибринолиза, активаторы того и другого процесса, ингибиторы того и другого процесса, ко- и профакторы того и другого процесса, активаторы и ингибиторы ко- и профакторов обоих процессов.
Поскольку эта книга — руководство по клинической физиологии, в дальнейших рассуждениях мы будем употреблять названия лишь минимального количества факторов, необходимых для решения клинических проблем или обоснования физиологических механизмов.
3. Внутри сосудов идет непрерывный процесс образования и растворения фибрина, необходимого для выстилки изнутри всего сосудистого русла, камер сердца, клапанов, нитей и т. д., хотя есть сомнения в том, что такой процесс идет непрерывно. Местный гемостаз при повреждении сосуда —близкий, но не идентичный процесс: это не просто образование фибрина, а вязкий метаморфоз тромбоцитов, их склеивание с возникновением пластинчатой тромбоцитарной «пробки». Затем на ее основе образуется фибринный сгусток, в котором останавливаются клеточные элементы крови, возникают молекулярная перестройка и ретракция тромба, плотно соединяющегося с сосудистой стенкой в месте ее повреждения. Спазм поврежденного сосуда с выходом из сосудистой стенки биологически активных веществ— важный компонент местного гемостаза.
4. В свертывании крови большую роль играют электрокинетические явления. Установлено, что сосудистая стенка имеет электрический заряд. Интима по отношению к адвентиции заряжена отрицательно, и трансмуральный потенциал составляет около 10—15 мВ. Определенный электроотрицательный заряд несут тромбоциты и эритроциты. Все это препятствует склеиванию тромбоцитов и эритроцитов между собой и с сосудистой стенкой.
Различные медиаторы (в частности, катехоламины, ацетилхолин), активные полипептиды (ангиотензин, брадикинин), кислые метаболиты, многие лекарственные вещества способны менять величину электрического потенциала сосудистой стенки, эритроцитов и тромбоцитов, способствуя или препятствуя их адгезии и агрегации. Вырабатываемый эндотелием сосудов простациклин (простагландин X) препятствует адгезии тромбоцитов к сосудистой стенке.
Электровазограмма (измерение трансмурального потенциала сосудистой стенки) меняется при стимуляции симпатического ствола и блуждающего нерва, при введении адренергических и холинергических препаратов, антикоагулянтов и фибрино-литиков.
Самосохраняющая функция крови обеспечивается тремя системами: свертывающей (образующей фибрин-тромб), антикоагулянтной (препятствующей возникновению фибринных сгустков и тромба) и фибринолитической (растворяющей уже образовавшиеся сгустки фибрина и тромб).
5. Известны два главных механизма свертывания крови, имеющие различное назначение (рис. 15): 1) сосудисто-тромбоцитарный гемостаз осуществляется главным образом в системе микроциркуляции и предназначен преимущественно для первичной остановки кровотечения из поврежденных сосудов; 2) коагуляционное тромбообразование — ферментативный трехфазный процесс, предназначенный в основном для образования внутрисосудистой фибринной выстилки, но участвующий и в остановке кровотечения, укрепляя тромбоцитарную пробку, причем оба процесса — сосудисто-тромбоцитарный гемостаз (первичный) и ферментативная коагуляция происходят не последовательно, а фактически одновременно.
После предварительных замечаний можно перейти к рассмотрению трех упомянутых выше систем крови — свертывающей, антйкоагулянтной и фибринолитической.
Свертывающая система крови. Как уже отмечено, свертывающая система представлена двумя главными механизмами — сосудисто-тромбоцитарным и ферментативно-коагуляционным.
Сосудисто-тромбоцитарный гемостаз начинается как гемостатическая реакция в месте повреждения сосудистой стенки. У раненой интимы с обнаженным коллагеном резко меняется электрический дзета-потенциал, в результате чего к раневой поверхности прилипают заряженные тромбоциты (адгезия). Одновременно начинаются склеивание тромбоцитов между собой (агрегация) и стимуляция ими ферментативной коагуляции.
Исследования последних лет показали, как мало мы знали о функции тромбоцитов, низводя их роль до пассивного хранения тромбокиназы. В них имеются участвующие в свертывании крови фибриноген, антигемофильный глобулин, тромбопластин, многие активаторы и ингибиторы фибринолиза. Оказалось, что эти диски диаметром 2—4 мкм и толщиной 1 мкм снабжены митохондриями, гранулами, содержащими серотонин, адреналин, лизосомные ферменты, АДФ и другие вещества, вакуолями, канальцами, сократительным белком тромбостенином, позволяющим тромбоциту менять свою форму. Многочисленные активные вещества адсорбированы на поверхности тромбоцитов, некоторые находятся внутри них и могут выходить на поверхность через микротубулы.
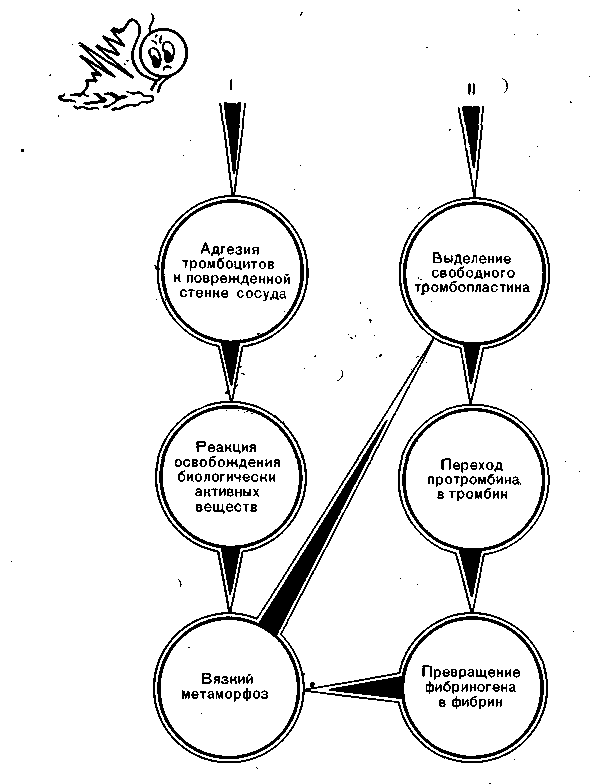
Рис. 15. Механизмы гемостаза. I — сосудисто-тромбоцитарный гемостаз; II — ферментативная коагуляция.
Функциональная взаимосвязь тромбоцитов и сосудистой стенки исключительно высока и не ограничивается сосудисто-тромбоцитарным гемостазом: около 15% тромбоцитов передают эндотелию свои биологически активные и питательные вещества, без чего возникают дефекты проницаемости сосудов. Помимо этого, тромбоциты участвуют в фагоцитозе инородных частиц, бактерий и вирусов, в реакции воспаления, отторжения инородных антигенных структур и во многих других не относящихся к гемостазу реакциях.
Адгезия тромбоцитов к обнаженному коллагену сосудистой стенки происходит за несколько секунд и сопровождается так называемой реакцией освобождения из тромбоцитов биологически активных веществ, которые способствуют следующей фазе сосудисто-тромбоцитарного гемостаза — агрегации тромбоцитов, заканчивающейся за несколько минут. Среди биологически активных веществ, освобождающихся из тромбоцитов, главным является АДФ, но к его действию присоединяется влияние серотонина, адреналина, тромбина и других факторов. Интересно, что тромбин, предназначенный, казалось бы, для ферментативной коагуляции, стимулирует агрегацию тромбоцитов, т. е. биофизический гемостаз, причем в количествах, во много раз меньших, чем требуется для включения ферментативной коагуляции.
В реакциях освобождения и в агрегации тромбоцитов важную и не до конца изученную роль играют система аденилциклаза — цАМФ — фосфодиэстераза; а также простагландины, среди которых есть активирующие агрегацию (ПГF2, ПГЕ2) и тормозящие ее (ПГЕ1).
В процессе адгезии и агрегации тромбоциты изменяют дисковидную форму на шаровидную (это происходит еще до приклеивания тромбоцита к коллагену), у них появляются псевдоподии и образуется сеть, на которую оседают фибрин и форменные элементы, образуя тромб. Сосудисто-тромбоцитарный гемостаз — это преимущественно биофизический процесс, основу которого составляют электрокинетические явления в стенке сосуда и действие биологически активных веществ, не относящихся к классическим факторам свертывания.
Что касается второго механизма свертывания крови — ферментативной коагуляции, то ее можно разделить на три фазы: 1) активацию тромбопластина, протеолитического фермента, содержащегося в неактивном, состоянии в форменных элементах крови и тканях; 2) превращение протромбина в тромбин под действием тромбопластина. Протромбин — белок глобулярной фракции, концентрация которого в плазме составляет 10—15%; 3) превращение фибриногена в фибрин под действием фермента тромбина. Фибриноген — белок глобулярной фракции, его концентрация в плазме 2—3,5 г/л (200—350 мг%). Как и протромбин, он синтезируется печенью, при функциональной недостаточности которой активность двух названных фаз ферментативного свертывания крови может быть снижена. Правда, в печени синтезируется только 75% фибриногена, и именно эта форма циркулирует в плазме. 25% фибриногена синтезируется мегакариоцитами костного мозга, и коагуляция этого фибриногена, адсорбированного на тромбоцитах, происходит медленнее, чем плазматического.
Образование фибрина-мономера — обратимый процесс. Затем происходят полимеризация фибрина и стабилизация его в виде тромба фибринстабилизирующим ферментативным фактором.
Активаторы ферментативной коагуляции содержатся во всех форменных элементах крови, при разрешении которых (например, при гемолизе) ферментативная коагуляция усиливается. Однако особо следует подчеркнуть роль тромбоцитов не только как инициаторов сосудисто-тромбоцитарного гемостаза, но и активаторов ферментативной коагуляции.
Рассмотренная схема трехэтапной ферментативной коагуляции упрощена сравнительно с уже сегодня известной нелинейной каскадно-комплексной многоступенчатой схемой свертывания, в которой участвуют несколько десятков различных факторов.
Для рассмотрения клинической физиологии синдрома РВС нам, вероятно, достаточно и этой упрощенной схемы. Однако надо подчеркнуть два важных обстоятельства: 1) в свертывании крови активно участвуют калликреин-кининовая и комплементарная системы, 2) в процессе свертывания образуются вещества, являющиеся его ингибиторами, т. е. относящиеся уже к антикоагулянтой системе.
Антикоагулянтная система. Ее не надо путать с фибринолитической системой: антикоагулянтная препятствует образованию тромбов, тогда как фибринолитическая растворяет уже образовавшиеся тромбы.
Мы различаем в антикоагулянтной системе две группы факторов: постоянно существующие и образующиеся в процессе свертывания.
Постоянные антикоагулянты. Из постоянно существующих физиологических антикоагулянтов самым мощным является антитромбин III — α2-глобулин, концентрация которого в плазме около 2 г/л (200 мг%). Он активируется гепарином и обеспечивает не менее 3/4 антикоагулянтной активности плазмы. Есть и другие естественные антикоагулянты, например α2-макроглобулин.
Активатор антитромбина III гепарин является мукополи-сахаридом, образующимся во всех органах и тканях. Наиболее активно синтез его происходит в легких и печени.
Будучи катализатором, почти не потребляемым в ходе реакции, гепарин делает медленную реакцию антитромбина III мгновенной. Главный (но не единственный) эффект активированного гепарином антитромбина III — блокада тромбина, превращающего фибриноген в фибрин. Установлено, что при низкой активности антитромбина III (патология печени, острые тромбозы, состояние после операции, применение оральных контрацептивов) тромбо-эмболические осложнения возникают чаще.
В меньшей степени гепарин тормозит другие звенья коагуляции. Он образует комплексы с фибриногеном, плазмином, адреналином, снижает адгезивность тромбоцитов, увеличивая их отрицательный заряд. Гепарин способствует дезагрегации эритроцитов и улучшает реологические свойства крови.
Физиологическая активность гепарина исключительно велика. Реагируя с положительно заряженными молекулами белка и NH2-группами, где бы они ни находились, гепарин оказывает тормозящее влияние более чем на 20 ферментативных систем; свертывающую, антиген — антитело, гиалуронидаза — гиалуроновая кислота и др. Гепарин является антагонистом серотонина, гистамина, альдостерона. Он активирует липолиз, реагирует с токсинами, вирусами, антибиотиками. Вероятно, именно высокая физиологическая активность сделала гепарин столь широко применяемым в реаниматологии средством.
Образующиеся антикоагулянты. К антикоагулянтам, возникающим в ходе свертывания крови, относится прежде всего сам сформировавшийся фибрин, который немедленно извлекает из плазмы весь непрореагировавший активный тромбин, тормозя дальнейшее, уже ненужное свертывание крови по типу обратной связи. Такой же или несколько меньшей антикоагулянтной активностью обладают пептиды А и В, отщепившиеся от фибриногена, когда он под действием тромбина превращается в фибрин.
Антикоагулянтные вещества образуются не только в ходе свертывания крови, но и в ходе фибринолиза—факт, который также потребуется для рассуждений о физиологических механизмах и интенсивной терапии синдрома РВС.
Поскольку мы отнесли к свертывающей системе механизм сосудисто-тромбоцитарного гемостаза, видимо, факторы и вещества, тормозящие этот механизм, должны быть отнесены к антикоагулянтной системе. В большинстве своем это вещества, тормозящие реакцию освобождения из тромбоцитов биологически активных продуктов.
Естественными ингибиторами эффекта тромбоцитов являются продукты расщепления фибрина в ходе фибринолиза, а также простагландин Е1.
Среди тромбоцитарных ингибиторов медикаментозного характера следует прежде всего назвать ацётилсалициловую кислоту, которая тормозит выход АДФ (основной фактор адгезии и агрегация тромбоцитов), воздействуя на продукцию некоторых простагландинов и кининов, способствующих освобождению АДФ. В связи с этим свойством ацетилсалициловой кислоты ее с успехом, используют при лечении ишемии мозга и миокарда, гемолитических синдромов, для хранения консервированной крови. Ее добавляют во флаконы с кровью либо дают внутрь донорам перед взятием у них крови. Антитромбоцитарный эффект ацетилсалициловой кислоты сохраняется в течение нескольких дней после однократного приема.
Так же, хотя и менее выражение, действуют бутадиен, индометацин, дипиридамол и низкомолекулярный декстран реополиглюкин.
Поскольку это имеет значение для дальнейших рассуждений, мы объединяем факторы, стимулирующие первичную адгезию и агрегацию тромбоцитов, а затем реакцию освобождения биологически активных веществ и вторичную агрегацию.
