
- •Введение
- •Часть I клиническая физиология главных синдромов критических состояний
- •Глава 1
- •Физиологические эффекты гиповолемии
- •Функциональные критерии
- •Глава 2 острая дыхательная недостаточность
- •Функциональные критерии
- •Принципы интенсивной терапии
- •Свертывание крови и фибринолиз
- •Первичная адгезия и агрегация
- •Реакция освобождения и вторичная агрегация
- •Принципы интенсивной терапии
- •Глава 4 гепаторенальный синдром
- •Физиологические механизмы
- •Функциональные критерии
- •Принципы интенсивной терапии
- •Глава 5 острая церебральная недостаточность
- •Физиологические механизмы
- •Функциональные критерии
- •Прогноз неврологического статуса
- •Принципы интенсивной терапии
- •Глава 6 болевой синдром
- •Физиологические механизмы
- •Принципы интенсивной терапии
- •Глава 7 операционный стресс
- •Функциональные критерии
- •Принципы физиологической защиты
- •Глава 8 нарушение метаболизма
- •Пути управления метаболизмом
- •Нарушение осмол яркости и водно-электролитного баланса
- •Часть II клиническая физиология методов интенсивной терапии, анестезии и реанимации
- •Реанимация при остановке сердца и дыхания
- •Г л а в а 11 инфузионная и трансфузионная терапия
- •Инфузия медикаментов
- •Парентеральное питание
- •Методы инфузионной терапии
- •Глава 12 вспомогательное кровообращение
- •Метод контрпульсации
- •Шунтирование желудочков
- •Функциональные эффекты
- •Глава 13 респираторная терапия
- •Оптимизация естественных механизмов дренирования мокроты
- •Глава 14 антигипоксическая терапия (ингаляционная, трансфузионная и медикаментозная)
- •Ингаляционная оксигенотерапия
- •Гипербарическая оксигенация
- •Энтеральная оксигенация
- •Трансфузионая оксигенация
- •Искусственная вентиляция легких
- •Клинико-физиологические аспекты процедуры искусственной вентиляции легких
- •Объективные критерии
- •Глава 16 искусственная миоплегия
- •Миорелаксанты и мышечная система
- •Глава 17 детоксикационная терапия
- •Стимуляция естественной детоксикации
- •Искусственная детоксикация
- •Синдроматическая терапия
- •Глава 18 мониторизация
- •Принципы мониторизации
- •Методы и цели
- •Параметры мониторизации
- •Часть III клинико-физиологический анализ итар в повседневной практике
- •Глава 19 акушерство
- •Амниотическая эмболия
- •Эклампсия
- •Глава 20 неонатология и педиатрия
- •Реанимация новорожденных
- •Бронхиолит
- •Синдром внезапной смерти младенца
- •Глава 21 пульмонология Влияние анестезиологического пособия на дыхание
- •Тромбоэмболия легочной артерии
- •Бронхоастматический статус
- •Отек легких
- •Синдром шокового легкого
- •Глава 22 кардиология
- •Внезапная кардиальная смерть
- •Кардиогенный шок
- •Глава 23 гепатология
- •Острая печеночная недостаточность
- •Нефрология Влияние анестезии на функции почек
- •Острая почечная недостаточность
- •Глава 25 гематология
- •Геморрагический шок
- •Глава 26 неврология и нейрохирургия
- •Эпилептический статус
- •Столбняк
- •Поражение головного мозга
- •Поражение спинного мозга
- •Глава 27 гастроэнтерология
- •Острейший гастроэнтерит
- •Травматология
- •Травматический шок
- •Синдром жировой эмболии
- •Газовая эмболия
- •Глава 29 иммунологические аспекты практики итар
- •Аллергия в практике итар
- •Анафилактический шок
- •Септический шоковый синдром
- •Список литературы
- •Оглавление
- •Часть I. Клиническая физиология главных синдромов критических состояний ..........……………………………………….. 12
- •Глава 1. Нарушение реологии крови и острая гиповолемия .…………….. 12
- •Глава 2. Острая дыхательная недостаточность ...…………………………... 30
- •Глава 11. Инфузионная и трансфузионная терапия ....……………………… 141
- •Глава 21. Пульмонология ...........………………………………………………….. 250
- •Глава 28. Травматология . . . .......………………………………………………….. 341
- •Глава 29. Иммунологические аспекты практики итар ..…………………….. 351
Анафилактический шок
Нельзя сказать, чтобы анафилактический шок встречался очень часто, но постепенно нарастающая аллергизация населения должна внушить тревогу и заставить подумать о вероятности учащения этой жестокой патологии. Несмотря на значительные успехи реаниматологии, летальность при анафилактическом шоке достигает 60%.
Анафилактический шок относится к I типу реакций иммунитета — атоническим (освобождение из тучных клеток биологически активных веществ). Он развивается в ответ на применение какого-либо аллергена, к которому организм был сенсибилизирован ранее. Все вещества, которые вводятся сегодня в тело человека при еде, питье, лечении, могут оказаться аллергенами и вызвать анафилактический шок.
Наиболее часто анафилактический шок вызывают пенициллин и другие антибиотики, новокаин и другие местные анестетики, кардиотраст и другие йодсодержащие контрастные вещества, трансфузионные препараты, содержащие белок, белковые гидролизаты и, декстраны, витамины (особенно группы В), лечебные сыворотки и вакцины.
Несмотря на то что общие анестетики подавляют иммунные реакции, описан анафилактический шок при введении всех общих анестетиков и релаксантов, особенно часто сомбревина (эпонтола). Анестезиологам следует помнить, что практически нет медикаментов и трансфузионных препаратов, применяющихся для премедикации, наркоза, миорелаксации, интенсивной терапии, под действием которых не могла бы возникнуть аллергическая реакция. Проблема эта настолько острая, что специальный международный симпозиум во Франции (Нанси, 1976 г.) был назван «Аллергический риск при анестезии».
Нередко анафилактический шок возникает в ответ на первое введение антибиотика или иного лекарства, когда, казалось бы, первичной сенсибилизации не было. Такие случаи могут быть объяснены наследственной передачей антител, использованием плохо отмытых шприцев, предшествующим вдыханием медикаментов и т. п.
Если же не удается обнаружить первое столкновение организма с антигеном, бурную реакцию на введение какого-либо вещества принято относить к анафилактоидному, или гистаминовому, шоку. При этом подразумевают, что освобождение (делиберация) гистамина из тучных клеток 1произошло не под действием реакции антиген — антитело, а в связи с неблагоприятным сочетанием различных веществ — делибераторов гистамина.
Помимо лекарств, анафилактический шок может быть вызван укусами пчел, ос и других насекомых. К анафилактическому шоку у человека, которого ужалила пчела или оса, надо относиться весьма серьезно. В США, например, смертельные исходы при этом наблюдаются в 3 раза чаще, чем при укусах гремучих змей.
Реже наблюдается холодовая и пищевая аллергия с анафилактическим шоком (в том числе, на коньяк, водку и крепленые вина). Не надо думать, что в таких случаях возникает не анафилактический шок, а естественная реакция на избыточные дозы коньяка, водки или, например, тиопентала, эфира, сомбревина при наркозе. Во-первых, анафилактический шок развивается при воздействии малых, иногда ничтожных количеств этих веществ, потому что его суть — не непосредственное действие самого аллергена (коньяк, тиопентал и т. п.), а физиологический эффект агрессивных веществ, которые аллерген «выпускает» из клеток, связанных антителами. Во-вторых, аллергологический анамнез и последующее антигенное тестирование позволяют достоверно подтвердить аллергический характер шоковой реакции.
Что касается холодовой аллергии, где, казалось бы, нет материального субстрата для атонической реакции, то возможны два варианта. Под действием холода могут образоваться делибераторы гистамина (анафилактоидный шок) или тучные клетки, расположенные в легких и омываемые холодным воздухом, могут выпустить стандартный набор активных веществ, вызывающих анафилаксию (см. ниже).
Физиологические механизмы. Комплекс антиген — антитело действует на тучные клетки, содержащие биологически активные вещества, делая мембрану клеток проницаемой и выпуская эти вещества наружу, чтобы они сыграли свою агрессивную роль.
Проницаемость мембраны для этих веществ зависит от циклического аденозин-3,5-монофосфата (цАМФ), управляемого ферментами аденилциклазой (образование цАМФ) и фосфодиэстеразой (инактивация цАМФ). Чем меньше в клетке цАМФ, тем быстрее из нее выходят агрессивные вещества.
Что это за агрессоры, с которых начинается танатогенез анафилактического шока? Биологически активных веществ, ми^но пребывающих внутри тучных клеток, пока аллерген не выпустил их наружу, вероятно, много, но мы перечислим здесь основные: гистамин, серотонин, ацетилхолин, брадикинин, гепарин, медленно реагирующая субстанция анафилаксии (SRS-A, или МРС-А), эозинофильный хемотаксический фактор анафилаксии (ЕСТ-А, или ЭХФ-А) и фактор, активирующий тромбоциты (PAF, или ФАТ). Именно эти вещества ответственны за ту вегетативную бурю, которая разыгрывается в организме во время анафилактического шока.
Хорошо известно и уже не раз обсуждалось в руководстве действие всех перечисленных веществ (кроме трех последних) на гладкие мышцы сосудов, бронхов, на проницаемость клеточных мембран, агрегацию тромбоцитов, ферментативные процессы и т. п.
Что касается МРС-А, то она образуется в течение нескольких часов (если больной их проживет!) и усиливает бронхиолоспазм и тонус различных гладкомышечных органов, а кроме того, расширяет венулы и увеличивает их проницаемость. Точная структура этого вещества неизвестна, но установлено, что на его эффект не влияют антигистаминные, антисеротониновые и антихолинергические средства. ФАТ усиливает уже происходящую агрегацию тромбоцитов, а ЭХФ-А увеличивает количество эозинофилов, которые выделяют или активируют ферменты, нейтрализующие гистамин, и другие медиаторы анафилаксии. Однако действия этих эозинофилов совершенно недостаточно, чтобы ликвидировать в организме опасные следы разгула агрессоров, выделившихся из тучных клеток.
П. Эрлих, еще будучи студентом, подробно изучивший эозинофилы (как, впрочем, и тучные клетки), сообщил о них впервые в 1879 г., но лишь в последнее десятилетие их функция стала несколько проясняться. Обнаружено, что основные белки, выделяемые гранулами эозинофилов, вызывают воспаление бронхиального эпителия, сходное с астматическими изменениями. Не на этом ли основан благоприятный эффект глюкокортикоидов при астме, поскольку установлено, что мокрота у больных бронхиальной астмой содержит большие количества основных белков из гранул эозинофилов? С другой стороны, эозинофилы с помощью своей арилсульфатазы и гистаминазы подавляют МРС-А и гистамин и тормозят выход из тучных клеток агрессоров анафилаксии. Следовательно, вопрос о том, полезна или вредна для организма обнаруживаемая в периферической крови эозинофилия, остается пока открытым.
Функциональные следствия выхода из тучных клеток агрессоров анафилаксии таковы (рис. 56).
Во-первых, возникает внезапная гиповолемия, когда объема крови не хватает из-за резкого расширения сосудистого русла вследствие вазомоторного паралича. Надо полагать, что связанное с этим замедление кровотока вызывает нарушение реологических свойств крови, которое ведет к ее секвестрации и усилению гиповолемии.
Во-вторых, нарушается проницаемость различных мембран и возникают интерстициальные отеки, прежде всего в мозге и в легких. В сочетании с нарушениями свертываемости крови и поражением эндотелия это может привести к петехиальным кровоизлияниям вокруг мелких сосудов в коже и жизненно важных органах; например в мозге. В связи с переходом жидкости в интерстиций наблюдаются сгущение крови (увеличиваются гемоглобин и гематокрит) и еще большее снижение ОЦК.
В-третьих, возникают ларингоспазм и бронхиолоспазм, к которому присоединяется действие интерстициального отека, вызывающего экспираторное закрытие дыхательных путей, а также накопление мокроты в дыхательных путях. Связанные с этим гипоксия, респираторный и метаболический,ацидоз еще больше нарушают проницаемость мембран, усиливая интерстициальные отеки и поражение легких.
В-четвертых, наблюдается спастическое сокращение кишечника, мочевого пузыря, матки с соответствующей клинической картиной (диарея, непроизвольное мочеиспускание, кровянистые выделения из влагалища).
Наконец, если больной переживает острый период, в дальнейшем могут развиться органные расстройства, связанные с цито- и гистотоксическими эффектами аллергии; гемолиз и тромболиз с последующей коагулопатией, острой почечной и печеночной недостаточностью, а в более поздние сроки — поражение мозга, гепатит, нефрит, миокардит.
Непосредственные механизмы танатогенеза в первые минуты анафилактического шока — острая недостаточность кровообращения в связи с сосудистым коллапсом и гиповолемией, острая дыхательная недостаточность из-за нарушения бронхиальной проходимости, отек мозга.
При более спокойном течении анафилактического шока успевают проявиться уртикарные высыпания на коже, мелкие кровоизлияния, нарушение систем гемостаза и фибринолиза с более или менее выраженными кровотечениями. В дальнейшем в клинической картине преобладает одно или несколько следствий анафилактического шока — поражения мозга, миокарда, печени, почек.
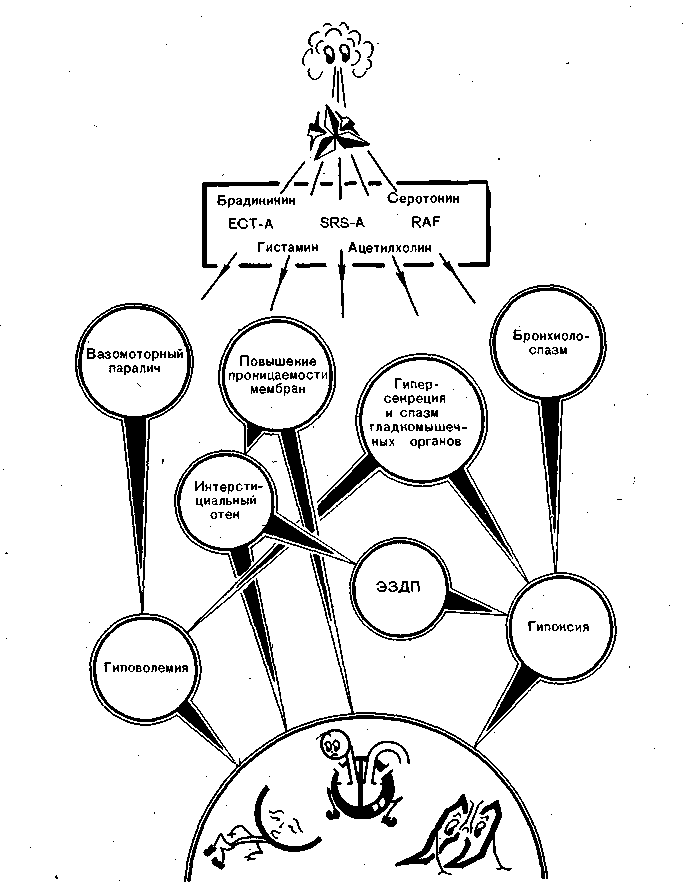
Рис. 56. Физиологические механизмы анафилактического шока.
Непосредственные причины смерти в первые минуты или часы — отек мозга, острая гиповолемия с миокардиальной недостаточностью и острая дыхательная недостаточность.
При патоморфологическом исследовании обнаруживают резкое полнокровие органов с повышенной проницаемостью капилляров, в отношении как плазмы, так и форменных элементов крови. Почти всегда наблюдаются отек мозга и других тканей и кровоизлияния во внутренние органы, в том числе геморрагическое инфарцирование легких.
Принципы интенсивной терапии. К сожалению, при лечении анафилактического шока целесообразнее использовать комплекс реанимации, а не интенсивной терапии, так как патология иногда развивается столь быстро, что квалифицированная помощь может опоздать.
Тем не менее, если известны механизмы танатогенеза и можно проследить развитие анафилактического шока, рациональные меры интенсивной терапии могут быть определены достаточно четко.
Устранение гиповолемии. Поскольку ведущим механизмом танатогенеза при анафилактическом шоке является острая гиповолемия, устранить ее надо в первую очередь. Это может быть достигнуто двумя путями — сокращением кровенос-
ного русла и увеличением ОЦК. Оба метода ликвидации гиповолемии в приложении к анафилактическому шоку имеют и достоинства, и недостатки.
1. Сокращение сосудистого русла можно получить введением вазопрессоров — адреналина, норадреналина, эфедрина, мезатона и др. Вопрос, однако, не столь прост, как может показаться.
Оказалось, что β-адреностимуляторы (адреналин, изопротеренол) повышают уровень цАМФ в клетке и тем самым сокращают выход из нее агрессивных веществ, а α-адреностимуляторы (норадреналин) и β-адреноблокаторы (индерал) оказывают противоположное действие, т. е. создают предпосылки для углубления анафилактического шока.
С другой стороны, адреналин на фоне гипоксии и метаболического ацидоза— постоянных спутников анафилактического шока — должен способствовать наступлению фибрилляции сердца. Кроме того, он повышает метаболизм, требуя от легких такого количества кислорода, которое они дать не в состоянии, да и кровоток пока не способен донести кислород до тканей. Правда, адреналин и другие β-адреностимуляторы достаточно быстро уменьшают или даже устраняют бронхиолоспазм. Может быть, полезным окажется ангиотензинамид (гипертензин), который в десятки раз активнее норадреналина?
2. Трансфузия различных жидкостей восполняет ОЦК довольно быстро, хотя, возможно, несколько позже, чем может сократиться сосудистое русло под действием вазопрессоров. Однако кристаллоидные растворы быстро покидают сосудистое русло в связи с повышенной проницаемостью капилляров. Декстраны (полиглюкин, реополиглюкин) удерживаются в сосудистом русле долго, но могут усилить аллергию.
Наиболее рациональным для устранения гиповолемии нам представляется струйное переливание 0,5—1,5 л 5% раствора глюкозы, в первые 200 мл которой добавлены 0,5 мл 0,1% раствора адреналина, а в следующие 200 мл — 0,5 мл 0,1% раствора норадреналина. В дальнейшем коррекция гиповолемии проводится на фоне прочих рассмотренных ниже мероприятий и осуществляется под контролем не только артериального, но и, главное, центрального венозного давления. Для устранения гиповолемии можно использовать полиглюкин, раствор Рингера, 5% раствор глюкозы, изотонический раствор хлорида натрия и другие кристаллоидные растворы.
Устранение острой дыхательной недостаточности. Поскольку главными механизмами острой дыхательной недостаточности при анафилактическом шоке являются бронхиолоспазм, интерстициальный отек легких и центральное нарушение регуляции дыхания, первая неотложная мера — это интубация трахеи и ИВЛ 100% кислородом. Одновременно применяется бронхоспазмолитическая терапия — внутривенное введение β2-адреностимулятора алупента (метапротеренол) и аэрозольная ингаляция того же алупента или (β1-адреностимулятора эуспирана (изопротеренол). Положительный эффект может дать внутривенное введение раствора эуфиллина, действующего как бронхоспазмолитик. Если в клинической картине преобладает холинергический эффект и бронхиолоспазм сопровождается брадикардией, необходимо ввести внутривенно раствор атропина (М-холинолитик).
Сочетанная терапия позволяет не только сохранить больному жизнь, но и устраняет некоторые опасные механизмы: ликвидируется бронхиолоспазм, благодаря высокому альвеолярному давлению при ИВЛ уменьшается интерстициальный отек, снижаются гипоксия и респираторный ацидоз.
Антигистамлнная терапия. Значительная часть механизмов танатогенеза при анафилактическом шоке связана с выраженной гистаминемией, поэтому необходимо внутривенное введение растворов антигистаминных препаратов (супрастин, пипольфен и т. д.), но не нужно слишком надеяться на эффективность этой меры.
Специфическая терапия. Не следует забывать, что анафилактический шок — бурная аллергическая реакция, при ликвидации которой может оказаться уместной специфическая терапия. Если шок качался после внутримышечного или подкожного введения какого-либо вещества и проксимальнее места инъекции можно наложить жгут, это надо сделать, хотя и не следует переоценивать значение такой меры. Аллергия тем и отличается от интоксикации, что при ней нет пропорциональной зависимости между тяжестью патологического эффекта и дозой всосавшегося препарата.
Что касается неспецифических ингибиторов иммунных реакций — глкжокортикоидных гормонов, то при любом виде анафилактического шока необходимо немедленно ввести внутривенно преднизолон или дексазон, хотя, насколько нам известно, объективной проверки эффективности этой меры не проводилось.
Большой интерес представляет попытка задержать биологически активные вещества в клетке, меняя проницаемость клеточной мембраны воздействием на уровень цАМФ. Как уже отмечалось, чем больше в клетке цАМФ, тем стабильнее клеточная мембрана. Количества цАМФ зависят от скорости его продукции (аденилциклаза) и инактивации (фосфодиэстераза). β-Адреностимуляторы (адреналин, алупент, эуспиран) стимулируют активность аденилциклазы, а метилксантины (эуфиллин) тормозят действие фосфодиэстеразы. То и другое действие увеличивает уровень цАМФ в клетке, и, следовательно, выход из нее гистамина и других аллергических агрессоров тормозится. Еще более активным стимулятором уровня цАМФ является 1-метил-3-изобутилксантин, который снижает активность фосфодиэстеразы.
Было бы странно, если бы в таких интимных процессах не приняли участие простагландины, имеющие особое сродство к мембране клеток. Оказалось, что простагландины E1 и Е2 повышают уровень цАМФ и тормозят выход гистамина из клеток. Кто знает, не окажутся ли простагландины в недалеком будущем наиболее физиологичными прерывателями анафилаксии?
Симптоматическая терапия может потребоваться в качестве важного дополнения к описанным выше мероприятиям. Нередко анафилактический шок сопровождается болевым и судорожным синдромом, при котором рекомендуются нейролептики и анальгетики. Если патогенетические меры не успели подействовать и наступила клиническая смерть, необходимо применить полный реанимационный комплекс.
Профилактика и лечение последствий. После того как сделано главное — нормализованы кровообращение и дыхание, необходимо заняться профилактикой и интенсивной терапией следствий анафилактического шока. Эти мероприятия можно разделить на четыре группы: 1) коррекция кислотно-щелочного состояния и водно-электролитного баланса; 2) диагностика и коррекция коагулопатии; 3) профилактика острой почечной и печеночной недостаточности; 4) профилактика миокардита, гломерулонефрита и других осложнений.
Профилактика анафилактического шока состоит в выявлении сенсибилизации к различным веществам, хотя серьезного успеха в практике не наблюдается. Учитывая, что очень часто вместо истинного анафилактического шока может развиться гистаминовый (анафилактоидный) шок, некоторые авторы [Watkins J., 1979] рекомендуют применять препарат полиамин 48/80, который вводят, чтобы определить наклонность организма к освобождению гистамина из клеток. Для премедикации пользуются блокаторами рецепторов гистамина типа хромогликата натрия, прометазина (дипразин) и циметидина (Н1- и Н2-гистаминоблокаторы).
