
- •1.Определение бас
- •2.Цели выделения бас
- •3.Первичная обработка биологического сырья.
- •3.1.Сырье для выделения бас
- •3.2.Обобщенная схема выделения бас
- •3.3.Сепарация.
- •3.4.Консервация.
- •Микроорганизмы
- •3.4.1.Охлаждение.
- •3.4.2.Консерванты
- •3.4.3.Уменьшение содержания воды
- •3.4.4.Герметизация
- •3.5.Измельчение и гомогенизация
- •3.5.1.Физические методы
- •3.5.2.Физико-химические методы
- •3.5.3.Химические методы
- •4.Экстракция
- •4.1.Классическая экстракция.
- •4.2.Сверхкритическая экстракция (sfe)
- •4.3.Твердофазная экстракция
- •5.Центрифугирование
- •5.1.Общие принципы центрифугирования
- •5.2.Дифференциальное центрифугирование
- •5.3.Зонально-скоростное центрифугирование
- •5.4.Изопикническое центрифугирование
- •5.5.Препаративные центрифуги
- •5.6.Конструкция роторов
- •5.7.Аналитические ультрацентрифуги
- •5.8.Определение молекулярных весов
- •5.8.1.Метод скорости седиментации
- •5.8.2.Метод седиментационного равновесия
- •5.8.3.Метод приближения к седиментационному равновесию
- •5.9.Исследование конформационных изменений в макромолекулах
- •5.10.Методы создания градиентов для центрифугирования
- •5.11.Извлечение продуктов из центрифужных пробирок
- •6.Мембранные технологии
- •6.1.Диализ
- •6.2.Электродиализ
- •6.3.Ультрафильтрация
- •6.4.Материалы мембран
- •6.5.Другие виды фильтрации
- •7.Буферные растворы.
- •8.Хроматография
- •8.1.Классификация хроматографических методов
- •8.1.1.Классификация по агрегатному состоянию фаз
- •8.1.2.Классификация по технике исполнения
- •8.1.3.Классификация по принципам разделения
- •8.2.Основы теории хроматографии
- •8.2.1.Общие понятия и принципы
- •8.2.2.Параметры хроматографического разделения
- •8.3.Адсорбционная хроматография
- •8.4.Распределительная хроматография
- •8.5.Эксклюзионная хроматография
- •8.6.Ионообменная хроматография
- •8.7.Аффинная хроматография
- •8.8.Обращенно-фазовая хроматография
6.Мембранные технологии
Мембранные технологии основаны на разделении смесей жидкостей или газов, а также присутствующих в них частиц на компоненты с использованием частично проницаемых мембран (рис. 18). Если размер пор достаточно мал – порядка 1-100 нм, такие мембраны

Рисунок 18. Принцип мембранных технологий.
позволяют разделять вещества по размерам молекул. Скорость прохождения молекул через мембрану зависит от давления, концентрации и температуры растворов с обеих сторон, а также проницаемости мембраны. Методы мембранных разделений различаются в зависимости от движущей силы, которая обеспечивает прохождение процесса.
6.1.Диализ
Диализ - метод разделения частиц различных размеров в жидкой смеси с помощью тонкой полупроницаемой мембраны, поры которой слишком малы для прохождения больших частиц (например, белков), но достаточно велики для прохождения растворенного вещества. Движущая сила – градиент химических потенциалов по разные стороны мембраны. Схема стандартного диализатора приведена на рисунке 19.
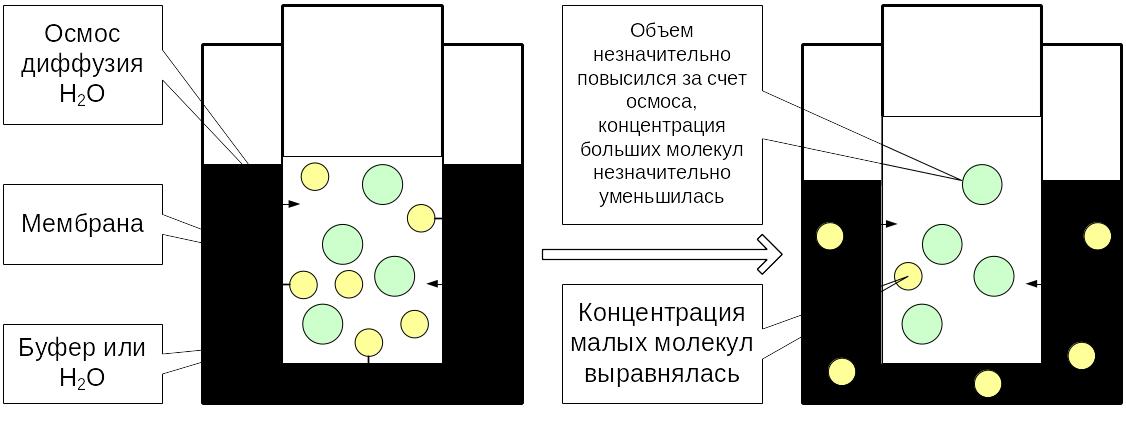
Рисунок 19. Диализ.
Материал, прошедший через мембрану, называется диализат. В процессе диализа осмотическое движение воды вызывает разбавление диализируемого раствора. В случае периодического диализатора концентрация низкомолекулярных веществ выравнивается между диализируемым и диализующим раствором. Для полного удаления этих соединений необходимо либо периодически заменят диализующий раствор или использовать проточный диализатор.
Простейшим лабораторным диализатором является сосуд большой емкости, снабженный мешалкой, в который опускают диализные мешки, заполненные образцами и герметично завязанные. Важно помнить, что мешки нельзя заполнять «под завязку» - поступающая внутрь осмотическая вода увеличивает объем внутреннего раствора и мешок может лопнуть.
Промышленные диализаторы, как правило, проточные (для интенсификации массопереноса). Диализ применяют для очистки растворов высокомолекулярных веществ от низкомолекулярных (например обессоливание) или для замены одних низкомолекулярных веществ на другие (перебуферивание). В медицине процесс диализа используется в аппарате «искусственная почка».
6.2.Электродиализ
Движущая сила – электрическое поле (рис. 20). Применяется для очистки растворов нейтральных высокомолекулярных веществ от солей.
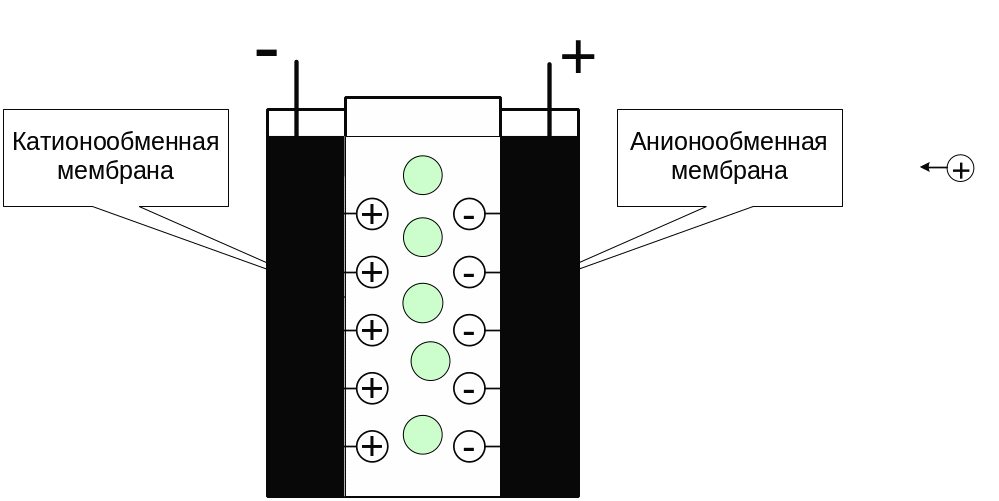
Рисунок 20. Электродиализ.
6.3.Ультрафильтрация
Движущая сила – градиент давлений. Возможны варианты как нутч-, так и друк-фильтров. Применение давления, а не разряжения, позволяет интенсифицировать процесс.
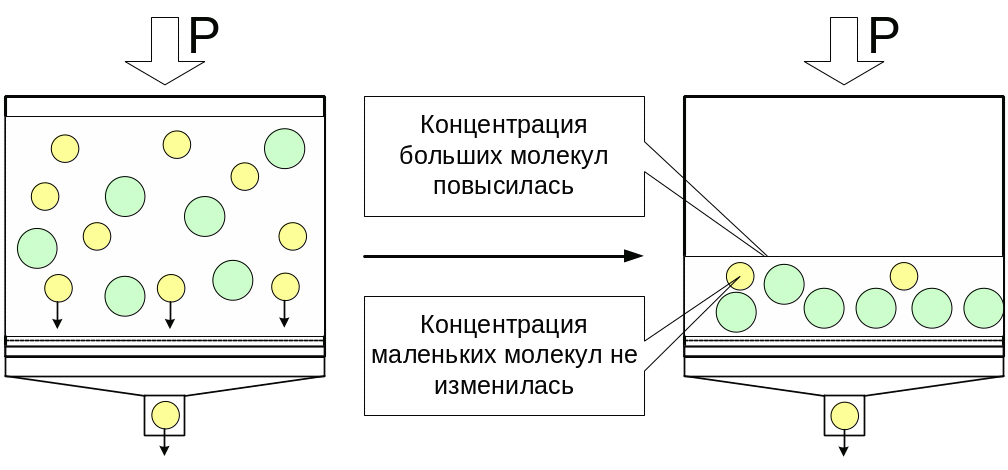
Рисунок 21. Ультрафильтрация.
Приборы для ультрафильтрации часто снабжают мешалками для того, чтобы исключить забивание пор.
Ультрафильтрацию применяют для концентрирования растворов высокомолекулярных веществ, при этом конечная концентрация низкомолекулярных компонентов в процессе ультрафильтрации не изменяется. В производстве лабильных лекарственных препаратов различные варианты ультра- и микрофильтрации применяются также для щадящей стерилизации.
6.4.Материалы мембран
Первыми материалами для мембран, способных разделять низко и высокомолекулярные соединения, были модифицированные природные полисахариды, например целлофан. Такого рода мембраны имели волокнистую структуру и большой разброс размеров пор, однако . В настоящее время применяются мембраны как из специально обработанной целлюлозы с более узким разбросом пор, так и из синтетических полимеров. Широкое применение находят «ядерные фильтры» (трековые мембраны) - микропористые фильтры, образующиеся при облучении полимерных плёнок ускоренными тяжёлыми ионами с последующим вытравливанием разрушенных участков полимера. Вдоль траектории ионов возникают сквозные каналы правильной формы. Эта технология позволяет получить высокую однородность размеров пор и возможность их варьировать в широких пределах (0,01—10 мкм). В промышленности также используют мембраны из неорганических материалов.
Мембраны характеризуются молекулярным весом веществ уже не проходящих через поры (MWCO - Molecular Weight Cut-Off), в отечественных источниках этот параметр называют просто размером пор – например «Диализный мешок, размер пор 12-14 кДа. Изготовлен из целлюлозы».
Для повышения интенсивности массопереноса мембраны могут собираться в пакеты или использоваться в виде пучков капилляров.
