
- •Оглавление
- •Основная литература
- •Дополнительная литература
- •Тематический план лекций для до
- •Тематический план лекций для озо
- •План лабораторных занятий для озо
- •Возможные темы рефератов
- •Занятие 1. Организация работ в лаборатории
- •Правила выживания в лаборатории
- •1.2. Дополнительная литература
- •1.4. Вопросы для самоконтроля
- •1.5. Задание на дом
- •Занятие 2. Вода, ее свойства и методы измерений рН
- •2.1. Физико-химические свойства и роль воды в биосфере
- •2.2. Дополнительная литература
- •2.3. Экспериментальная часть
- •2.3.1. Приготовление ацетатных буферных растворов
- •2.3.3. Электрометрические измерения
- •2.4. Вопросы для самоконтроля
- •2.5. Задание на дом
- •Занятие 3. Типы, дозировка и способы анализа растворов
- •3.2. Дополнительная литература
- •3.3. Экспериментальная часть
- •3.3.3. Сравнительный качественный анализ аминокислот
- •3.4. Вопросы для самоконтроля
- •3.5. Задание на дом
- •Занятие 4. Методы спектроскопии в анализе биомолекул и клеток
- •4.2. Дополнительная литература
- •4.3. Экспериментальная часть
- •4.3.2. Определение концентрации гемоглобина (Hb) в крови
- •4.3.3. Определение количества эритроцитов в крови с помощью турбидиметрии
- •4.4. Вопросы для самоконтроля
- •4.5. Задание на дом
- •Занятие 6. Основные приемы препаративной биохимии
- •6.2. Дополнительная литература
- •6.3. Экспериментальная часть
- •6.3.2. Разделение гемоглобина и теней эритроцитов
- •6.3.3. Высаливание белковых фракций плазмы крови и их
- •6.4.Вопросы для самоконтроля
- •6.5. Задания на дом
- •Занятие 7. Методы количественного анализа белков
- •7.2. Дополнительная литература
- •7.3. Экспериментальная часть
- •7.3.1. Количественное исследование белковых фракций крови биуретовым методом
- •7.4. Вопросы для самоконтроля
- •7.5. Задание на дом
- •Занятие 8. Деление молекулярных смесей методами хроматографии
- •8.2. Дополнительная литература
- •8.3. Экспериментальная часть
- •8.3.1. Хроматография аминокислот и пептидов на бумаге
- •8.3.2. Гель-хроматография смеси на колонке Сефадекса g – 50
- •8.4. Вопросы для самоконтроля
- •8.5. Задание на дом
- •Занятие 9. Итоговое № 1. Статическая
- •9.2. Задание на дом
- •Занятие 10. Разделение биополимеров методами электрофореза
- •10.2. Дополнительная литература
- •10.4. Вопросы для самоконтроля
- •10.5. Задание на дом
- •Занятие 11. Количественный анализ и свойства ферментов
- •11.2. Дополнительная литература
- •11.3. Экспериментальная часть
- •11.3.1. Получение разведенного препарата амилазы слюны
- •11.3.2. Количественное определение активности амилазы слюны способом Вольгемута
- •11.3.3. Выявление специфичности амилазы
- •11.3.4. Зависимость активности амилазы от температуры
- •11.3.4. Зависимость активности амилазы от величины рН инкубационной смеси. 1. В соответствии с таблицей протокола опыта,
- •11.4. Вопросы для самоконтроля
- •11.5. Задание на дом
- •Занятие 12. Брожение как модель изучения процессов метаболизма
- •12.2. Дополнительная литература
- •12.3. Экспериментальная часть
- •12.3.2. Количественное определение ортофосфата
- •12.4. Вопросы для самоконтроля
- •12.5. Задание на дом
- •Занятие 13. Углеводы. Методы определения и диагностическая роль глюкозы
- •13.2. Дополнительная литература
- •13.3. Экспериментальная часть
- •13.3.1. Глюкозооксидазный метод определения глюкозы в био-жидкостях с помощью тест-наборов фирмы Lachema (Чехия)
- •12.3.2. Определение глюкозы в крови с помощью экспресс-анализатора Эксан-г (Литва)
- •12.3.3. Определение глюкозы в крови с помощью автономного экспресс-измерителя пкг-02-«Сателлит» (Россия)
- •13.4. Вопросы для самоконтроля
- •13.5. Задание на дом
- •Занятие 14. Основы химии и метаболизма липидов и биомембран
- •14.2. Дополнительная литература
- •14.3 Экспериментальная часть
- •14.3.2. Метод определения общего холестерола в биожидкостях, с помощью тест-набора реагентов «Новохол» (зао «Вектор-Бест»)
- •14.4. Вопросы для самоконтроля
- •14.5. Задание на дом
- •Занятие 16. Основы метаболизма азотистых соединений
- •Варианты азотистого баланса
- •Потребность животных в аминокислотах (По р. Марри и др., 1993, с изменениями)
- •16.2. Дополнительная литература
- •16.3 Экспериментальная часть
- •16.3.1. Определение количества мочевины в биожидкостях с помощью тест-набора фирмы Lachema (Чехия)
- •16.3.2. Определение концентрации креатинина в биожидкостях с помощью тест-набора фирмы Lahema (Чехия)
- •16.4. Вопросы для самоконтроля
- •16.5. Задания на дом
- •Занятие 17. Семинар по интеграции метаболизма
- •17.2. Темы реферативных сообщений
- •17.3. Обсуждение рефератов
- •17.4. Задания на дом
- •Занятие 18. Контрольные вопросы к итоговому № 2. Способы управления метаболизмом
- •Приложение
16.3.2. Определение концентрации креатинина в биожидкостях с помощью тест-набора фирмы Lahema (Чехия)
Креатинин – ангидрид креатина, содержащийся в крови, мозге и особенно в мышцах, как в форме транспортного макроэрга - креатинфосфата, так и в свободном состоянии. Следы креатина есть в нормальной моче, но в мышцах, он неферментативно и необратимо распадается до креатинина. Эндогенный креатинин экскретируется в почках клубочковой фильтрацией и секрецией в микротрубочках, со скоростью ~ на 20 % больше клиренса инулина.
Его суточная экскреция удивительно пропорциональна массе мускулатуры (табл. 16.4) и составляет в моче женщин – 53-97 мкмоль/л и 61-115 мкмоль/л у мужчин.
Таблица 16.4
Возрастные нормы содержания (мг/кг) в суточной моче
(по Murray R.K. et al., 1990)

Обмен этих соединений азота связан с аминокислотой глицином и незаменимыми для консументов, аргинином и метионином (рис. 16.2).
Принцип метода: В щелочной среде креатинин взаимодействует с пикриновой кислотой, давая оранжево-красную окраску (реакция Jaffe), которую измеряют фотометрически. Метод малоспецифичен, т.к. восстановители типа глюкозы, вещества с активной метиленовой группой, кетокислоты, мочевина, мочевая кислота и пигменты: билирубин, Hb – могут завышать результаты. Поэтому определение ведут после осаждения белков биожидкостей.
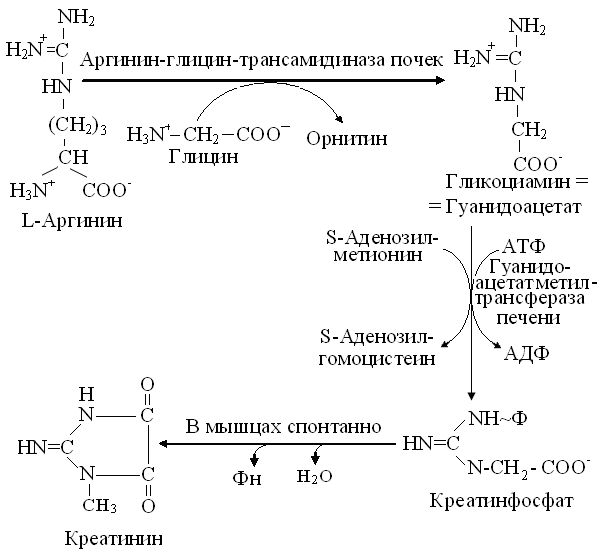
Рис. 16.2. Схема обмена креатина и креатинина
Ход работы: 1. В соответствии с таблицей, внести в 3 пронумерованных центрифужных пробирки:
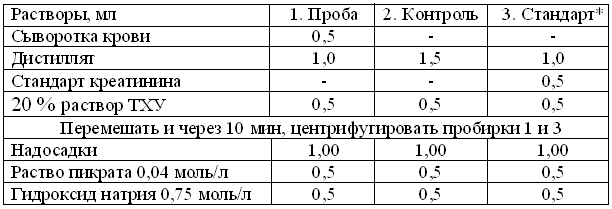
* - В связи с необходимостью экономии стандартного раствора креатинина, пробу 3 – Стандарт, с концентрацией креатинина 177 мкмоль/л и добавкой СА, на группу студентов, выполняет лишь одна рабочая пара.
2. Растворы перемешать и точно через 20 мин фотометрировать при λ 490 нм, в кювете толщиной 10 мм против контроля, абсорбцию пробы и стандарта.
3. По формуле: Креатинин, мкмоль/л = 177 х А опыта/А стандарта,
рассчитать концентрацию креатинина в исследуемой сыворотке.
Нормальное содержание креатинина в плазме крови здоровых людей: 0,7-1,5 мг/дл или 60-132 мкмоль/л. Оно может повышаться при приеме ряда лекарств и острых и хронических воспалительных болезнях почек.
16.4. Вопросы для самоконтроля
16.4.1. Объясните, почему азот концентрируется не в соединениях, а в атмосфере Земли?
16.4.2. Зачем и какие соединения азота нужны организмам?
16.4.3. Что такое синтрофия и чем она вызвана?
16.4.4. Что вы знаете о генах азотфиксации?
16.4.5. Какие соединения азота способны усваивать клетки-консументы?
16.4.5. Что такое витамины?
16.4.6. Каким показателем оценивают динамические состояния организмов и популяций?
16.4.7. Объясните понятия заменимые и незаменимые аминокислоты и, какова их роль с позиций питания человека?
16.4.8. Объясните причины зависимости консументов от внешних источников аминокислот.
16.4.9. В чем заключается полноценность пищевых белков для человека?
16.4.10. Что общего у сериновых протеиназ, входящих в системы пептидгидролаз ЖКТ, свертывания крови и комплемента?
16.4.11. Назовите основные источники аминокислот для клеток животных.
16.4.12. Что такое остаточный азот крови и зачем нужен этот критерий?
16.4.13. Какую роль играет определение мочевины в крови?
16.4.14. Есть ли смысл определять количество мочевины в моче и, при каких условиях?
16.4.15. Что такое креатинин и, какую информацию может дать его определение в плазме крови?
