- •1 Вопрос
- •Вопрос 12:Фруктозо-1,6-дисфосфатный путь (гликолиз)
- •Вопрос 13: Окисление пирувата
- •Вопрос 15: Метаболизм-обмен веществ.
- •Катаболизм-распад,получение энергии Амфиболизм-промежуточный обмен Анаболизм-построение, затрата энергии
- •1) Эндоспоры
- •5) Формирование покровов споры и экзоспориума
- •2) Экзоспоры
- •3) Миксоспоры
- •4) Цисты
- •8. Основные типы брожения:
- •25. Круговорот углерода в мире микроорганизмов. Зависимость судьбы углерода от наличия кислорода в окружающей среде. Полное и неполные окисления. Автотрофы и гетеротрофы. Метаногены, метилотрофы
- •Превращение различных форм азота микроорганизмами. Аммонификация белков. Ассимиляционная и диссимиляционная нитратредукция. Аммонификация нитрата. Азотфиксация. Нитрификация.
- •27. Нитратное дыхание. Микроорганизмы, ведущие диссимиляционную нитратредукцию. Механизмы реакций и ферменты процесса нитратного дыхания. Условия процесса. Энергетические возможности процесса.
- •1 Окисление аммиака до нитрит-аниона
- •2 Окисление нитрит-аниона до нитрат-аниона
- •32. Симбиоз в мире микроорганизмов. Виды симбиоза. Примеры комменсализма, мутуализма, паразитизма. Облигатные и факультативные симбионты.
1 Окисление аммиака до нитрит-аниона
Первая стадия — окисление аммиака до нитрит-аниона, которое осуществляют нитрозные бактерии родов Nitrosomonas, Nitrosococcus и Nitrosospira (ранее выделялись также рода Nitrosolobus, Nitrosovibrio, но сейчас их представители включены в Nitrosospira) по следующему механизму:
NH3 + O2 + НАДН2 → NH2OH + H2O + НАД+
NH2OH + H2O → HNO2 + 4H+ + 4e−
1/2O2 + 2H+ + 2e− → H2O
Предполагается, что на первом этапе субстратом является именно аммиак, а не аммоний, поэтому процесс не идёт в кислой среде. Ферментом для первой реакции служит аммиакмонооксигеназа, фермент с очень низкой субстратной специфичностью, окисляющая также метан, оксид углерода, циклогексан, фенол, бензиловый спирт, однако со скоростью на порядки ниже. Гидроксиламин ингибирует работу фермента. В бесклеточных экстрактах восстановителем может служить НАД(Ф)·H, однако в клетке его роль, скорее всего, выполняет один из компонентов дыхательной цепи.
Следующую реакцию осуществляет гидроксиламиноксидоредуктаза, расположенная в периплазме. Окислителем в них служит цитохром c, с него электрон передаётся на убихинон и далее в дыхательную цепь, на цитохромоксидоредуктазу и, в конечном итоге, на кислород. При этом запасается энергия в виде трансмембранного протонного потенциала.
Образование НАД(Ф)·H для фиксации углекислого газа в цикле Кальвина происходит путём обратного переноса части электронов.
2 Окисление нитрит-аниона до нитрат-аниона
Вторая стадия — окисление аниона азотистой кислоты до аниона азотной, производимое нитратными бактериями (почвенный род Nitrobacter и водные Nitrospira, Nitrococcus, Nitrospina). Процесс протекает в одну реакцию:
NO2− + H2O → NO3− + 2H+ + 2e−
катализируемую нитрит:нитрат-оксидоредуктазой, локализованной в ЦПМ. Далее электроны передаются на цитохромы дыхательной цепи, в которой единственным пунктом транслокации протонов является цитохромоксидаза.
Образование НАД(Ф)·H для фиксации углекислого газа также происходит путём обратного переноса электронов.
Организмы
Нитрозных и нитритных бактерий ранее выделяли в семейство Nitrobacteraceae, сейчас с развитием геносистематики их рода разнесены по разным подклассам протеобактерий. Оптимальная для их развития температура 25—30 °C и pH 7,5—8,0. В кислой среде процесс не идет. Все эти бактерии — грамотрицательные хемолитоавтотрофы, использующие энергию окисления соединений азота для синтеза органических веществ из углекислого газа. Некоторые из них способные переключаться на хемоорганогетеротрофный метаболизм, однако ни одного хемолитогетеротрофа среди данных организмов найдено не было. Морфологически эти группы разнообразны, в большинстве своем мелкие, подвижные, с полярным или перитрихиальным жгутикованием. Окисление они проводят на цитоплазматической мембране.
Гетеротрофная нитрификация
Особо выделяют гетеротрофную нитрификацию, происходящую у многих бактерий и грибов и связанную с окислением аммиака и азота органических соединений без использования полученной энергии, попутно с окислением органического вещества и, предположительно, посредством кислорода, образуемом при разложении пероксида водорода. Удельная активность этого процесса на 2-4 порядка ниже, чем в случае автотрофной нитрификации, однако именно с ним связано происхождение чилийской селитры а также вся нитрификация в почвах и водоемах с низкими значениями pH.
Процесс нитрификации является конечной стадией минерализации азотсодержащих органических загрязнений. Наличие нитратов в очищенных сточных водах служит одним из показателей степени их полной очистки; поэтому необходимо применять такие очистные сооружения, которые обеспечили бы оптимальные условия для жизнедеятельности нитрифицирующих бактерий
Справка. Для легкого чтения.
Известно, что аммоний является более
предпочтительной формой азота для питания растений, поскольку нитраты
необходимо восстанавливать в аммоний, что требует дополнительных затрат
энергии. Однако это преимущество аммония часто не является
определяющим для растений, так как интенсивность ассимиляции аммония или нитра-
тов зависит еще от свойств почвы (рН, содержания катионов, соотношения
аммония и нитратов), фазы развития и особенностей биологии конкретных
видов растений. На слабокислых почвах более эффективны нитратные
удобрения, на нейтральных почвах - аммиачные удобрения в связи с отсутствием
негативного эффекта от их быстрого подкисления. В начальные фазы роста
растений оптимальным источником азота являются нитраты, а при
достаточном развитии листовой поверхности и, соответственно, высоком уровне
синтеза углеводов - аммиачный азот, так как устраняется накопление в клетках
растений аммиака в токсичных концентрациях.
Во многих природных экосистемах, особенно находящихся на последних
стадиях сукцессии (хвойные леса, луговые степи), аммонийный азот в почвах
преобладает над нитратным, а растения адаптированы к преимущественному
усвоению аммонийного азота.
В агроэкосистемах большинство сельскохозяйственных культур
энергичнее потребляют из почвы нитратный азот. Одна из причин этого - более
активное поступление питательных элементов в форме катионов в растения
при ассимиляции нитратов и изменение соотношения аммония и нитратов
при окультуривании почв. Улучшение физико-химических свойств,
происходящее при окультуривании почв, обусловливает повышение доли нитратов в
запасах минерального азота - с 20% в почвах с низким плодородием до 60% в
хорошо окультуренных почвах, а при внесении азотных удобрений и до 90%.
В большинстве случаев это обусловлено не столько использованием
нитратных удобрений, сколько интенсификацией нитрификации в почвах, поскольку оптимумы условий для возделывания сельскохозяйственных культур и процесса нитрификации сходны. Поэтому неслучайно, что высокую
нитрифицирующую активность уже давно используют как один из показателей
хорошего плодородия почв.
Вместе с тем избыточное образование нитратов в почвах агроэкосистем, а
в ряде случаев и в почвах природных экосистем, является причиной
многочисленных проблем, которые непосредственно касаются здоровья человека и
устойчивого функционирования биосферы. Нитраты легко теряются из
почвы - вымываются из почвенных горизонтов в грунтовые воды или
улетучиваются после восстановления микроорганизмами до N20 и N2 при денитрификации. Газообразные потери азота в форме N20 происходят и
непосредственно в ходе нитрификации. Поступление нитратов в подземные воды и
водоемы ухудшает качество питьевой воды и вызывает эвтрофикацию
водоемов, высокое содержание нитратов в аэрозолях приводит к кислотным
дождям, респираторным заболеваниям и другим негативным последствиям, а
возрастание эмиссии N20 из почв усиливает парниковый эффект и
разрушение озонового слоя атмосферы.
Накопление нитратов в питьевой воде и растениях (особенно овощных и
кормовых) и передача их по пищевым цепям вызывает серьезные
медико-биологические проблемы. Чрезмерное поступление нитратов в организм
человека нарушает проницаемость мембран эритроцитов, повышает количество
холестерина в крови, снижает резистентность организма к действию
мутагенных и канцерогенных агентов. Образующиеся из нитратов нитриты и окись
азота вызывают метгемоглобинемию, нитрозосоединения обладают
канцерогенным действием.
30. Превращение микроорганизмами соединений серы. Десульфуризация белков. Ассимиляционная и диссимиляционнаясульфатредукция. Окисление восстановленных соединений серы. Накопление микроорганизмами элементарной серы. Механизмы процессов и основные группы микроорганизмов.
S=>в организмах всегда восстановленная, и находится в виде сульфгидрильных групп (HS) и дисульфатоф –S-S-/
Содержатся только в аминокислотах: метионин, цистеин, гомоцистеин.
В природе больше в окисл. Состоянии.
Живые организмы должны уметь восстанавливать окисленные соединения.
Сульфатредукция(почти все бактерия, растения, грибы)
SO4 (2-) (сульфат ион)–крайняя степень окисленности, является конечным акцептором электронов(принимает). Идет с затратой АТФ. Процесс анаэробный не требует O2.
Бывают:
1.ассимиляционная (-HS –S-S-)
2.диссимиляционная (H2Sбудет выделяться)
Оба процесса ведут к полному восстановлению серы.
SO4(2-) сульфат=>SO3(2-) сульфит=>S3O6 (2-) тритионат=>S2O3(2-) тиосульфат=>H2S (S2-) сероводород.
8[H]+SO4(2-)=>H2S+2H2O+2OH(-) среда подщелачивается.
[H]-лактат, бутират, ацетат, формиат, пропионат, этанол, молекулярный Н2 для диссимиляционнойСульфатредукции..
Диссимиляционная СР.
Не могут использовать сахара высоко молекулярные субстраты.Микроорганизмы используют-низкомолекулярную органику и неорганику.
Десульфуризация
Окисление органических веществ анаэробными бактериями за счѐт восстановления сульфатов. Во всех системах, содержащих органические вещества и сульфаты и не содержащих свободного кислорода, развивается деятельность десульфуризирующих бактерий (десульфуризаторы), отнимающих кислород у сульфатов для окисления органического вещества. Пищей для этих микроорганизмов служат многие органические соединения растений и животных, нефти, битумы, рассеянные в осадочных породах, тяжѐлые углеводороды, начиная с гексана, и другие соединения. Десульфуризаторы развиваются при обычных температурах (но они установлены и в горячих водах) в солончаках, илах морей и солѐных озѐр, в подземных водах, местами и в морской воде. В результате десульфуризации в почвах, илах и подземных водах накапливается сероводород, возникает восстановительный сероводородный барьер.
Почти все бактерии, грибы и зеленые растения способны использовать в качестве источника серы сульфат. Они получают сульфид, необходимый для синтеза серусодержащих аминокислот, путем «ассимиляционнойсульфатредукции». Первая реакция на этом пути является общей как для диссимиляционного, так и для ассимиляционного восстановления сульфата. Далее при диссимиляционнойсульфатредукции происходит прямое восстановление активированного сульфата, а при ассимиляционной следует еще одна реакция активации. Восстановление сульфата в клетке начинается с его активации, на которую непосредственно затрачивается энергия АТР
Отличияд.СР от а.СР
Основные отличия диссимиляционнойсульфатредукции от ассимиляционной сводятся к следующему: диссимиляционное восстановление сульфата присуще только узкому кругу высокоспециализированных эубактерий; активность процесса диссимиляционнойсульфатредукции намного выше, чем ассимиляционной, следствием чего является накопление в среде больших количеств H2S; наконец, различны механизмы обоих процессов.
|
|
|
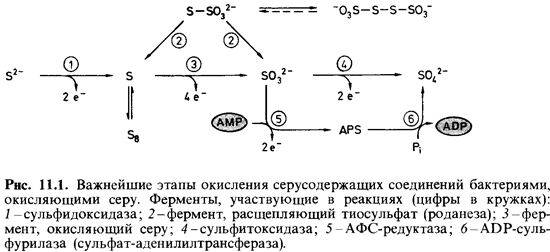
Окисление восстановленных соединений серы Способностью получать энергию в результате окисления восстановленных соединений серы обладают грам-отрицательные бактерии с полярно расположенными жгутиками, объединяемые в род Thiobacillus. Недавно была открыта спирилла с полярными жгутиками (Thiomicrospira), а также неподвижная термофильная бактерия Sulfolobus (табл. 11.3). Большинство тиобацилл может окислять различные соединения серы, образуя в качестве конечного продукта сульфат: Т. thiooxidans образует большие количества серной кислоты и хорошо переносит низкие значения рН среды (клетки не теряют жизнеспособности даже в 1 н. растворе серной кислоты). Такое подкисление среды во многих случаях полезно для нас. Чтобы уменьшить щелочность, в известковые почвы вносят элементарную серу; в результате образуемая тиобациллами серная кислота перводит карбонат кальция в более растворимый сульфат кальция, который вымывается из почвы. Этапы окисления соединений серы. Трудность изучения отдельных стадий этого процесса связана с тем, что в водных растворах сероводород и сера окисляются и небиологическим путем, хотя и медленно. На рис. 11.1 представлены наиболее важные реакции. Желтая элементарная сера (серный цвет) представляет собой кольцо из восьми атомов (S8); она плохо растворима в воде (0,176 мг/л). Как полагают, электроны, освобождающиеся при окислении сульфита до сульфата, поступают в дыхательную цепь на уровне цитохрома с. По крайней мере некоторые тиобациллы {Thiobacillusthioparus, T. denitrificans) способны использовать выделяющуюся при этом окислении энергию для фосфорилирования на уровне субстрата.
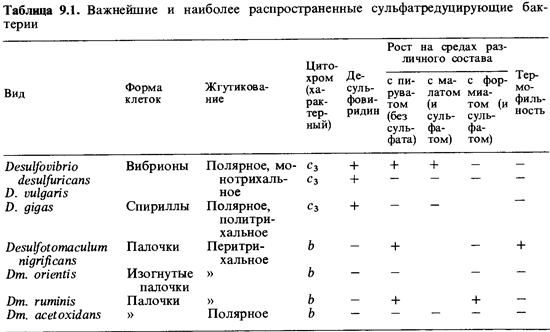
Реакции (1) и (2) противоположны реакциям диссимиляционного восстановления сульфата (рис. 9.3). Нитчатые и другие серобактерии. В местах, где в осадках стоячих и медленно текущих вод образуется H2S, часто можно обнаружить на черной поверхности ила бесцветные нитчатые серобактерии Beggiatoa, Thiothrix и Thioploca (см. рис. 2.44 и 3.17), а также крупные одноклеточные формы Achromatium oxaliferum и Thiovulum (см. рис. 2.44). На Beggiatoa С. Н. Виноградский проводил свои эксперименты, которые легли в основу представления о хемолитоавтотрофии. Однако получить хотя бы одну из этих «классических серобактерий» в чистой культуре и подробно изучить их физиологические и биохимические особенности до сих пор не удалось1. Неудача попыток выращивать их в чистой лабораторной культуре связана, очевидно, с особыми требованиями этих бактерий. Наряду с сероводородом им нужен молекулярный кислород, но они переносят его присутствие только в самых малых концентрациях (т.е. являются микроаэрофилами). Для создания таких оптимальных условий необходимы особые экспериментальные приемы и много терпения. Сероводород как основа бессветовой экосистемы. Для жизни всех высших гетеротрофных организмов необходима биомасса, создаваемая с помощью фотосинтеза. Однако несколько лет назад было найдено исключение из этого правила. Систематика. Сульфатредуцирующие бактерии-это физиологическая группа, для которой характерна способность к образованию сероводорода из сульфата (табл. 9.1). Донорами водорода служат простые низкомолекулярные соединения, образующиеся при анаэробном разложении биомассы, главным образом целлюлозы: лактат, ацетат, пропионат, бутират, формиат, этанол, высшие жирные кислоты и молекулярный во-
дород. По степени усвоения органических кислот различают две группы сульфатредуцирующих бактерий: 1. Бактерии, относящиеся к первой группе, окисляют донор водорода не полностью и выделяют уксусную кислоту. Таковы виды спорообра-зующего рода Desulfotomaculum (D.nigrificans, D. orientis и D. ruminis) и неспорообразующего рода Desulfovibrio (D. vulgaris, D.desulfuricans, D. gigas, D. thermophilus и другие). 2. Вторая группа включает роды и виды, часть которых может расти, используя спирты, ацетат, высшие жирные кислоты или бензоат, а другие способны даже к хемоавтотрофному росту в присутствии водорода и формиата. К этой группе относятся спорообразователи (Desulfotomaculum acetoxidans), а также неспорообразующие палочки(Desulfobacter), кокки (Desulfococcus), сардины (Desulfosarcina), нитевидные формы, передвигающиеся путем скольжения (Desulfonema), и некоторые другие бактерии. Восстановление сульфата. Почти все бактерии, грибы и зеленые растения способны использовать в качестве источника серы сульфат. Они получают сульфид, необходимый для синтеза серусодержащих аминокислот, путем «ассимиляционнойсульфатредукции». Первая реакция на этом пути является общей как для диссимиляционного, так и для ассимиляционного восстановления сульфата. Далее при диссимиляционнойсульфатредукции происходит прямое восстановление активированного сульфата, а при ассимиляционной следует еще одна реакция активации. Восстановление сульфата в клетке начинается с его активации, на которую непосредственно затрачивается энергия АТР (рис. 9.3); с помощью
АТР-сульфурилазы (сульфатаденилтрансферазы) дифосфатный остаток АТР обменивается на сульфат: ATP + S04 ^ Аденозин-5:фосфосульфат + PPj Дифосфат (пирофосфат) расщепляется пирофосфатазой. Продуктом активации является аденозин-5-фосфосульфат (АФС). Последующие реакции могут быть различными. На пути ассимиляционного восстановления сульфата АФС с помощью АФС-киназы и АТР фосфорилируется у ряда организмов с образованием фосфоаденозинфосфосульфата (ФАФС); лишь этот вдвойне активированный сульфат восстанавливается сначала до сульфита, а затем до сульфида. При диссимиляционнойсульфатредукции АФС с помощью АФС-редуктазы восстанавливается до сульфита, что сопровождается образованием AMP. Восстановление сульфита до сульфида происходит, видимо, у разных бактерий по-разному. С помощью сульфитредуктазы сульфит прямо восстанавливается до сульфида (на что затрачивается 6 электронов) без образования промежуточных продуктов. В такого рода восстановлении как и в ассимиляционной сульфитредукции - участвуют, по-видимому, железопорфириновые соединения (десульфовиридин, десульфору-бидин). Второй механизм состоит в последовательном трехступенчатом восстановлении сульфита с образованием промежуточных продуктов, таких как тритионат и тиосульфат (рис. 9.3). Предполагается, что электроны для восстановления сульфита доставляются цитохромами (у одних бактерий -цитохромом Ь, у других-цитохромом с). Фосфорилирование, сопряженное с переносом электронов. Предположение отакого рода фосфорилировании у сульфатредуцирующих бактерий основано на данных о наличии цитохромов и железосерных белков в плазматических мембранах, а также о высоком выходе энергии. Ци-тохром с3 обладает, по сравнению с другими цитохромами, весьма низким окислительно-восстановительным потенциалом (Јj = - 205 мВ) и находится на внешней поверхности мембраны или в периплазматиче-ском пространстве. У хорошо изученных видов сульфатредуцирующих бактерий была обнаружена конститутивная гидрогеназа (Н2 :цитохром-с3-оксидо-редуктаза), с помощью которой Н2 может как поглощаться и активироваться, так и выделяться в окружающую среду. Некоторые сульфатре-дуцирующие бактерии растут в присутствии Н2 и сульфата как единственных источников энергии. Способность к восстановлению сульфата с помощью Н2 и к образованию больших количеств сероводорода, не связанному с заметным ростом, вероятно, характерна для большинства сульфатредуцирующих бактерий. Перенос электронов с Н2 как донора, сопровождающийся восстановлением 1 моля сульфата до 1 моля сульфида, вероятно, сопряжено с регенерацией 3 молей АТР, из которых, однако, 2 моля расходуются на активацию сульфата. Окисление органических субстратов. Классические сульфатредуци-рующие бактерии, которые были известны до 1975 года (например, Desulfovibrio vulgaris), окисляют органические субстраты не до Н20 и С02, а до уксусной кислоты. Эти бактерии не имеют полного цикла трикарбоновых кислот. Однако недавно было выделено несколько видов, способных окислять ацетат, высшие жирные кислоты и бензоат. Ассимиляция органических субстратов. Энергия, получаемая сульфат-редуцирующими бактериями в результате окислительногофосфорили-рования, делает возможной ассимиляцию органических веществ (органических кислот, аминокислот и т.п.). Некоторые штаммы способны синтезировать клеточные компоненты из ацетата и С02, если донором водорода служит Н2. Организмы, ассимилирующие органические вещества в процессе окисления неорганического донора электронов, можно называть хемолитогетеротрофами. Фиксация С02 в цикле Кальвина у данной группы микроорганизмов не обнаружена.
|
31.Основные понятия медицинской микробиологии. Патогенность, вирулентность. Важнейшие группы патогенных микроорганизмов. Профилактика заболеваний и борьба с инфекциями. Заболевания, вызываемые грибами, бактериями, вирусами, прионами.
Патогенность-способность паразита вызывать заболевание, (свойство вида). Некоторые бактерии одного рода могут быть непатогенными и патогенными(Bacillus, Pseudomonas).
Вирулентность-степень патогенности, (свойство штамма). Есть МКО, у которых вирулентность низкая и они никак не проявляются.
Вирулентность:1.Инвазивность - способность размножаться в организме хозяина, B.antracis.
2. Токсигенность - способность МКО производить токсины в организме хозяина, повреждать ткани, Corynebacterium diphteriae.
Инфекция – передача МКО от одной особи к другой.
Инфекция + патологический процесс = заболевание.
Проникновение МКО:1.с пищей и водой, 2. Аэрозольный, 3. Прямой контакт, 4. Раневая инфекция, 5. Укус животного.
Инфекция:1.Поражение слизистых. Если не нарушена норм микрофлора, то все норм. Если поврежден эпителий, то прыщи, язвы. Поверхностная колонизация эпителия. 2. Проникновение внутрь эпителия. Всегда патологический процесс. Механизм проникновения основан на фагоцитозе, Shigella disenteriae, Vibrio cholera.3. Проникновение в глубокие ткани. Brucella (бруцилёз)
Токсины: 1.Эндотоксины (клетки МКО). ЛПС на поверхности клеток вызывают иммунную реакцию. В основном гр-. Комплексы ЛПС с белками. Нечувствительны к нагреванию. 2. Экзотоксины – секретируемые вещества, которые выделяются из микробной клетки, выделяются в культуральную жидкость при культивировании. Инактивируются при повышении температуры. Токсигенность кодируется плазмидами.
Заболевания, вызываемые грибами: Candida ablicans – представители нормальной микрофлоры, причина микоза – лечение антибиотиками других заболеваний, которые подавляют нормальную микрофлору бактерий. Если не лечить - системные микозы, молочница.
Заболевание, вызываемые бактериями: Salmonella typhi(брюшной тиф), S. Typhimurium (Паратиф), Vibrio cholerae (холера), Corynebacterium diphteriae (дифтерия), Micobactetium tuberculosis (туберкулез), Yersinia pestis (чума), Baccillus antracis (сибирская язва), Streptococi pneumonia (пневмония), Brucella abortis (бруцеллёз), neisseria gonurheae (гонорея), Treponema pallidum(сифилис), Clostridium tetani (столбняк).
Заболевание, вызываемые вирусами: Ретровирусы( ВИЧ), Herpesvirus (герпеса, ветрянка), Tobacovirus(ВТМ), Грипп, гепетит, Корь, Краснуха, Вирус папилломы человека, оспа, ОРЗ(аденовирусы), полиомиелит, энцефалит.
Заболевание, вызываемые прионами: Бешенство коров, губчатая энцефалопатия, куру, фатальная семейная бессонница.