
- •1. Предмет коллоидной химии
- •1.1. Основные понятия и определения
- •1.2. Классификация дисперсных систем
- •1.3. Поверхностное натяжение. Свободная поверхностная энергия
- •1.3.1. Поверхностное натяжение индивидуальных жидкостей
- •1.3.2. Поверхностное натяжение многокомпонентных растворов
- •2. Поверхностные явления
- •2.1. Классификация поверхностных явлений
- •2.2. Адсорбция
- •2.2.1. Основные понятия и определения
- •2.2.2. Природа адсорбционных сил
- •2.2.3. Теории адсорбции
- •Теория мономолекулярной адсорбции Ленгмюра
- •1 Моль – частиц,
- •Теория полимолекулярной адсорбции Поляни (потенциальная теория адсорбции)
- •Теория полимолекулярной адсорбции бэт
- •2.2.4. Уравнения адсорбции
- •Фундаментальное адсорбционное уравнение Гиббса
- •Закон Генри
- •Уравнение Фрейндлиха
- •2.2.5. Адсорбция на границе жидкость-газ Понятие о пав
- •Ориентация молекул пав в поверхностном слое
- •Изотермы поверхностного натяжения и адсорбции пав
- •Физический смысл констант уравнения Шишковского
- •Поверхностная активность. Правило Дюкло – Траубе
- •Методы определения величины адсорбции
- •2.2.6. Адсорбция на твердой поверхности Особенности адсорбции на поверхности твердых тел
- •Классификация твердых адсорбентов
- •Требования, предъявляемые к адсорбентам
- •Адсорбция газов. Капиллярная конденсация
- •Адсорбция из жидких сред
- •1. Молекулярная адсорбция
- •2. Ионная адсорбция
- •3. Ионообменная адсорбция
- •Применение адсорбционных процессов
- •2.3. Адгезия и смачивание
- •2.3.1. Основные понятия
- •2.3.2. Работа адгезии и когезии
- •2.3.3. Смачивание
- •2.3.4. Связь между работой адгезии и краевым углом смачивания
- •3. Электрические свойства дисперсных систем. Электрокинетические явления
- •3.1. Возникновение электрического заряда на поверхности раздела фаз
- •3.2. Современные представления о строении дэс
- •3.3. Строение мицеллы гидрофобного золя
- •3.4. Факторы, влияющие на электрокинетический потенциал
- •3.4.1. Влияние температуры
- •3.4.2. Влияние электролитов
- •Влияние индифферентных электролитов
- •Влияние неиндифферентных электролитов
- •3.4.3. Влияние рН среды
- •3.4.4. Влияние природы дисперсионной среды
- •3.5. Электрокинетические явления
- •3.5.1. Электрофорез
- •3.5.2. Потенциал седиментации
- •3.5.3. Электроосмос
- •3 .5.4. Потенциал течения
- •4. Устойчивость и нарушение устойчивости лиофобных золей
- •4.1. Седиментационная устойчивость
- •4.2. Агрегативная устойчивость и коагуляция
- •Теория устойчивости гидрофобных золей длфо
- •Факторы, определяющие агрегативную устойчивость коллоидных систем
- •4.3. Коагуляция гидрофобных дисперсных систем
- •4.3.1. Коагуляция золей электролитами
- •Концентрационная коагуляция
- •Нейтрализационная коагуляция
- •Явление неправильных рядов
- •4.3.2. Кинетика коагуляции
- •Константа скорости быстрой коагуляции
- •Константа скорости медленной коагуляции
- •5. Свойства дисперсных систем
- •5.1. Оптические свойства дисперсных систем
- •5.1.1. Рассеяние света
- •Теория светорассеяния Рэлея
- •5.1.2. Поглощение света и окраска золей
- •5.1.3. Оптические методы исследования коллоидных растворов
- •5.2. Молекулярно-кинетические свойства дисперсных систем
- •5.2.1. Броуновское движение
- •5.2.2. Диффузия
- •5.2.3. Осмос
- •5.3. Получение дисперсных систем
2.3.3. Смачивание
Смачивание – один из видов адгезии, который реализуется при взаимодействии жидкости с твердой или более плотной жидкой фазой при наличии одновременного контакта трех несмешивающихся фаз, одна из которых газ (воздух).
Рассмотрим явление смачивания на примере капли жидкости (Ж), нанесенной на поверхность твердого тела (Т). При этом возможны следующие случаи.
1 .
Капля жидкости самопроизвольно
растекается по поверхности, пока не
покроет её всю или пока слой жидкости
не станет мономолекулярным. Это полное
смачивание. Пример: капля воды на
обезжиренном стекле (рис. 24а).
.
Капля жидкости самопроизвольно
растекается по поверхности, пока не
покроет её всю или пока слой жидкости
не станет мономолекулярным. Это полное
смачивание. Пример: капля воды на
обезжиренном стекле (рис. 24а).
2. Капля жидкости на твердой поверхности самопроизвольно принимает почти сферическую форму. При этом твердая поверхность не смачивается жидкостью, наблюдается полное несмачивание. Пример: капля ртути на неметаллической поверхности (рис. 24в).
3. Между этими крайними случаями наблюдаются различные промежуточные случаи, когда поверхность частично смачивается жидкостью (рис. 24б).
Форма капли жидкости на твердой
поверхности зависит от соотношения
значений межфазовых поверхностных
натяжений на границе раздела следующих
фаз: твердое тело – газ
![]() ,
жидкость – газ
,
жидкость – газ
![]() и твердое тело – жидкость
и твердое тело – жидкость
![]() .
Линию соприкосновения всех трех
поверхностей раздела называют линией
смачивания. Замкнутая линия смачивания
образует периметр смачивания.
.
Линию соприкосновения всех трех
поверхностей раздела называют линией
смачивания. Замкнутая линия смачивания
образует периметр смачивания.
К оличественной
мерой смачивания служит краевой угол
смачивания
оличественной
мерой смачивания служит краевой угол
смачивания
![]() – угол между твердой поверхностью и
касательной, проведенной к поверхности
капли в точке соприкосновения трех фаз.
Его измеряют со стороны жидкой фазы
(рис. 25).
– угол между твердой поверхностью и
касательной, проведенной к поверхности
капли в точке соприкосновения трех фаз.
Его измеряют со стороны жидкой фазы
(рис. 25).
У становим
связь краевого угла смачивания с
межфазовыми поверхностными натяжениями.
Равновесие
капли определяется одновременным
воздействием трех поверхностных
натяжений, которые на рис. 26 показаны в
виде векторов, направленых по касательной
к соответствующей поверхности. Два из
них (
и
)
действуют на поверхности твердого тела
в противоположных направлениях. Сила
направлена к поверхности под углом
.
становим
связь краевого угла смачивания с
межфазовыми поверхностными натяжениями.
Равновесие
капли определяется одновременным
воздействием трех поверхностных
натяжений, которые на рис. 26 показаны в
виде векторов, направленых по касательной
к соответствующей поверхности. Два из
них (
и
)
действуют на поверхности твердого тела
в противоположных направлениях. Сила
направлена к поверхности под углом
.
Используя геометрическое равновесие сил, получаем
![]() .
.
Решаем уравнение относительно
![]()
![]() – уравнение Юнга. (38)
– уравнение Юнга. (38)
Проанализируем уравнение Юнга:
если
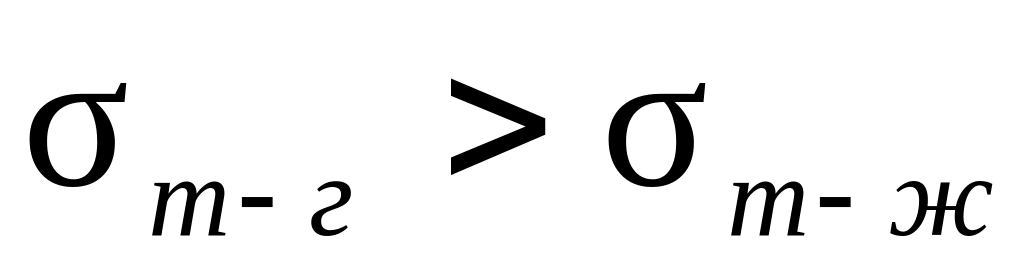 ,
,
 ,
,
 – поверхность смачивается жидкостью;
Капля жидкости растекается,
закрывая часть твердой поверхности.
За счет этого происходит частичная
замена поверхности с большей поверхностной
энергией
на поверхность с меньшей поверхностной
энергией
,
следовательно, запас энергии в системе
уменьшится. С другой стороны, при
растекании капли увеличивается площадь
поверхности жидкость – газ, что приводит
к увеличению свободной энергии системы.
Отсюда следует вывод:
– поверхность смачивается жидкостью;
Капля жидкости растекается,
закрывая часть твердой поверхности.
За счет этого происходит частичная
замена поверхности с большей поверхностной
энергией
на поверхность с меньшей поверхностной
энергией
,
следовательно, запас энергии в системе
уменьшится. С другой стороны, при
растекании капли увеличивается площадь
поверхности жидкость – газ, что приводит
к увеличению свободной энергии системы.
Отсюда следует вывод:
если
![]() ,
то происходит полное смачивание;
,
то происходит полное смачивание;
если
![]() ,
то жидкость частично смачивает поверхность
,
то жидкость частично смачивает поверхность
если
 ,
,
 ,
,
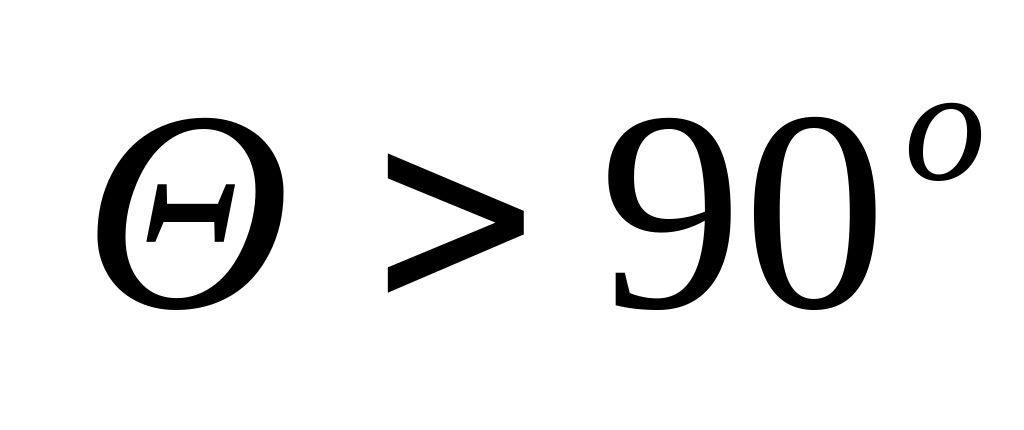 – поверхность не смачивается жидкостью;
– поверхность не смачивается жидкостью;чем меньше поверхностное натяжение жидкости на границе с воздухом , тем лучше жидкость смачивает поверхность.
С точки зрения смачивания твердой поверхности водой различают гидрофильные и гидрофобные поверхности. Если для воды , то поверхность гидрофильная, если – гидрофобная. К гидрофильным поверхностям относят высокоэнергетические поверхности (кварц, стекло), которые хорошо смачиваются водой. Воск, парафин, тефлон, фторопласты, полиэтилены, твердые жиры плохо смачиваются водой, т.е. представляют собой гидрофобные поверхности.
Смачивание можно изменять за счет модификации свойств твердых поверхностей путем их гидрофобизации или гидрофилизации и за счет регулирования поверхностного натяжения жидкости. Например, при стирке смачивание ткани увеличивается при добавлении стирального порошка, содержащего ПАВ. Для предотвращения промокания обуви ее покрывают веществом с более низким поверхностным натяжением – кремом для обуви.
