
Первичная структура нуклеиновых кислот Строение полинуклеотидной цепи
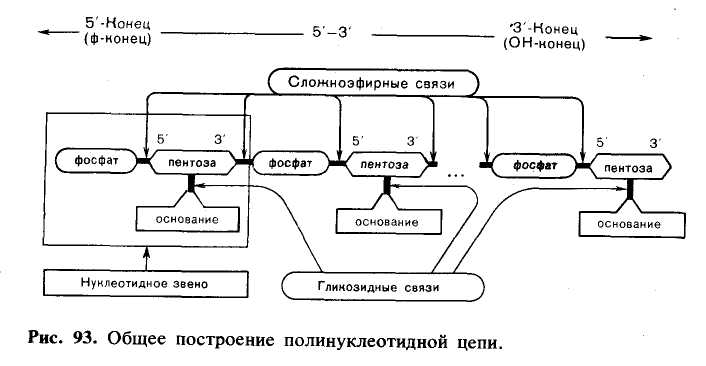
Нуклеотиды связываются в длинные цепи с помощью фосфатных групп, образуя высокомолекулярные продукты поликонденсации— нуклеиновые кислоты. Рибонуклеотиды образуют РНК, дезоксирибонуклеотиды — ДНК. Фосфатная группа в полинуклеотидной цепи образует две сложноэфирные связи: с С-3' предыдущего нуклеотидного звена и с С-5' последующего нуклеотидного звена (рис.94).
Полимерная цепь нуклеиновых кислот состоит из чередующихся пентозных и фосфатных остатков, а гетероциклические основания являются «боковыми» группами, присоединенными к пентоз-ным остаткам. Концы линейной (неразветвленной) полинуклеотидной цепи обозначают: 5'-конец (слева) и 3'-конец (справа), так как написание цепи обычно начинают с 5'-конца. В этом случае общее направление образования фосфодиэфирных связей в цепи обозначается 5'→3'. На 5'-конце находится фосфатная
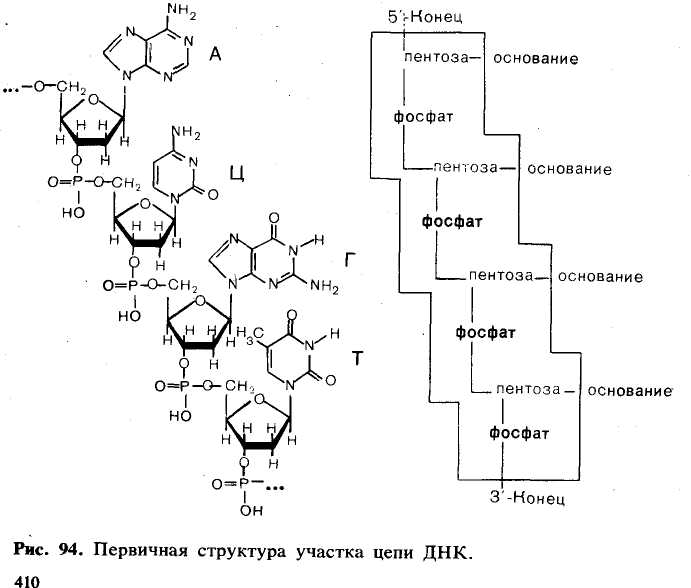
На рис. 94 приведено строение произвольного участка цепи ДНК, включающего четыре нуклеиновых основания. Легко вообразить, какое множество сочетаний может быть получено при
построении цепей путем варьирования последовательностей четырех мононуклеотидных остатков.
Принцип построения цепи РНК такой же, как и у ДНК, с двумя исключениями: пентозным остатком в РНК является D-рибоза и в наборе гетероциклических оснований используется не тимин, а урацил.
• Первичная структура нуклеиновых кислот — это последовательность нуклеотидных звеньев, связанных ковалентными связями в непрерывную цепь полинуклеотида.
Для удобства записи первичной структуры нуклеиновых кислот существует несколько способов сокращений. Один из них заключается в использовании ранее приведенных сокращенных названий нуклеозидов и обозначении фосфатной группы буквой «ф» (в иностранной литературе и в ряде отечественных источников— латинской буквой «р»). Знак «ф» ставится слева от обозначения нуклеозида, если у него этерифицирован углеводный остаток по С-5', и справа, если он этерифицирован по С-3'. Иногда букву «ф» опускают и заменяют ее черточкой. Например, приведенный на рис. 94 фрагмент цепи ДНК сокращенно можно записать:
АфЦфГфТф или А-Ц-Г-Т. Более точно дезоксирибонуклеози-ды записываются дА, дГ, дЦ, но буква «д» часто не указывается, если из текста очевидно, что речь идет о ДНК.
Нуклеиновые кислоты представляют собой гетерополимеры, т. е. они состоят из нуклеотидов с разными гетероциклическими основаниями.
Нуклеотидный состав ДНК и РНК

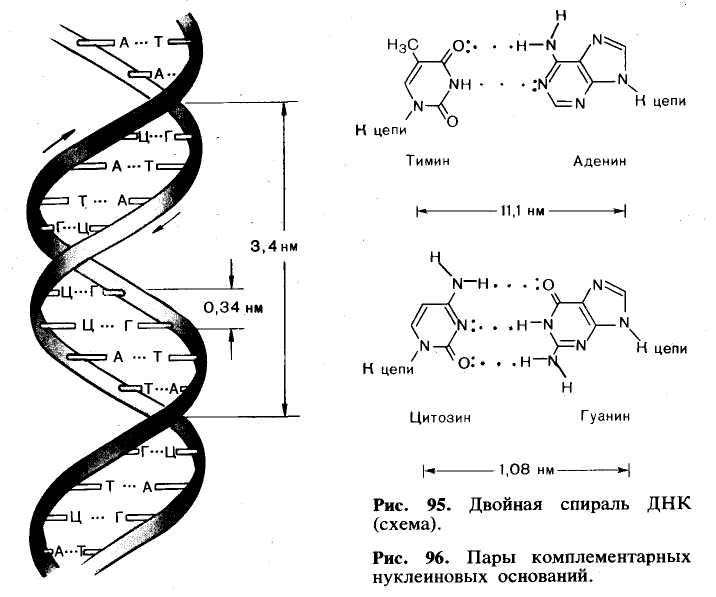
Выделение и идентификацию компонентов нуклеиновых кислот производят с помощью физико-химических методов. Очень важную роль в разделении сложных смесей играют хроматографиче-ские методы. Пиримидиновые и пуриновые основания, обладающие вследствие ароматического характера заметным поглощением около 260 нм, обычно идентифицируют с помощью УФ-спектроскопии. Поскольку нуклеотиды имеют кислотный характер и способны находиться в ионизированном состоянии, то для их идентификации используют также электрофорез.
Наряду с определением нуклеотидного состава важнейшая задача состоит и в установлении нуклеотидной последовательности, т. е. порядка чередования нуклеотидных звеньев. Общий подход заключается в использовании блочного метода: сначала полинуклеотидную цепь направленно расщепляют на более мелкие блоки — олигомеры и определяют в них нуклеотидную последовательность. Такой анализ повторяют дважды, используя во второй раз такие расщепляющие агенты, которые делят цепь на фрагменты в иных местах по сравнению с первым разом. Полинуклеотидную цепь расщепляют на довольно короткие фрагменты. Более длинные олигонуклеотиды пока еще трудно поддаются изучению.
Наиболее удобными объектами исследования оказались транспортные РНК (тРНК), как имеющие относительно небольшую молекулярную массу. К настоящему времени установлен состав и нуклеотидная последовательность более чем у 100 тРНК. Достигнуты большие успехи и в установлении первичной структуры ДНК.
