
- •Тема 1. «Основные компоненты продуктов, их превращение в процессе хранения и переработке» План
- •Контрольные вопросы
- •Тема 2. «Белки» План
- •Суточная потребность организма человека в аминокислотах
- •Изомерия и номенклатура.
- •2.Белки.
- •Строение.
- •Характеристика трёх структур белковых молекул
- •Классификация
- •Свойства.
- •Гидратация.
- •Денатурация белков.
- •Пенообразование
- •Гидролиз белков
- •Горение
- •Цветные реакции
- •3. Пищевая ценность белков.
- •4.Нуклеиновые кислоты
- •Контрольные вопросы.
- •Практические задания
- •Тема 3. «Углеводы» План
- •Контрольные вопросы
- •Задачи и практические задания
- •Тема 4. «Липиды (жиры и масла)» План
- •Тема 5. «Витамины» План
- •Суточная потребность человека в витаминах и их основные функции.
- •Водорастворимые витамины
- •Жирорастворимые витамины.
- •Тема 6. «Вода» План
- •Тема 7. «Минеральные вещества»
- •Контрольные вопросы
- •Тема 8. «Пищевые кислоты» План
- •Тема 9. «Ферменты»
- •Классификация ферментов.
- •Некоторые примеры использования ферментов в промышленности
- •Задачи.
- •Тема 10. «Составление рационального питания» План.
- •Контрольные вопросы
- •Тема 11. «Пищевые добавки» План.
- •Природные токсиканты и загрязнители.
- •Контрольные вопросы.
Денатурация белков.
При денатурации под влиянием внешних факторов (температуры, механического воздействия, действия химических агентов и ряда других факторов) происходит изменение вторичной, третичной и четвертичной структур белковой макромолекулы, т.е. её пространственной структуры. Первичная структура, а следовательно, и химический состав белка не меняются. Изменяются физические свойства: снижается растворимость, способность к гидратации, теряется биологическая активность. Меняется форма белковой макромолекулы, происходит агрегирование. В тоже время увеличивается активность некоторых химических групп, облегчается воздействие на белки протеолитических ферментов, а следовательно, он легче гидролизуется.
В пищевой технологии особое практическое значение имеет тепловая денатурация белков, степень которой зависит от температуры, продолжительности нагрева и влажности. Это необходимо помнить при разработке режимов термообработки пищевого сырья, полуфабрикатов, а иногда и готовых продуктов. Особую роль процессы тепловой денатурации играют при бланшировании растительного сырья, сушке зерна, выпечке хлеба, получении макаронных изделий. Денатурация белков может вызываться и механическим воздействием (давлением, растиранием, встряхиванием, ультразвуком). Наконец, к денатурации белков приводит действие химических реагентов (кислот, щелочей, спирта, ацетона).Все эти приёмы широко используются в пищевой и биотехнологии.
Пенообразование
Под процессом пенообразования понимают способность белков образовывать высококонцентрированные системы «жидкость-газ», называемые пенами. Устойчивость пены, в которой белок является пенообразователем, зависит не только от его природы и от концентрации, но и от температуры. Белки в качестве пенообразователей широко используются в кондитерской промышленности (пастила, зефир, суфле). Структуру пены имеет хлеб, а это влияет на его вкусовые свойства.
Молекулы белков под влиянием ряда факторов могут разрушаться или вступать во взаимодействие с другими веществами с образованием новых продуктов. Для пищевой промышленности можно выделить два очень важных процесса: 1) гидролиз белков под действием ферментов и 2) взаимодействие аминогрупп белков или аминокислот с карбонильными группами восстанавливающих сахаров. Под влиянием протеаз – ферментов, катализирующих гидролитическое расщепление белков, последние распадаются на более простые продукты (поли- и дипептиды) и в конечном итоге на аминокислоты. Скорость гидролиза белка зависит от его состава, молекулярной структуры, активности фермента и условий.
Гидролиз белков
Реакцию гидролиза с образованием аминокислот в общем виде можно записать так:
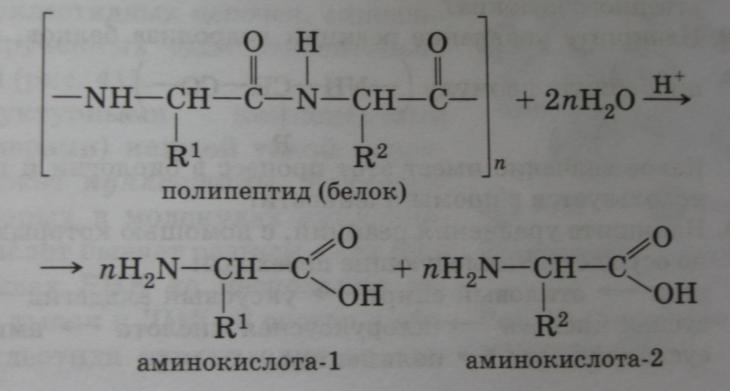
Горение
Белки горят с образованием азота, углекислого газа и воды, а также некоторых других веществ. Горение сопровождается характерным запахом жжёных перьев.
Цветные реакции
Используют следующие реакции:
ксантопротеиновую, при которой происходит взаимодействие ароматических гетероароматических циклов в молекуле белка с концентрированной азотной кислотой, сопровождающееся появлением желтой окраски;
биуретовую, при которой происходит взаимодействие слабощелочных растворов белков с раствором сульфата меди (II) с образованием комплексных соединений между ионами меди и полипептидами. Реакция сопровождается появлением фиолетово-синей окраски.
