
- •Хід роботи Дослід 1. Одержання і властивості метану
- •Дослід 1.1 Одержання метану.
- •Дослід 1.2. Горіння метану.
- •Дослід 1.3. Дослідження властивостей метану.
- •Дослід 2. Добування і властивості етилену
- •Дослід 2.1. Добування етилену.
- •Дослід 2.2. Доведення ненасиченого характеру етилену.
- •Дослід 2.3. Горіння етилену.
- •Дослід 4. Одержання і властивості ацетилену
- •Контрольні запитання та вправи
- •Лабораторна робота №2
- •Хід роботи. Дослід 1 Вивчення властивостей спиртів
- •1.1 Випробовування спиртів індикатором
- •1.2 Взаємодія спиртів з активними металами
- •І.3 Окислення спиртів
- •1.4 Якісна реакція на багатоатомні спирти
- •Дослід 2 Окислення альдегідів
- •2.1 Окислення мурашиного альдегіду купрум гідроксидом
- •Дослід 3 Вивчення властивостей карбонових кислот
- •3.1.Дисоціація карбонових кислот
- •3.2 Pеакції солеутворення
- •3.2.1 Взаємодія карбонових кислот з активними металами.
- •3.2.2 Взаємодія карбонових, кислот з основними оксидами
- •3.2.3 Взаємодія карбонових кислот з гідроксидами металів.
- •3.2.4 Взаємодія карбонових кислот з солями
- •3.3Якісна реакція на оксикислоти
- •3.3.1 Виявлення молочної кислоти сироватці
- •Контрольні запитання
- •Лабораторна робота №3
- •Хід роботи
- •1. Вивчення розчинності жирів
- •2. Вивчення емульгування жирів
- •3. Вивчення хімічних властивостей жирів
- •3.1 Реакція омилення жиру
- •3.2 Реакція бромування ненасичених жирів
- •4.Виявлення ненасиченості жирів
- •5.Обмінні реакції мила
- •5.1. Реакції з сильними кислотами. В пробірку налийте 1-2 мл. Розчину господарського мила та додайте 1 мл сульфатної кислоти Запишіть спостереження, рівняння реакції та висновки.
- •5.2. Реакції з розчиненими у воді солями
- •Контрольні запитання
- •Лабораторна робота №4
- •Хід роботи
- •1 Вивчення хімічних властивостей моноцукридів Вивчення властивостей глюкози.
- •1.1.1Реакції глюкози, як багатоатомного спирту
- •1.1.2 Реакції глюкози, як альдегіду
- •1.2.1 Реакції фруктози, як кетоноспирту
- •2.1 Інверсія цукрози
- •2.2 Доведення мономерного складу цукрози
- •3.Вивчення властивостей крохмалю
- •3.1 Якісна реакція на крохмаль
- •3.2 Кислотний гідроліз крохмалю
- •Лабораторна робота №5
- •Хід дослідів Дослід 1. Вивчення денатурації білка.
- •Дослід 2. Кольорові реакції на білок
- •Література
Івано-Франківський державний коледж технологій та бізнесу
ЗОШИТ
для лабораторних робіт
з органічної хімії
студента(ки) ІІ курсу
Спеціальність : 5.05170101Виробництво харчової продукції
Групи _________
____________________________________________
Лабораторна робота № 1
Тема Добування та вивчення властивостей вуглеводнів.
Мета : Набути навиків проведення хімічного досліду, закріпити на практиці правила техніки безпеки, навчитися самостійно робити спостереження та висновки з проведених дослідів, дослідити властивості насичених та ненасичених вуглеводнів, здійснити якісні реакції на кратні зв’язки .
Прилади та реактиви: штатив із затискачем, штатив із пробірками, прилад для одержання газу з газовідвідною трубкою, ступка , склянка, пальник, безводний ацетат натрію(CH3COONa), натронне вапно(суміш NаОН і Са(ОН)2 ), суміш етилового спирту(C2H5OH) з концентрованою сірчаною кислотою(H2SO4) ,карбід кальцію(CaC2) розчин перманганату калію(KMnO4), бромна вода(Br2 ), скіпка.
Хід роботи Дослід 1. Одержання і властивості метану
У лабораторіях метан звичайно одержують нагріванням суміші ацетату натрію і натронного вапна (суміш NаОН і Са(ОН)2).
Дослід 1.1 Одержання метану.
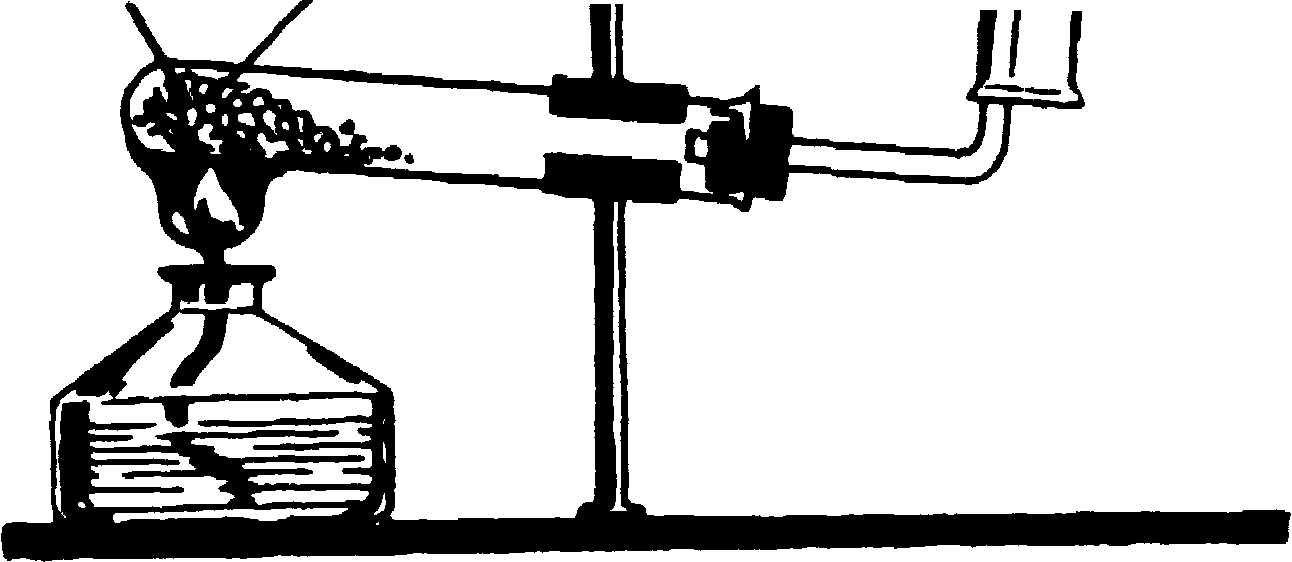 У
ступку насипати 2—3 г
(половину чайної ложки) безводного
оцтовокислого
натрію і приблизно в три рази більшу
кількість натронного вапна (суміш NаОН
і
Са(ОН)2
). Товкачем
розмішати в ступці оцтовокислий
натрій і натронне вапно. Всипати отриману
суміш у пробірку ,
закрити корком
з газовідвідною
трубкою і закріпити
її в затискачі
штатива.
У
ступку насипати 2—3 г
(половину чайної ложки) безводного
оцтовокислого
натрію і приблизно в три рази більшу
кількість натронного вапна (суміш NаОН
і
Са(ОН)2
). Товкачем
розмішати в ступці оцтовокислий
натрій і натронне вапно. Всипати отриману
суміш у пробірку ,
закрити корком
з газовідвідною
трубкою і закріпити
її в затискачі
штатива.
Випробувати прилад на герметичність, і обережно почати нагрівати пробірку із сумішшю. Прогріти всю пробірку, потім, нагріваючи суміш біля дна, поступово пересувати пальник далі так, щоб могли реагувати нові порції суміші. Коли почнеться активне виділення газу, збирати його в пробірки. Як тільки обидві пробірки заповняться газом, припинити нагрівання.
Записати спостереження , відповідне рівняння реакції та висновок .
Спостереження |
|
|
|
|
|
|
|
|
|
|
Рівняння реакції |
|
|
|
|
|
|
|
|
Висновок |
|
|
|
|
|
|
Дослід 1.2. Горіння метану.
Підпалити газ, шо виділяється.
Записати спостереження. Яким полум’ям горить метан. Чому?. Запишіть відповідне рівняння реакції та висновок.
Спостереження |
|
|
|
|
|
|
|
|
|
|
Рівняння реакції |
|
|
|
|
|
|
|
|
Висновок |
|
|
|
|
|
|
|
Дослід 1.3. Дослідження властивостей метану.
Для проведення цього досліду можна скористатися приладом, у якому одержали метан. Якщо треба, то суміш оцтовокислого натрію з натронним вапном замінити свіжою порцією.
Сильно нагріти суміш і пропустити метан, що виділяється, через розчин перманганату калію в пробірці, а потім через бромну воду - в іншій пробірці. Звернути увагу, що знебарвлення розчину не відбувається.
Записати спостереження та висновки з проробленого досліду.
Спостереження |
|
|
|
|
|
|
|
|
|
|
Рівняння реакції |
|
|
|
|
|
|
|
|
Висновок |
|
|
|
|
|
|
|
|
|
