Билет3
1. Молочный сахар — лактоза содержится только в молоке. Гидролиз лактозы происходит в кишечнике, причем протекает он медленно, в связи с чем процессы брожения в кишечнике ограничиваются и нормализуется жизнедеятельность полезной кишечной микрофлоры. Поступление в организм лактозы способствует развитию молочнокислых бактерий, подавляющих в кишечнике развитие гнилостных микроорганизмов. Целлюлоза (клетчатка) по химической структуре весьма близка к полисахаридам. В кишечнике человека железистый аппарат не продуцирует ферментов, расщепляющих целлюлозу, и таким образом не в состоянии переваривать ее. Однако некоторые кишечные бактерии вырабатывают ферменты, которые расщепляют целлюлозу. Высоким содержанием клетчатки характеризуются зерновые продукты. Однако помимо общего количества клетчатки важное значение имеет ее качество. Менее грубая, нежная клетчатка хорошо расщепляется в кишечнике и лучше усваивается. Такими свойствами обладает клетчатка картофеля и овощей. Известна роль клетчатки в стимулировании перестальтики кишечника. Она способствует выведению из организма холестерина. Объясняется это тем, что клетчатка адсорбирует стерины и препятствует обратному их всасыванию. Клетчатка играет важную роль в нормализации полезной кишечной микрофлоры. Гала̀ктоземи́я — наследственное заболевание, в основе которого лежит нарушение обмена веществ на пути преобразования галактозы в глюкозу (мутация структурного гена, ответственного за синтез фермента галактозо-1-фосфатуридилтрансферазы). Галактоза, поступающая с пищей в составе молочного сахара — лактозы, подвергается превращению, но реакция превращения не завершается в связи с наследственным дефектом ключевого фермента. Галактоза и её производная накапливаются в крови и тканях, оказывая токсическое действие на центральную нервную систему, печень и хрусталик глаза, что определяет клинические проявления болезни. Тип наследования галактоземии аутосомно-рецессивный. При непереносимости фруктозы наблюдается отсутствие фруктозо-1-монофосфатальдолазы, а сахарозы — отсутствие -фруктофуранозидазы. Клинические симптомы в виде рецидивирующих поносов, рвот, дистрофии, при непереносимости сахарозы проявляются после введения ребенку прикорма или перевода ребенка на смешанное или искусственное вскармливание молочными смесями с добавлением сахара. Часть больных одновременно не переносят и крахмал. Непереносимость фруктозы проявляется острым расстройством со стороны желудочно-кишечного тракта и развитием токсикоза в более тяжелых случаях при введении ребенку фруктовых соков. Непереносимость дисахаридов — наследственная или приобретённая недостаточность активности дисахаридаз, обусловливающая нарушения расщепления и всасывание дисахаридов; вызывает непереносимость лактозы, сахарозы и/или мальтозы; проявляется расстройствами пищеварения и питания в виде хронической ферментативной диспепсии.
2.
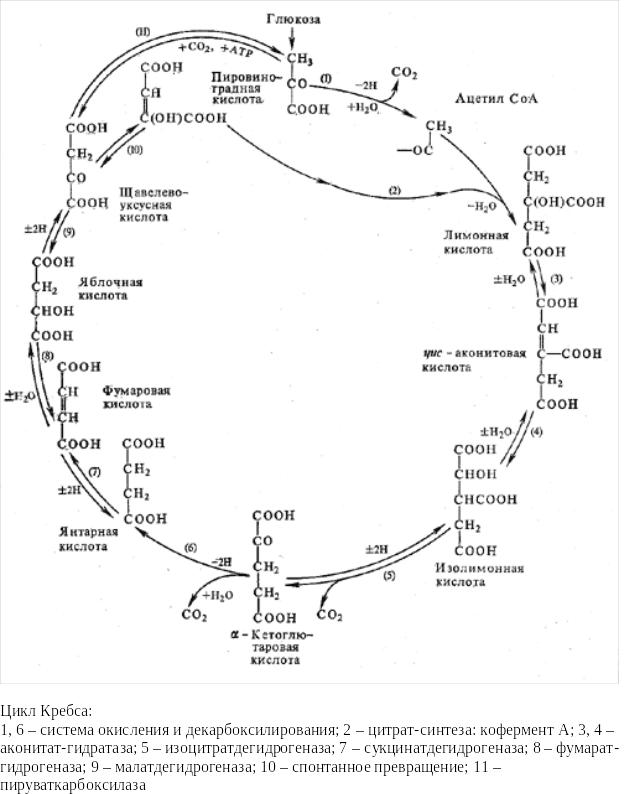
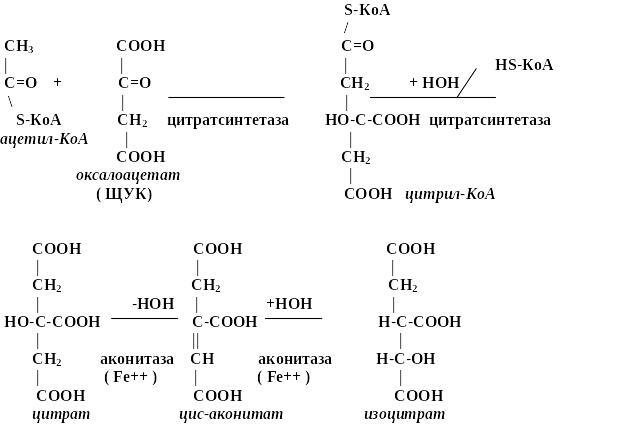
3. Понятие о специфических и общих путях катаболизма. Окислительное декарбоксилирование пировиноградной кислоты. Специфические и общие пути катаболизма . В катаболических процессах можно выделить два звена: - специфические пути катаболизма, разные для различных классов соединений (белков, жиров, углеводов и др.), - общие пути катаболизма - единые пути катаболизма для различных классов веществ, являющиеся продолжением специфических путей. С общими путями катаболизма, в основном, связаны главные биоэнергетические процессы, сопряженные с высвобождением и накоплением энергии в клетке.К специфическим путям катаболизма относятся реакции гидролиза белков, углеводов, липидов происходящие в желудочно-кишечном тракте или в тканях, реакции разрушения моносахаридов, аминокислот, жирных кислот, спиртов, происходящие в клетках и, в конце концов, завершающиеся образованием пировиноградной кислоты или ацетильным радикалом в форме ацетил-КоА.
Окислительное декарбоксилирование пировиноградной кислоты
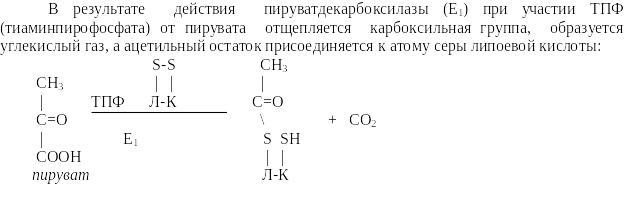
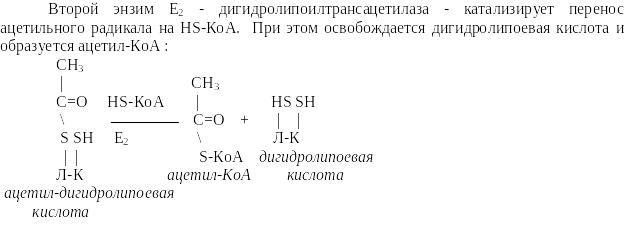
Окислительное декарбоксилирование пирувата катализируется мультиэнзимным пируват-дегидрогеназным комплексом, локализованным на внутренней мембране митохондрий со стороны матрикса. Пируват-дегидрогеназный комплекс (окислительная декарбоксилаза пировиноградной кислоты) состоит из трех ферментов (Е1,Е2,Е3): Е1-пируватдекарбоксилаза с коферментом ТПФ (тиаминпирофосфат), Е2-дигидролипоил-трансацетилаза с коферментом липоевая кислота (ЛК) и кофактором - НS-КоА, Е3-дигидролипоил-дегидрогеназа с коферментом ФАД и кофактор - НАД Пировиноградная кислота (пируват) и ацетил-КоА являются теми метаболитами, которые, включаясь в общие пути катаболизма, разрушаются до углекислого газа и воды, поставляют энергию для синтеза АТФ в митохондриях. К общим путям катаболизма относятся следующие метаболические процессы (оба эти процесса локализованы в митохондриях): - окислительное декарбоксилирования пировиноградной кислоты; - превращение ацетил-КоА в цикле трикарбоновых кислот Кребса (Ц Т К ).Пируват (пировиноградная кислота) является одним из центральных метаболитов углеводного обмена. При окислительном декарбоксилировании пирувата образуется ацетил-КоА - ключевой субтсрат цикла трикарбоновых кислот Кребса. В анаэробных условиях из пирувата образуется молочная кислота. В процессе глюконеогенеза из пируват синтезируется глюкоза. Повышение уровня пирувата наблюдается при гиповитаминозе В1, при интенсивной мышечной работе, при сердечной декомпенсации, сахарном диабете, при гепатитах. В ликворе концентрация пирувата резко повышается после черепно-мозговой травмы, при менингите, абсцессе мозга.
Окисление пирувата

4. Общая схема источников и путей превращения глюкозы в тканях.
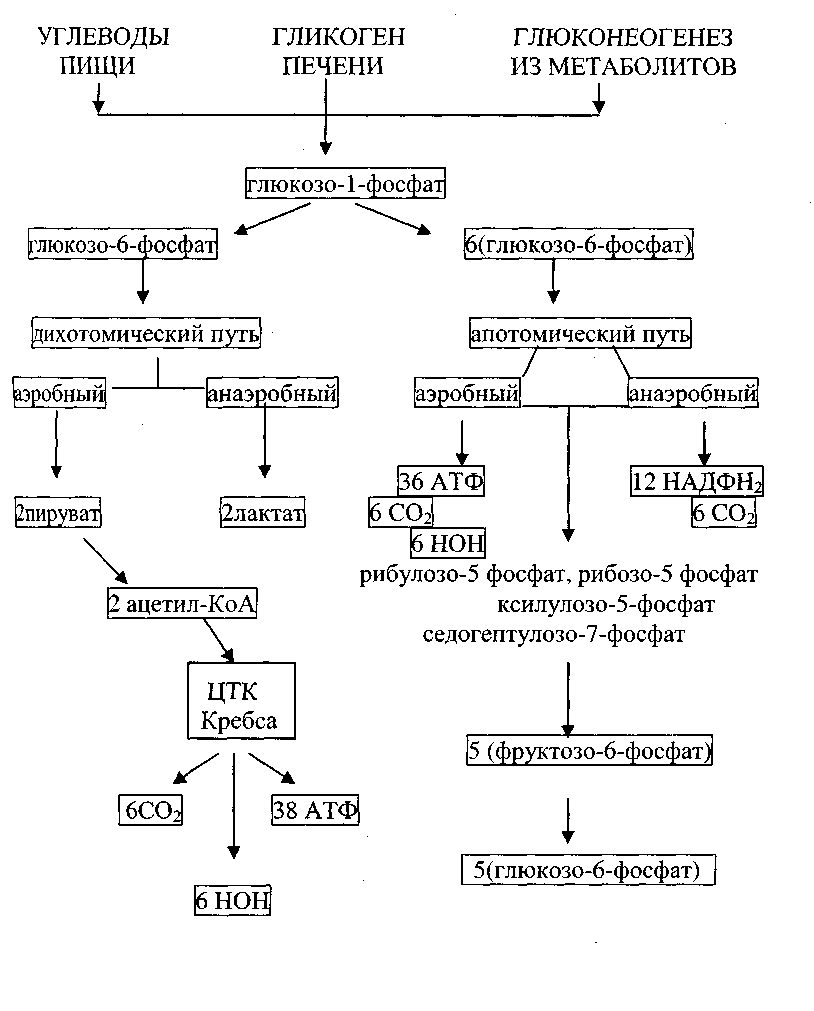
Билет7
1. Гликолиз и глюконеогенез (цикл Кори). Глюконеогенез- синтез из субстрата не углеводного происхождения.
Молочная кислота накапливается в клетках и , особенно в интенсивно работающих скелетных мышцах не яв-ся метаболитом, который подлежит выведению из организма человека. Из клеток, в которых идет анаэробный дихотомический распад глюкозы лактат поступает в кровь. Далее током крови доставляется в печень, где используется как субстрат для новообразования глюкозы – глюконеогенеза. В печени под воздействием лактатдегидрогеназы молочная кислота вначале окисляется в пируват:
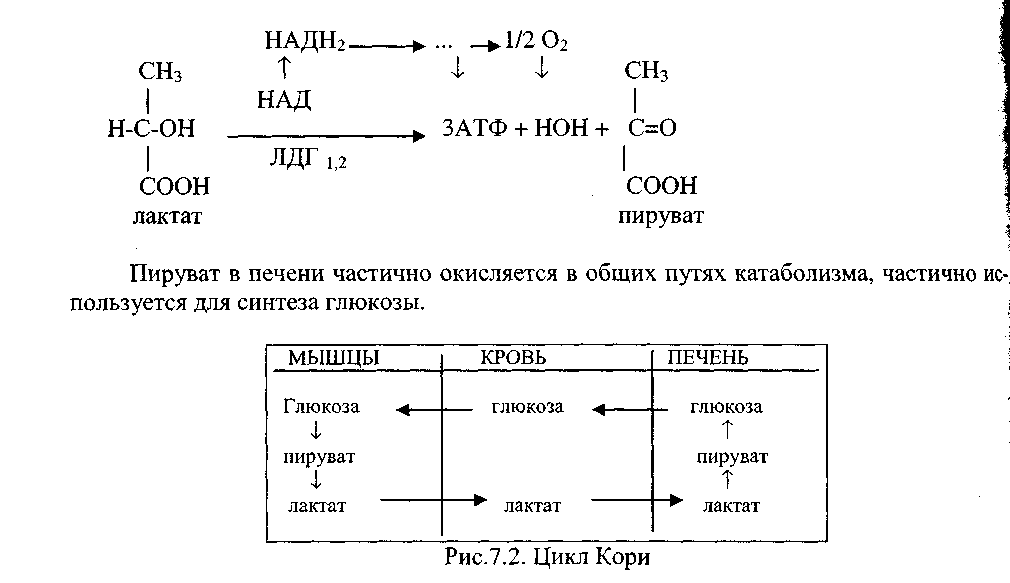
Пируват в печени частично окисляется в общих путях катаболизма ,частично используется для синтеза глюкозы.
Глюконеогенез из пирувата, в принципе протекает по тому же пути, что и анаэробный гликолиз, но в обратном направлении. Однако первые две реакции глюконеогенеза отличаются от реакции гликолиза:
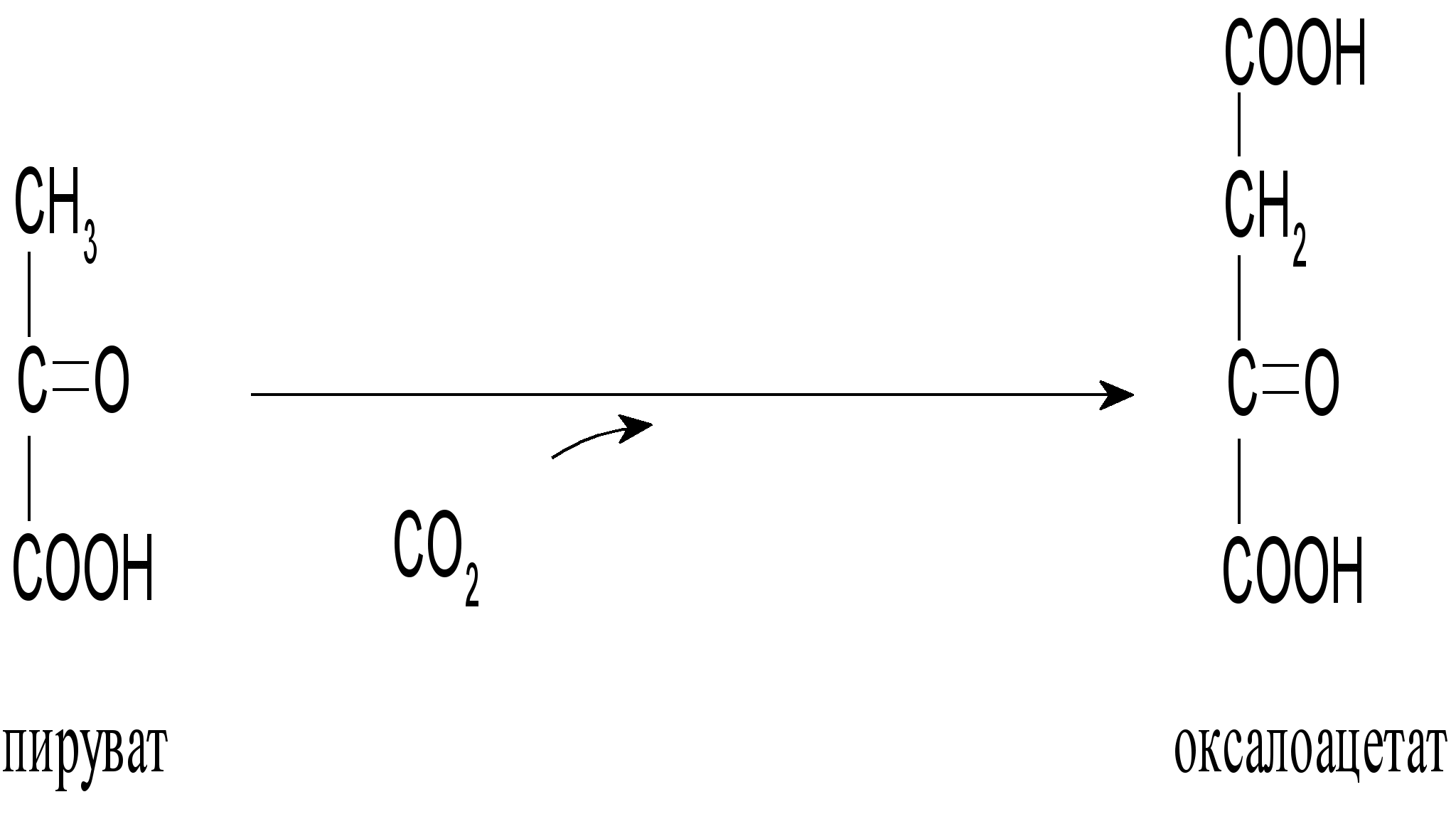
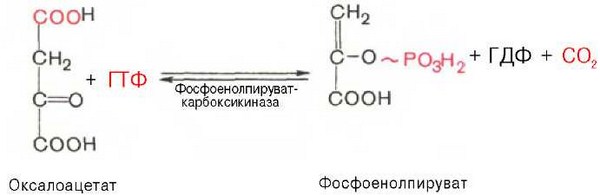
CH2
ǀǀ
C-O-PO3H2 фруктоза-1,6-дифосфат фруктоза-6-фосфат
ǀ фосфатаза
COOH
Фосфоенопируват
Фруктоза-6-фосфат глюкоза-6-фосфат глюкоза
Изомераза фосфатаза
2. Из дисахаридов в питании человека основную роль играет сахароза. При гидролизе сахароза распадается на глюкозу и фруктозу. Источниками сахарозы в питании человека являются главным образом тростниковый и свекловичный сахар.Натуральными источниками сахарозы в питании являются бахчевые, некоторые овощи и фрукты. Молочный сахар — лактоза содержится только в молоке. Гидролиз лактозы происходит в кишечнике, причем протекает он медленно, в связи с чем процессы брожения в кишечнике ограничиваются и нормализуется жизнедеятельность полезной кишечной микрофлоры. Поступление в организм лактозы способствует развитию молочнокислых бактерий, подавляющих в кишечнике развитие гнилостных микроорганизмов. Целлюлоза (клетчатка) по химической структуре весьма близка к полисахаридам. В кишечнике человека железистый аппарат не продуцирует ферментов, расщепляющих целлюлозу, и таким образом не в состоянии переваривать ее. Однако некоторые кишечные бактерии вырабатывают ферменты, которые расщепляют целлюлозу. Высоким содержанием клетчатки характеризуются зерновые продукты. Однако помимо общего количества клетчатки важное значение имеет ее качество. Менее грубая, нежная клетчатка хорошо расщепляется в кишечнике и лучше усваивается. Такими свойствами обладает клетчатка картофеля и овощей. Известна роль клетчатки в стимулировании перестальтики кишечника. Она способствует выведению из организма холестерина. Объясняется это тем, что клетчатка адсорбирует стерины и препятствует обратному их всасыванию. Клетчатка играет важную роль в нормализации полезной кишечной микрофлоры. Гала̀ктоземи́я — наследственное заболевание, в основе которого лежит нарушение обмена веществ на пути преобразования галактозы в глюкозу (мутация структурного гена, ответственного за синтез фермента галактозо-1-фосфатуридилтрансферазы). Галактоза, поступающая с пищей в составе молочного сахара — лактозы, подвергается превращению, но реакция превращения не завершается в связи с наследственным дефектом ключевого фермента. Галактоза и её производная накапливаются в крови и тканях, оказывая токсическое действие на центральную нервную систему, печень и хрусталик глаза, что определяет клинические проявления болезни. Тип наследования галактоземии аутосомно-рецессивный. При непереносимости фруктозы наблюдается отсутствие фруктозо-1-монофосфатальдолазы, а сахарозы — отсутствие -фруктофуранозидазы. Клинические симптомы в виде рецидивирующих поносов, рвот, дистрофии, при непереносимости сахарозы проявляются после введения ребенку прикорма или перевода ребенка на смешанное или искусственное вскармливание молочными смесями с добавлением сахара. Часть больных одновременно не переносят и крахмал. Непереносимость фруктозы проявляется острым расстройством со стороны желудочно-кишечного тракта и развитием токсикоза в более тяжелых случаях при введении ребенку фруктовых соков. Непереносимость дисахаридов — наследственная или приобретённая недостаточность активности дисахаридаз, обусловливающая нарушения расщепления и всасывание дисахаридов; вызывает непереносимость лактозы, сахарозы и/или мальтозы; проявляется расстройствами пищеварения и питания в виде хронической ферментативной диспепсии.
3. Пища, продукты питания, которые может использовать человек растительного и животного происхождения. Основные химические компоненты пищи: белки, жиры, углеводы, витамины. По содержанию аминокислот различают полноценные и неполноценные белки. К полноценным белкам относятся белки, содержащие все незаменимые аминокислоты. Это белки животного происхождения и некоторые бобовых культур. В пищевом отношении биологически ценными являются легкоплавкие липиды, к которым относятся растительные масла. В их составе содержаться полиненасыщенные жирные кислоты и среди них незаменимая линолевая кислота. В состав пищи должны входит минеральные в-ва и вода. Вода – это самое распространенное минеральное в-во в живых организмах. Нет ни одного организма, который мог бы обходиться без нее. Являясь неотъемлемым пищи, вода выполняет: является растворителем и стабилизатором биомолекул и ионов; явл-ся регулятором теплового баланса организма; обеспечивает транспортную функцию; способствует сохранению внутриклеточного давления, поддерживает форму клеток; явл-ся структурным компонентом клеточных мембран; используется для синтеза биомолекул; обеспечивает катаболизм биомолекул реакциями гидролиза. Минеральные в-ва находятся в организме человека в неодинаковом количестве. Макроэлементы – Ca, P, Mg, K, Na, Fe. Микроэлементы – I, F, Cu, Co, Mn, Zn. Все минеральные в-ва в организме находятся в виде соединений образующие ионы. Мин в-ва определяют величину осмотического и гидроосмотического давления. Они используются для построения опорных тканей. Короче, минеральные вещества выполняют биоэлектрическую, осмотическую, структурную, регуляторную, транспортную, энергетическую, опорную и синтетическую функции. При недостатке йода разрастается щитовидная железа (эндемический зоб), при недостатке фтора – кариес, недостаток цинка – задержка роста и специфический гиперкераноз. Отсутствие меди и кобальта – анемия.
4. .Понятие о специфических и общих путях катаболизма. Окислительное декарбоксилирование пировиноградной кислоты. Специфические и общие пути катаболизма . В катаболических процессах можно выделить два звена: - специфические пути катаболизма, разные для различных классов соединений (белков, жиров, углеводов и др.), - общие пути катаболизма - единые пути катаболизма для различных классов веществ, являющиеся продолжением специфических путей. С общими путями катаболизма, в основном, связаны главные биоэнергетические процессы, сопряженные с высвобождением и накоплением энергии в клетке.К специфическим путям катаболизма относятся реакции гидролиза белков, углеводов, липидов происходящие в желудочно-кишечном тракте или в тканях, реакции разрушения моносахаридов, аминокислот, жирных кислот, спиртов, происходящие в клетках и, в конце концов, завершающиеся образованием пировиноградной кислоты или ацетильным радикалом в форме ацетил-КоА.
Окислительное декарбоксилирование пировиноградной кислоты
Регуляция общих путей катаболизма. Анаболические функции цикла Кребса


Билет8
1. Понятие о тканевом дыхании и биологическом дыхании. Высвобождение свободной энергии при катаболизме углеводов, липидов и аминокислот может происходить в животном организме в аэробных и анаэробных условиях. Энергетически более выгоден аэробный путь катаболизма, который сопровождается в обязательном порядке поглощением тканями кислорода и выделением углекислого газа, т.е явление называемое тканевое дыхание или внутреннее, клеточное дыхание. В основе биологического окисления различных энергетических субстратов, как показали исследования, лежат три след. Типа реакций:1.перенос электронов2.перенос атомов водорода3.перенос атомов кислорода Основными энергетическими субстратами служат углеводы и жиры. Так клетки головного мозга млекопитающих вообще не способны использовать для клеточного дыхания, ничего кроме глюкозы. Окисление глюкозы в клетке, как главного энергетического субстрата, происходит путем последовательных реакций дегидрирования. При этом в анаэробных условиях окисление глюкозы завершается образованием двух молекул пирувата, которые восстанавливаются в две молекулы лактата. В аэробных условиях, образующиеся в цитозоле при гликолизе две молекулы пирувата подвергаются в митохондриях окислительному декарбоксилированию с образованием двух молекул ацетил КоА, которые разрушаются в цикле Кребса до углекислого газа и воды с высвобождением свободной энергии, трансформируемой ферментами дыхательной цепи митохондрий в макроэргические связи АТФ
Дегидрирование субстратов и окисление водорода как источник энергии в клетке. Биологическое окисление это процесс дегидрирования субстрата с помощью промежуточных переносчиков водорода и его конечного акцептора. Если в роли конечного акцептора выступает кислород, процесс называется аэробным окислением или тканевым дыханием, если конечный акцептор представлен не кислородом анаэробным окислением. Анаэробное окисление имеет ограниченное значение в организме человека. Основная функция биологического окисления обеспечение клетки энергией в доступной форме. Тканевое дыхание процесс окисления водорода кислородом до воды ферментами цепи тканевого дыхания. Оно протекает по следующей схеме: Вещество окисляется, если отдает электроны или одновременно электроны и протоны (атомы водорода), или присоединяет кислород. Способность молекулы отдавать электроны другой молекуле определяется окислительно-восстановительным потенциалом (редокс-потенциалом). Любое соединение может отдавать электроны только веществу с более высоким окислительно-восстановительным потенциалом. Окислитель и восстановитель всегда образуют сопряженную пару.
2. Согласно предложенной П. Митчеллом гипотезе, движущей силой фосфорилирования АДФ служит энергия разности редокс-потенциалов, возникающая при переносе электронов от окисляемого субстрата по дыхательной цепи к кислороду трансформируемая в энергию протонного электрохимического потенциала ( dM H+) , возникающая на внутренней мембране митохондрий. За счет протонов отщепляемых от окисляемых субстратов и накопления их тна наружной стороне мембраны митохондрий, она оказывается электроположительной , а со стороны митохондриального матрикса заряжается элктроотрицательно. Ионы Н+ , выведенный наружу , под воздействием электроосмотических сил устремляются внутрь , в митохондриальный матрикс через специальные протонный каналы , в которых функционирует Н+ - АТФ синтетаза . Переход ионов Н+ с более высокой в зону с более низкой их концентрацией сопровождается выделением свободной энергии , за счет которой и сетезируется АТФ. До определенного времени считалось что АТФ и только АТФ выполняет универсальную аккумулирующую энергию функцию в клетке. Однако исследованиями В,П Скулачева и другими биоэнергетиками было устанолено что трансмембранный электрохимический потенциал , возникающий на мембране за счет Н+ градиента является универсальной формой энергии в клетке и может быть использован : -для синтеза АТФ ; - для транспорта ионов кальция и др. ионов; - для транспорта фосфатов; - для транспорта АДФ и АТФ; - для теплообразования ; - для сократительной и двигательной активности.В нормальной функционирующей клетке процесс трансформации энергии и степень окислительного фосфорилирования зависит от целого ряда факторов : от целостности митохондриальной мембраны , от типа окисляемого субстрата , от уровня кислорода , доставки неорганического фосфата и уровня АДФ.
3 Гликолиз и глюконеогенез (цикл Кори). Глюконеогенез- синтез из субстрата не углеводного происхождения. Молочная кислота накапливается в клетках и , особенно в интенсивно работающих скелетных мышцах не яв-ся метаболитом, который подлежит выведению из организма человека. Из клеток, в которых идет анаэробный дихотомический распад глюкозы лактат поступает в кровь. Далее током крови доставляется в печень, где используется как субстрат для новообразования глюкозы – глюконеогенеза. В печени под воздействием лактатдегидрогеназы молочная кислота вначале окисляется в пируват:
Пируват в печени частично окисляется в общих путях катаболизма ,частично используется для синтеза глюкозы.
Глюконеогенез из пирувата, в принципе протекает по тому же пути, что и анаэробный гликолиз, но в обратном направлении. Однако первые две реакции глюконеогенеза отличаются от реакции гликолиза:
CH2
ǀǀ
C-O-PO3H2 фруктоза-1,6-дифосфат фруктоза-6-фосфат
ǀ фосфатаза
COOH
Фосфоенопируват
Фруктоза-6-фосфат глюкоза-6-фосфат глюкоза
Изомераза фосфатаза
4. Биосинтез и мобилизация гликогена. Биологическая роль этого процесса.
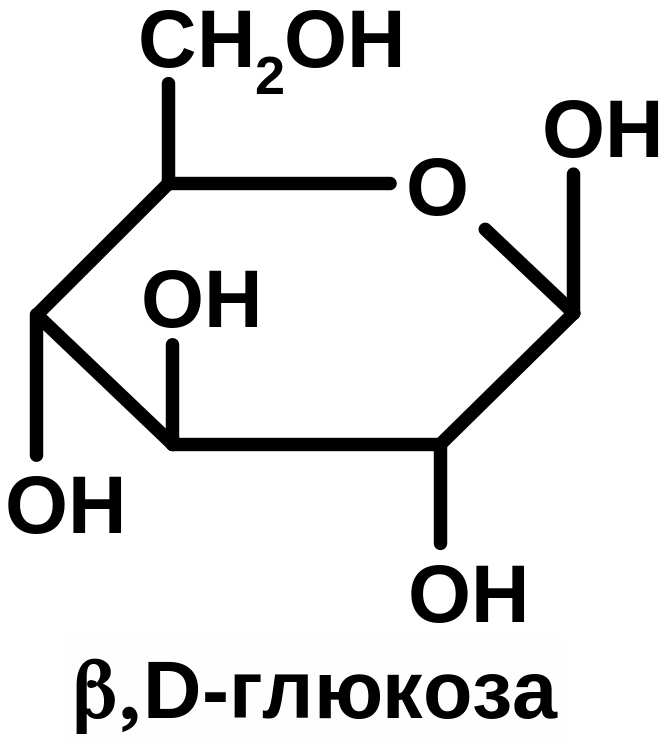
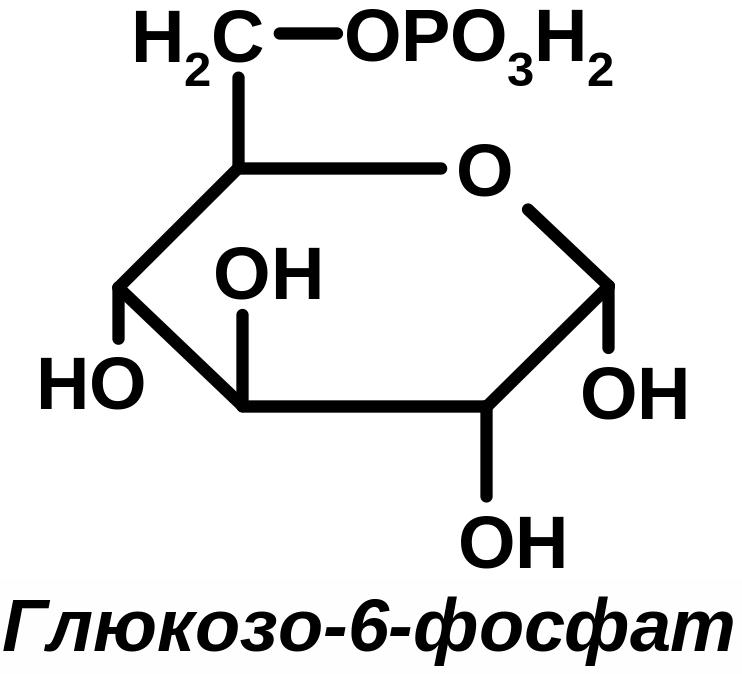
Биологический синтез гликогена Установлено, что гликоген образуется почти во всех клетках организма, однако наибольшее содержание гликогена обнаружено в печени (2-6%) и в мышцах (0,5-2%). Т.к. общая мышечная масса организма человека велика, то большая часть всего гликогена содержится в мышцах. Глюкоза из крови легко поступает в клетки организма и в ткани, легко проникая через биологические мембраны. Инсулин обеспечивает проницаемость мембран, это единственный гормон, обеспечивающий транспорт глюкозы в клетки органов и тканей. Как только глюкоза поступает в клетку, она сразу же как бы запирается в ней. В результате первой метаболической реакции, катализируемой ферментом гексакиназой в присутствии АТФ, глюкоза превращается в фосфорный эфир – глюкозо-6-фосфат, для которого клеточная мембрана не проницаема. Глюкозо-6-фосфат теперь будет использоваться клеткой в метаболических реакциях (анаболизм, катаболизм). Из клетки глюкоза может обратно выйти в кровь только после гидролиза под действием фосфатазы (глюкозо-6-фосфатазы). Этот фермент есть в печени, почках, в эпителии кишечника, в других органах и тканях его нет, следовательно, проникновение глюкозы в клетки этих органов и тканей необратимо. Процесс биосинтеза гликогена можно записать в виде 4-х стадий: глюкоза (гексакиназа, АТФАДФ) глюкозо-6-фосфат (фосфоглюкомутаза) глюкозо-1-фосфат (глюкозо-1-фосфат-уридин трансфераза) УДФ-глюкоза (гликоген-синтетаза, +[C6Н10О5]n) [C6Н10О5]n+1 (это наращенный гликоген) +УДФ
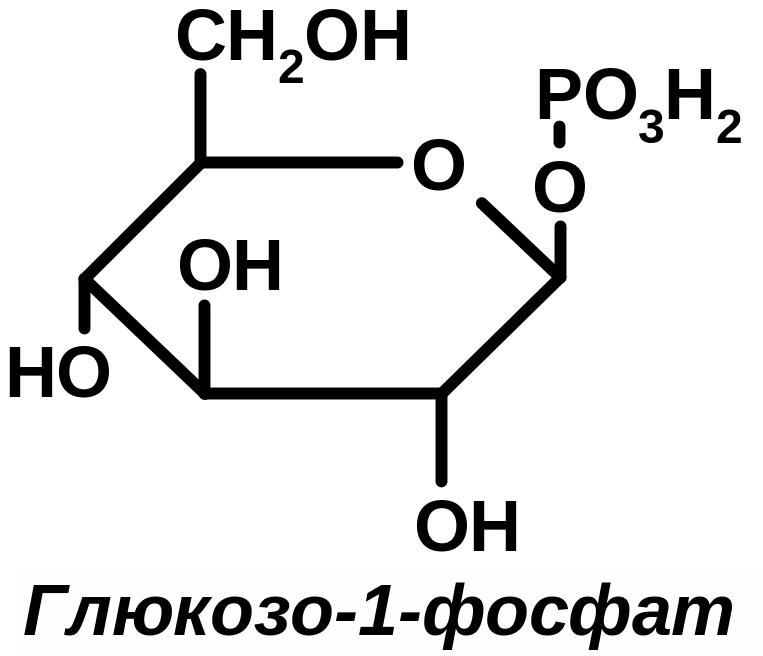 Затем
УДФ+АТФ(нуклеозиддифосфаткиназа)
УТФ+АДФ. Т.о. на присоединение 1 молекулы
глюкозы тратмтся 2 молекулы АТФ.
Гликогенсинтаза является трансферазой,
которая переносит остатки глюкозы,
входящие в УДФ-глюкозу на гликозидную
связь остаточного в клетке гликогена.
При этом образуются -1,4-
гликозидные связи. Образование
-1,6-гликозидных
связей в точках ветвления гликогена
катализирует специальный фермент
гликогенветвящий. Гликоген в клетках
печени накапливается во время пищеварения,
и рассматривается как резервная форма
глюкозы, которая используется в
промежутках между приёмами пищи. Распад
гликогена
Он может идти двумя путями: 1. Основной
– фосфоролитический
- протекает в печени, почках, эпителии
кишечника. Схематически его можно
записать в виде 3-х стадий: а) [C6Н10О5]n
(это гликоген)
(фосфорилаза А, +Н3РО4)
глюкозо-1-фосфат +[C6Н10О5]n-1;
б) глюкозо-1-фосфат
(фосфоглюкомутаза) глюкозо-6-фосфат; в)
глюкозо-6-фосфат
(глюкозо-6-фосфатаза, +Н2О)
глюкоза + Н3РО4;
2. Не основной – амилолитический.
его доля мала и незначительна. Протекает
в клетках печени при участии: - -амилазы
слюны, расщепляющей -1,4-гликозидные
связи; - амило-1,6-гликозидазы, расщепляющей
-1,6-гликозидные
связи в точках ветвления гликогена; -
-амилазы,
которая последовательно отрывает
концевые остатки глюкозы от боковых
цепей гликогена.
Затем
УДФ+АТФ(нуклеозиддифосфаткиназа)
УТФ+АДФ. Т.о. на присоединение 1 молекулы
глюкозы тратмтся 2 молекулы АТФ.
Гликогенсинтаза является трансферазой,
которая переносит остатки глюкозы,
входящие в УДФ-глюкозу на гликозидную
связь остаточного в клетке гликогена.
При этом образуются -1,4-
гликозидные связи. Образование
-1,6-гликозидных
связей в точках ветвления гликогена
катализирует специальный фермент
гликогенветвящий. Гликоген в клетках
печени накапливается во время пищеварения,
и рассматривается как резервная форма
глюкозы, которая используется в
промежутках между приёмами пищи. Распад
гликогена
Он может идти двумя путями: 1. Основной
– фосфоролитический
- протекает в печени, почках, эпителии
кишечника. Схематически его можно
записать в виде 3-х стадий: а) [C6Н10О5]n
(это гликоген)
(фосфорилаза А, +Н3РО4)
глюкозо-1-фосфат +[C6Н10О5]n-1;
б) глюкозо-1-фосфат
(фосфоглюкомутаза) глюкозо-6-фосфат; в)
глюкозо-6-фосфат
(глюкозо-6-фосфатаза, +Н2О)
глюкоза + Н3РО4;
2. Не основной – амилолитический.
его доля мала и незначительна. Протекает
в клетках печени при участии: - -амилазы
слюны, расщепляющей -1,4-гликозидные
связи; - амило-1,6-гликозидазы, расщепляющей
-1,6-гликозидные
связи в точках ветвления гликогена; -
-амилазы,
которая последовательно отрывает
концевые остатки глюкозы от боковых
цепей гликогена.
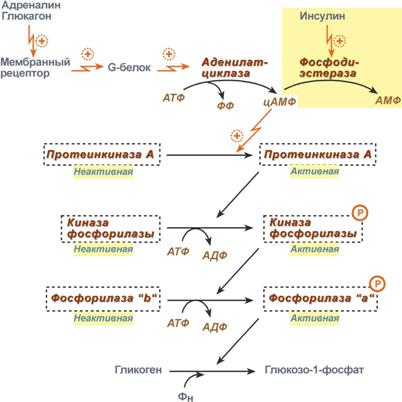
Гликоген является резервным углеводом животных тканей. Избыток углеводов, поступающих с пищей, превращается в гликоген, который откладывается в печени, образуя депо углеводов, используемых для различных физиологических функций — важная роль в регуляции уровня сахара в крови. Общее содержание гликогена около 500 г. Если углеводы с пищей не поступают, то запасы его исчерпываются через 12-18 часов. В связи с истощением резервов углеводов усиливаются процессы окисления жирных кислот. Обеднение печени гликогеном ведет к возникновению жировой инфильтрации, а далее — к жировой дистрофии печени
Билет9
1. Регуляция цепи переноса электронов и протонов (дыхательный контроль).Согласно предложенной Митчелом гипотезе, движущей силой фосфорилирования АДФ служит энергия разности редокс-потенциалов, возникающая при переносе электронов от окисляемого субстрата по дыхательной цепи к кислороду и трансформируемой в энергию протонного электрохимического потенциала (dMH+), возникающего на внутренней мембране митохондрий.За счет протонов отщепляемых от окисляемых субстратов и накопления их на наружной стороне мембраны митохондрий, она оказывается электроположительной, а со стороны митохондриального матрикс через специальные протонные каналы, в которых функционирует H+-АТФ синтетаза
При окислении одной молекулы субстрата на один атом поглощенного митохондриями кислорода может использоваться от одного до трех молекул фосфорной кислоты и синтезироваться при этом 1, 2 или 3 молекулы АТФ. Это процесс - процесс синтеза АТФ в реакциях биологического окисления субстратов получил название - окислительное фосфорилирование. Для его количественной оценки был введен показатель окислительного фосфорилирования - коэффициент Р/О . Коэффициент Р/О (АДФ/О) - это есть отношение количества молекул фосфорной кислоты (АДФ) к количеству атомов кислорода использованных митохондриями при окислении какого-либо субстрата.
2.
3. Биосинтез и мобилизация гликогена. Биологическая роль этого процесса.
Биологический синтез гликогена Установлено, что гликоген образуется почти во всех клетках организма, однако наибольшее содержание гликогена обнаружено в печени (2-6%) и в мышцах (0,5-2%). Т.к. общая мышечная масса организма человека велика, то большая часть всего гликогена содержится в мышцах. Глюкоза из крови легко поступает в клетки организма и в ткани, легко проникая через биологические мембраны. Инсулин обеспечивает проницаемость мембран, это единственный гормон, обеспечивающий транспорт глюкозы в клетки органов и тканей. Как только глюкоза поступает в клетку, она сразу же как бы запирается в ней. В результате первой метаболической реакции, катализируемой ферментом гексакиназой в присутствии АТФ, глюкоза превращается в фосфорный эфир – глюкозо-6-фосфат, для которого клеточная мембрана не проницаема. Глюкозо-6-фосфат теперь будет использоваться клеткой в метаболических реакциях (анаболизм, катаболизм). Из клетки глюкоза может обратно выйти в кровь только после гидролиза под действием фосфатазы (глюкозо-6-фосфатазы). Этот фермент есть в печени, почках, в эпителии кишечника, в других органах и тканях его нет, следовательно, проникновение глюкозы в клетки этих органов и тканей необратимо. Процесс биосинтеза гликогена можно записать в виде 4-х стадий: глюкоза (гексакиназа, АТФАДФ) глюкозо-6-фосфат (фосфоглюкомутаза) глюкозо-1-фосфат (глюкозо-1-фосфат-уридин трансфераза) УДФ-глюкоза (гликоген-синтетаза, +[C6Н10О5]n) [C6Н10О5]n+1 (это наращенный гликоген) +УДФ
Затем УДФ+АТФ(нуклеозиддифосфаткиназа) УТФ+АДФ. Т.о. на присоединение 1 молекулы глюкозы тратмтся 2 молекулы АТФ. Гликогенсинтаза является трансферазой, которая переносит остатки глюкозы, входящие в УДФ-глюкозу на гликозидную связь остаточного в клетке гликогена. При этом образуются -1,4- гликозидные связи. Образование -1,6-гликозидных связей в точках ветвления гликогена катализирует специальный фермент гликогенветвящий. Гликоген в клетках печени накапливается во время пищеварения, и рассматривается как резервная форма глюкозы, которая используется в промежутках между приёмами пищи. Распад гликогена Он может идти двумя путями: 1. Основной – фосфоролитический - протекает в печени, почках, эпителии кишечника. Схематически его можно записать в виде 3-х стадий: а) [C6Н10О5]n (это гликоген) (фосфорилаза А, +Н3РО4) глюкозо-1-фосфат +[C6Н10О5]n-1; б) глюкозо-1-фосфат (фосфоглюкомутаза) глюкозо-6-фосфат; в) глюкозо-6-фосфат (глюкозо-6-фосфатаза, +Н2О) глюкоза + Н3РО4; 2. Не основной – амилолитический. его доля мала и незначительна. Протекает в клетках печени при участии: - -амилазы слюны, расщепляющей -1,4-гликозидные связи; - амило-1,6-гликозидазы, расщепляющей -1,6-гликозидные связи в точках ветвления гликогена; - -амилазы, которая последовательно отрывает концевые остатки глюкозы от боковых цепей гликогена.
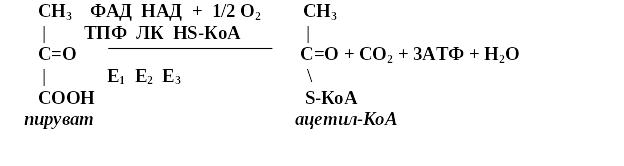
4. Биологическая роль пентозофосфатного цикла состоит в следующим: - образуется большое кол-во восстановленного НАДФ. При окислении одной молекулы глюкозо-6-фосфата образуется 12 НАДФН2, которые используются для синтеза жирных к-т, стероидных гормонов; - синтезируются различные пентозы, в том числе рибоза, необходимая для построения молекул нуклеотидов и нуклеиновых к-т; - происходит синтез 36 молекул АТФ. Пентозофосфатный цикл состоит из 2 фаз: - 1фаза – окисление 6 молекул глюкозо-6-фосфата и образование 12 НАДФН2, 6 молекул СО2, 6 молекул фосфопентоз; - 2фаза – превращение фосфопентоз в транскетолазных реакциях и образование 5 фруктозо-6-монофосфата и превращение их в глюкозо-6-фосфат.
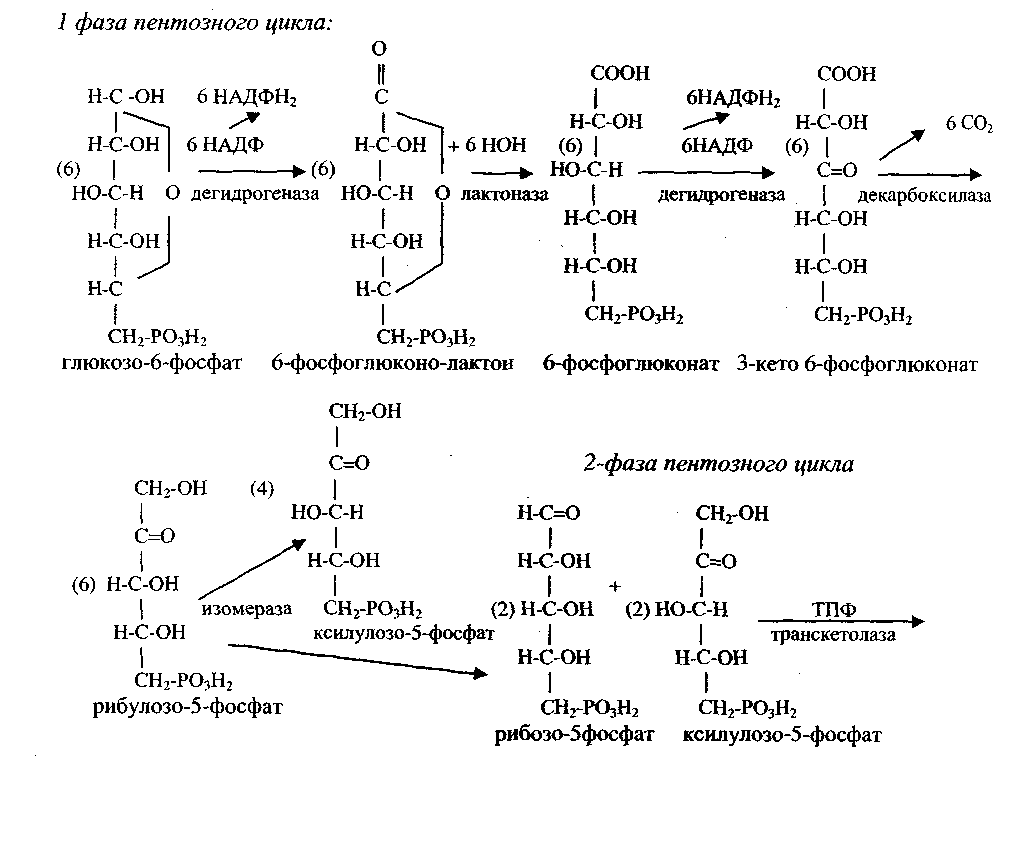
2 фаза пентозофосфатного цикла: