
Амперометрическое титрование
Полярографический метод можно применить для определения точки эквивалентности в титриметрических методах анализа, если хотя бы один из участников реакции или ее продукт окисляется или восстанавливается на микроэлектроде.
В процессе амперометрического титрования после прибавления отдельных порций реактива регистрируют величину диффузионного тока при постоянном потенциале индикаторного электрода. По этим данным строят кривую амперометрического титрования в координатах: сила тока - объем титранта (Iд – V) и графически находят точку эквивалентности. В качестве индикаторных электродов в амперометрическом титровании обычно применяют платиновые, графитовые и другие твердые электроды, чаще всего вращающиеся.
В амперометрическом титровании необходимо различать электрохимическую реакцию, протекающую на границе раздела электрод-раствор, и химическую реакцию, протекающую в растворе между определяемым веществом и титрантом.
Вид кривой амперометрического титрования зависит от того, какой компонент реакции титрования вступает в электродную реакцию: определяемое вещество, титрант или продукт реакции. Различают следующие типы кривых амперометрического титрования:
1.Титрование по диффузионному току определяемого вещества (рис.6а)
Пример. При титровании раствора, содержащего Аg+, иодидом калия используется процесс восстановления ионов серебра на платиновом вращающемся катоде. В ходе титрования сила тока Iд уменьшается, так как концентрация ионов серебра в растворе падает в результате образования осадка AgI , а после достижения точки эквивалентности остается постоянной.
2. Титрование по диффузионному току титранта (рис.6б)
Пример. При титровании раствора, содержащего Ag+, иодидом калия используется процесс анодного окисления иодид-иона. В этом случае концентрация І– в растворе увеличивается после достижения точки эквивалентности; это приводит к возрастанию силы тока Iд.
3. Титрование по диффузионному току определяемого вещества и титранта.
До точки эквивалентности диффузионный ток уменьшается с уменьшением концентрации определяемого вещества. После точки эквивалентности диффузионный ток возрастает с увеличением концентрации титранта в растворе (рис.6в).
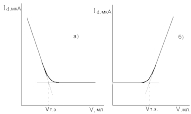
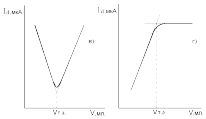
Рис. 6. Виды кривых амперометрического титрования: а) по диффузионному току определяемого вещества; б) по диффузионному току титранта; в) по диффузионному току определяемого вещества и титранта; г) по диффузионному току продукта реакции.
4. Титрование по диффузионному току, обусловленному продуктом реакции титрования.
Пример. Титрование мышьяковой кислоты иодидом калия:
HAsO42– + 2 I– + 2H+ HAsO32– + I2 + H2O.
В ходе химической реакции образуется свободный иод (продукт реакции), концентрация которого возрастает до точки эквивалентности, после чего остается постоянной. Диффузионный ток восстановления свободного иода до І– на платиновом электроде возрастает до точки эквивалентности (рис. 6г) при Е = –0,05 В по реакции:
I2
+
2ē  2
I–.
2
I–.
Точка эквивалентности во всех случаях находится графически как точка пересечения соответствующих прямых (рис. 6.).
В методах амперометрического титрования используют реакции осаждения, комплексообразования и окисления – восстановления. Многие анионы – Сl–, Br–, I–, SO42–, MoO42–и др. – титруются солью свинца при потенциале: E = –0,4 B, при этом регистрируется ток восстановления Pb2+ на ртутном капающем электроде.
В реакциях осаждения часто применяется осаждение органическими реагентами: 8-оксихинолином, купфероном, диметилглиоксимом и др., причем титрование можно проводить как по току восстановления катиона, так и по току органического реагента.
Широко используется в амперометрическом титровании реакция образования этилендиаминтетраацетатных комплексов с различными катионами: Вi3+, Fe3+, Fe2+, Ni2+, Pb2+, Zn2+, Cu2+, Co2+, Cd2+.
При амперометрическом титровании с использованием реакций окисления – восстановления в качестве титрантов используют К2Сr2O7; KBrO3 и I2 – для определения восстановителей; FeSO4, Na2S2O3 – для определения окислителей.
Для амперометрического титрования характерна экспрессность, его можно проводить в разбавленных растворах (до 10–6 10–5 М), анализировать мутные и окрашенные растворы. Амперометрическое титрование характеризуется более высокой чувствительностью, чем полярография. Несложное аппаратурное оформление и простота в обращении также выгодно отличают этот метод от других.
Амперометрическое титрование применяется для определения катионов и анионов в различных технических и природных объектах, минеральном сырье, природных водах, промышленных растворах, продуктах металлургии и т. д., а также в анализе многих органических веществ.
