
- •Законы Менделя.
- •Полигены (предложены Мазером). Полигенное наследование.
- •Гены-модификаторы
- •Хромосомная теория наследственности. (Морган и др.)
- •Генетический анализ неполного сцепления.
- •Карты хромосом.
- •Принципы построения цитологических карт:
- •Картирование генов у человека.
- •Метод отношения правдоподобия
- •Получение гибридных соматических клеток.
- •Картирование генов с использованием транслокаций и делеций.
- •Метод днк-зондов.
- •N мутант n
- •Молекулярные основы наследственности.
- •Структурные особенности строения и упаковки хромосом.
- •Приготовление хромосомных препаратов.
- •Денверовская классификация:
- •Полимеразная цепная реакция (пцр).
- •1983 Г. Карри Муллис метод анализа геномной днк.
- •Блот-гибридизация по Саузерленду (гибридизация in situ).
- •Плазмиды.
- •Геномная и тканеспецифичная днк. Библиотеки генов, их скрининг.
- •Секвенирование последовательностей днк.
- •Механизмы, нарушающие равновесие генов в популяции
- •Дрейф генов.
- •Генетика пола.
- •Мобильные элементы генома (мгэ).
- •Транспозоны млекопитающих.
- •Функциональное значение мгэ.
- •Изменчивость наследственного материала.
- •Мутационная теория. Классификация мутаций.
- •Закон гомологических рядов Вавилова.
- •Генеративные и соматические мутации.
- •Индуцированные мутации.
- •Хромосомные перестройки.
- •Полиплоидия.
- •Эксцезионная репарация. Темновая репарация и внеплановый синтез днк.
N мутант n
Р: ♀
![]() Х ♂
Х ♂
![]() →
→
![]() → признаки аллельные
→ признаки аллельные
Цис-испытание оказалось неинформативным, т.к. невозможно по результатам скрещивания отличить сцепленные аллельные признаки от неаллельных.
Транс-испытание (родитель имеет оба генотипических изменения).
Р: ♀
 Х ♂
Х ♂
 →
→
 →
аллельные
→
аллельные
слепые зрячие
Расщепление – расхождение аллелей в потомстве гетерозигот.
Вывод Льюиса: неаллельные гены рекомбинируют, сцепление не влияет на функциональный критерий.
Рекомбинационный критерий (Морган). Основан на том, что аллельные гены расщепляются (могут и рекомбинировать), поэтому нужно исключить аллельную рекомбинацию.
Р: ♀ Аа х ♂ Аа
G: А а А а
F1: AA, Aa, Aa, aa.
Для использования рекомбинационного критерия необходимо, чтобы один родитель обладал 2 генотипическими изменениями, а другой не имел ни одного.
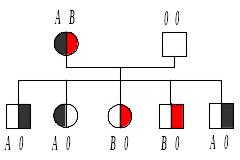

Гены аллельны, т.к. наблюдается Гены не аллельны.
расщепление.
Рекомбинационный критерий может давать ошибку 10-6, которая объясняется внутригенным кроссинговером.
Грин, Льюис, Оливер исследовали дрозофил Scute. Они проводили возвратное скрещивание компаундов.
![]()
![]() х
→
х
→
Должны получаться только мутантные формы, но когда они исследовали выборку до 10000 и более мух, то они обнаружили, что в результате таких скрещиваний появляются потомки дикого типа. Это объясняется, если допустить возможность существования внутригенного кроссинговера.
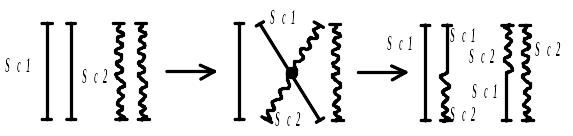
Стали говорить о псевдоаллелизме, но когда обнаружили это явление у других видов, то согласились, что ген не является единицей рекомбинации.
Функциональный критерий тоже может давать ошибки, причина – комплиментация аллельных генов. Особенность межаллельной комплиментации – не все аллели, а только сочетания некоторых из них могут образовывать зиготу дикого типа. Это связано с тем, что каждый мутантный аллель имеет свой участок повреждения.
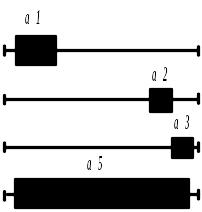
![]() → N
→ N
![]() → N
→ N
![]() → мутант
→ мутант
Генные продукты (белки) в цитоплазме могут взаимодействовать.
Т.о. в результате исследований получили:
ген дробим, состоит из отдельных частей, расположенных в них в отдельном порядке и они могут независимо изменяться при мутациях. Единица мутации - мутон (нуклеотид).
ген не является единицей рекомбинации, т.к. кроссинговер может происходить внутри сложного гена. Единица рекомбинации – рекон.
ген является единицей функции, но действие гена в целом обусловлено интеграцией его отдельных частей
Молекулярные основы наследственности.
1868 г. – Мишер открыл ДНК.
1928 г. – Гриффитс обнаружил явление трансформации при изучении пневмококковой инфекции у мышей. Использовал 2 штамма:
S – штамм: гладкая оболочка – мыши гибнут
R – штамм: шероховатая капсула – мыши живы
Если взять S – штамм и нагреть их, а затем ввести мышам, то мыши выживают. Гриффитс смешал живые невирулентные пневмококки с нагретыми капсульными формами. Заразил ими мышей, через некоторое время мыши погибли. При исследовании тканей погибших мышей он обнаружил гладкие капсульные формы и сделал вывод, что какой-то компонент убитых бактерий способен трансформировать бескапсульные формы, в результате чего они приобретали способность синтезировать полисахаридную капсулу. Но природу вещества Гриффитс не выявил.
1944 г. – Эвери, МакЛеод и МакКарти повторили эксперименты Гриффитса in vitro и обрабатывали бескапсульные штаммы экстрактами ДНК и получали трансформацию. Они обработали экстракт протеазами, рибонуклеазами и ДНК – азами. И только в последнем случае экстракт терял способность к превращению бескапсульных форм в капсульные, т.о. именно ДНК, выделенная из бактерий, несущих ген капсульного полисахарида может переносить ген в бактерии, не содержащие подобного гена.
1952 г. – получена ещё одна группа доказательств (Херши и Чейз).
Была инфицирована бактерия E. coli фагом Т2, у которого была помечена оболочка радиоактивной серой (35S) и ДНК 32Р. Через некоторое время культуру встряхивали и разделяли, обнаружили, что практически весь меченый фосфор находится внутри бактерий, а почти вся меченая сера находится в питательной среде. Было проанализировано потомство бактериофагов. Оказалось, что потомство содержало 30% меченого фосфора и только 1% меченой серы.
Позже удалось инфицировать бактерии чистой фаговой ДНК из чего был сделан вывод, что генетический материал фага сосредоточен в ДНК.
1953 г. – Уотсон и Крик установили пространственную структуру на основе рентгеноструктурного анализа.
ДНК – двойная спираль, соединение обеспечивается азотистыми основаниями, между которыми возникают водородные связи. Спаривание азотистых оснований строго определенно. Спирали закручены по часовой стрелке (В-форма), в результате суперспирализации могут появляться левозакрученные области.
Антипараллельное расположение цепей обеспечивает стабильность.
Уотсон и Крик – ДНК – цепи способны к раскручиванию и последующему делению, образуются одноцепочечные молекулы ДНК, которые служат матрицей, на которую присоединяются соответствующие нуклеотиды (полуконсервативная репликация).
Гипотеза была подтверждена в 1958 г. Мезельсоном и Сталем. Они брали кишечную палочку на минимальной среде, причем азот бактерии могли получать из хлористого аммония, содержащего тяжёлый азот. Поэтому все пуриновые и пиримидиновые основания содержали тяжелый азот и вся ДНК была тяжелой. Затем бактерии выделяли из культуры и переносили на среду, содержащую неорганический азот и после 1-2 циклов репликации отмывали, центрифугировали полученные пробы в градиенте хлористого цезия. Т.о. было доказано, что синтез ДНК идет полуконсервативным путем.
Репликация ДНК – многоэтапный процесс, который начинается с релаксации ДНК – снятие суперспирализации.
В этом процессе участвуют ферменты – топоизомеразы:
топоизомераза 1 способна разрезать сахарофосфатный остов, происходит раскручивание нити, снимаются супервитки и затем она же соединяет разрыв.
топоизомераза 2 разрезает обе нити ДНК и сшивает их потом.
Репликация начинается в точке Ори (ориджины) – участки богатые А – Т парами, ДНК – боксы – определенные последовательности ДНК из 9 или13 нуклеотидов (очень консервативны), разрыв водородных связей происходит за счет ДНК – хеликазы.
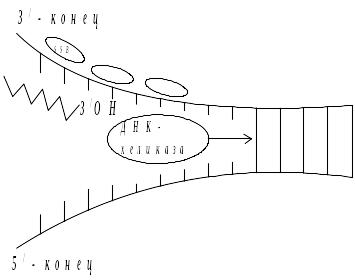
Супервитки, которые образуются перед двигающейся репликативной вилкой снимаются топоизомеразами. Для того чтобы на разделенных цепях ДНК не образовывались шпильки и все нуклеотиды одноцепочечной ДНК были доступны для спаривания, в клетках имеются специальные белки SSB, которые способны связываться только с одноцепочечной ДНК и удерживать её в раскрученном состоянии.
Синтез цепи ДНК осуществляется с помощью ДНК – полимеразы 3. Но ДНК – полимераза не способна присоединять основания просто так, ей обязательно нужен спаренный 3/ гидроксильный конец, поэтому прежде, чем ДНК – полимераза начнет синтез ДНК, синтезируется затравка из РНК – нуклеотидов (≈10) с помощью фермента праймазы.
Цепь растет в направлении 3/ - 5/. Но не существует фермента ДНК – полимеразы, которая могла бы наращивать цепь с 5/ - конца, поэтому когда Оказаки обнаружил, что в клетке во время репликации образуются и некоторое время существуют небольшие фрагменты ДНК и была предложена следующая модель: на противоположной цепи синтезируется затравка и формируется спаренный нуклеотид с 3/ - гидроксильным концом. К нему ДНК – полимераза 3 способна присоединять нуклеотиды, комплиментарные нуклеотидам основной нити ДНК. Также происходит на другой нити ДНК. Когда синтезирующийся участок ДНК доходит до затравки, ДНК – полимераза 3 отсоединяется и в дальнейшем работает ДНК – полимераза 1, которая способна отщеплять нуклеотиды затравки и застраивать образующуюся брешь нуклеотидами. Когда брешь застроена, то 2 нуклеотида, оказавшиеся рядом сшиваются с помощью фермента – ДНК – лигазы.
Та цепь, которая синтезируется непрерывно называется лидирующей, другая – отстающей.
ДНК – полимераза 3 обладает также корректорной активностью, т.е. она проверяет правильность спаренных нуклеотидов (в начале, когда присоединяет и после, когда подходят следующие нуклеотиды). Благодаря этому обеспечивается высокая точность процесса репликации.
Генетический код .
В любом участке ДНК только одна из цепей кодирует АК, поэтому код – последовательность нуклеотидов, а не пар нуклеотидов.
Свойства:
триплетен (1 триплет – колирует 1 АК)
не перекрывается: 1961 г. Ф. Крик показал, что код должен читаться неперекрывающимися триплетами с фиксированной стартовой точкой, которая означает, что считывание начинается на одном конце и заканчивается на другом. Различные части кодирующей последовательности не могут считываться независимо друг от друга. Началом синтеза белка для любого гена является кодон АУГ (метионин) . В конце гена стоят кодоны УАА, УАГ, УГА, которые являются сигналами окончания синтеза белка (стоп-кодоны). Для повышения надежности процесса терминации стоп – кодоны дублируются и первым при этом выступает УАА. Нуклеотидная последовательность, которая начинается с последующего кодона делит следующие кодоны на триплеты и заканчивается стоп – кодоном – рамка считывания.Интервал между стартовым и стоп – кодоном является открытой рамкой считывания. Мутации, при которых изменяется рамка считывания, называются мутациями сдвига рамки.
вырожденность – одной АК соответствует несколько кодонов, но кодоны используются с разной частотой.
универсальность – определенному кодону соответствует определенная АК у любого вида организмов. Известно, что имеются исключения, которые делают код квазиуниверсальным, это касается прежде всего митохондриального генома.
