
- •Лекция №13. Дикарбоновые кислоты
- •Ароматические
- •1) Щавелевая кислота.
- •2) Малоновая кислота.
- •3) Янтарная кислота.
- •4) Адипиновая кислота (гександиовая).
- •5) Бутендиовая кислота.
- •6) Фталевая кислота (бензол-1,2-дикарбоновая).
- •7) Терефталевая кислота (бензол-1,4-дикарбоновая кислота)
- •8) Угольная кислота.
Лекция №13. Дикарбоновые кислоты
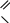 О
О
Дикарбоновые кислоты – органические кислоты, содержащие 2 карбоксильные группы - С
ОН
В основе названий – соответствующие предельные. В главную цепь включают атомы углерода карбоксильных групп. Наличие двух карбоксильных групп обозначается приставкой – «ди» и суффиксом – «овая».
Изомерия.
Структурная, обусловленная разветвлением углеродного скелета.
Взаимное расположение функциональных групп.
НООС – СООН – этандиовая (щавелевая)
НООС – СН2 – СН2 – СООН – бутандиовая (янтарная)
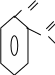 О
О
С – ОН
1 О
2 С
ОН
бензол-1,2-дикарбоновая (фталевая)
 О
О
С – ОН
1
2
О
3 С
ОН - бензол-1,3-дикарбоновая (изофталевая)
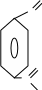 О
О
С – ОН
1
2
3
4 О
С
ОН - бензол-1,4-дикарбоновая (терефталевая)
Физические свойства.
Кристаллические вещества с высокими температурами кипения и плавления. Низшие гомологи растворимы в воде, способны образовывать водородные связи подобно спиртам и монокарбоновым кислотам.
Гомологический ряд.
Предельные (алифатические).
НООС – СООН – этандиовая (щавелевая)
НООС – СН2 – СООН – пропандиовая (малоновая)
НООС – (СН2)2 – СООН – бутандиовая (янтарная)
НООС – (СН2)3 – СООН – пентандиовая (глутаровая)
НООС – (СН2)4 – СООН – гександиовая (адипиновая)
Непредельные
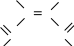 Н
Н
Н
Н
6. С С
О О
С С
НО ОН – цис-бутендиовая (малеиновая)
 О
О
Н С
С С ОН
О Н
С
НО – транс-бутеновая (фумаровая)
Ароматические
О О О
С – ОН С – ОН С – ОН
1 О 1 1
2 С 2 2
ОН О
3 С 3
ОН 4 О
С
ОН
фталевая изофталевая терефталевая
бензол-1,2-диовая
Химические свойства.
Сходны с монокарбоновыми, образуют те же функциональные производные, но участвовать могут одна или сразу две функциональные группы.
Взаимное влияние карбоксильных групп приводит к появлению специфических свойств.
Кислотные свойства более сильные. Высокая кислотность низших представителей объясняется электроакцепторным действием второй функциональной группы, которая способствует делокализации отрицательного заряда в анионе, образующимся на I ступени диссоциации.
 О
О
О
О
1. НООС – С ↔ Н+ + НООС – С
ОН О -

По мере удаления карбоксильных групп их взаимное влияние затухает.
Дикарбоновые кислоты диссоциируют главным образом по I ступени, по II ступени кислотность низкая из-за нестабильности 2-х зарядного аниона
2. Взаимодействие со щелочами.
а) НООС – СООН + NaOH → HOOC – COONa + H2O
гидроксалат Na (кислая)
б) НООС – СООН + 2NaOH → NaOOC – COONa + 2H2O
оксалат Na (средняя)
3. Реакции нуклеофильного замещения.
а) образование сложных эфиров
(при обычных условиях)
 С2Н5ОН
О
С2Н5ОН
О
НООС – С
-Н2О О – С2Н5
НООС – СООН моноэтиловый эфир щавелевой кислоты
2С2Н5ОН О О
С – С
-2Н2О Н5С2 – О О – С2Н5
диэтиловый эфир щавелевой кислоты
б) образование амидов
самостоятельно
в) образование хлорангидридов
4. Специфические реакции.
а) декарбоксилирование (для щавелевой и малоновой кислот)
 t = 200°C O
t = 200°C O
Н ООС
– СООН
H – C + CO2↑
ООС
– СООН
H – C + CO2↑
OH
муравьиная кислота
t = 150°C O
Н ООС – СН2 – СООН H3С – C + CO2↑
OH
малоновая кислота уксусная кислота
б) образование ангидридов (циклических)
т. к. по мере удлинения цепи ослабевает влияние карбоксильных групп друг на друга:
 О
О
О
О
СН2 С СН2 С
О Н t = 230°C
ОН -Н2О О
СН2 С
О СН2 С
О
янтарная кислота янтарный ангидрид
 О
О
О
О
СН2 С СН2 С
О Н
СН2 t СН2 О
ОН -Н2О
СН2 С СН2 С
О О
глутаровая кислота глутаровый ангидрид
Отдельные представители:
