- •Содержание
- •Введение
- •Раздел 1. Классы неорганических соединений
- •Раздел 2. Строение атома
- •Раздел 3. Периодический закон и периодическая система элементов д.И. Менделеева
- •Раздел 4. Химическая связь и строение молекул
- •Раздел 5. Основы термодинамики
- •Раздел 6. Скорость химической реакции
- •Раздел 7. Химическое равновесие
- •Раздел 8. Способы выражения концентрации растворов
- •Раздел 9. Электролитическая диссоциация и ионные реакции
- •Раздел 10. Гидролиз растворов солей
- •Раздел 11. Окислительно-восстановительные реакции
- •Раздел 12. Химические свойства металлов
- •Раздел 13. Гальванический элемент
- •Раздел 14. Коррозия металлов
- •Раздел 15. Органическая химия
- •Вопросы для подготовки к зачету
- •Список литературы
Раздел 14. Коррозия металлов
14.1 Для указанных в задании сплавов составьте схему электрохимической коррозии и напишите электродные уравнения катодных и анодных процессов в кислой среде. Укажите вторичный процесс и продукт коррозии.
14.2 Первый металл в данном сплаве рассмотрите в виде возможного металлического покрытия для защиты от коррозии второго металла. Определите тип покрытия, составьте схему коррозии и напишите электродные уравнения катодных и анодных процессов в нейтральной среде. Укажите вторичный процесс и продукт коррозии.
Таблица 14 - Коррозия металлов
|
Вариант |
Сплав металлов |
|
Вариант |
Сплав металлов |
|
1 |
2 |
|
1 |
2 |
|
1 |
Mg / Fe |
|
19 |
Mg / Ni |
|
2 |
Mg / Ag |
|
20 |
Al / Ag |
|
3 |
Al / Cd |
|
21 |
Al / Cr |
|
4 |
Al / Cu |
|
22 |
Ti / Fe |
|
5 |
Ti / Co |
|
23 |
Mn / Cu |
|
Продолжение таблицы 14 |
||||
|
1 |
2 |
|
1 |
2 |
|
6 |
Mn / Ni |
|
24 |
Mn / Zn |
|
7 |
Mn / Bi |
|
25 |
Cr / Cu |
|
8 |
Cr / Ag |
|
26 |
Cr / Pb |
|
9 |
Cr / Sn |
|
27 |
Zn / Fe |
|
10 |
Zn / Pb |
|
28 |
Zn / Bi |
|
11 |
Zn / Cu |
|
29 |
Fe / Co |
|
12 |
Fe / Cu |
|
30 |
Fe / Sn |
|
13 |
Fe / Ni |
|
31 |
Ni / Co |
|
14 |
Ni / Sn |
|
32 |
Ni / Ag |
|
15 |
Ni / Cu |
|
33 |
Mg / Pb |
|
16 |
Pb / Cu |
|
34 |
Pb / Bi |
|
17 |
Pb / Fe |
|
35 |
Ti / Cu |
|
18 |
Mg / Cu |
|
|
|
Раздел 15. Органическая химия
15.1 Для заданного в таблице соединения определите принадлежность к гомологическому ряду, тип гибридизации всех атомов углерода, дайте ему название по систематической номенклатуре. Укажите типы всех связей, отметьте первичные, вторичные, третичные, четвертичные атомы углерода.
15.2 Изобразите формулы всех структурных и пространственных изомеров.
15.3 Напишите реакцию данного вещества с приведенным реагентом. Рассмотрите его в качестве мономера в реакциях полимеризации и поликонденсации.
Таблица 15 - Органическая химия
|
Вариант |
Формула соединения |
Реагент |
|
1 |
2 |
3 |
|
1 |
CH3-CH2-CH2-Cl |
Н2О/ NaOH |
|
2 |
CH3-CH2-CH2-OH |
HCl / H+ |
|
3 |
CH3-CH2-CH2-COOH |
CH3-OH / H+ |
|
Продолжение таблицы 15 |
||
|
1 |
2 |
3 |
|
4 |
CH3-CH2-CH2-NH2 |
HCl |
|
5 |
CH3-CH2-CH2-CHO |
[Ag(NH3)2]OH |
|
6 |
CH3-CO-CH2-CH3 |
Cl2/ hν |
|
7 |
CH3-CH(CH3)-CH2-OH |
Na |
|
8 |
CH3-CH2-CH(C2H5)-COOH |
NaOH |
|
9 |
CH3-CH=C(C2H5)-CH3 |
HBr |
|
10 |
CH2=C(CH3)-CH3 |
H2O / H+ |
|
11 |
CH3-CH=CH-CH2-CH3 |
Br2 / н.у. |
|
12 |
CH3-CH(CH3)-CH2-CH(CH3)-CH3 |
Br2 / hν |
|
13 |
CH3-CH(CH3)-CH2-CH3 |
HNO3 (разб.) / t, p |
|
14 |
HC≡C-CH(CH3)-CH2-CH3 |
2Br2 / н.у. |
|
15 |
HC≡C-CH2-CH2-CH3 |
[Ag(NH3)2]OH |
|
16 |
CH2=CH-CH2-CH2-CH3 |
KMnO4 / Na2CO3 |
|
17 |
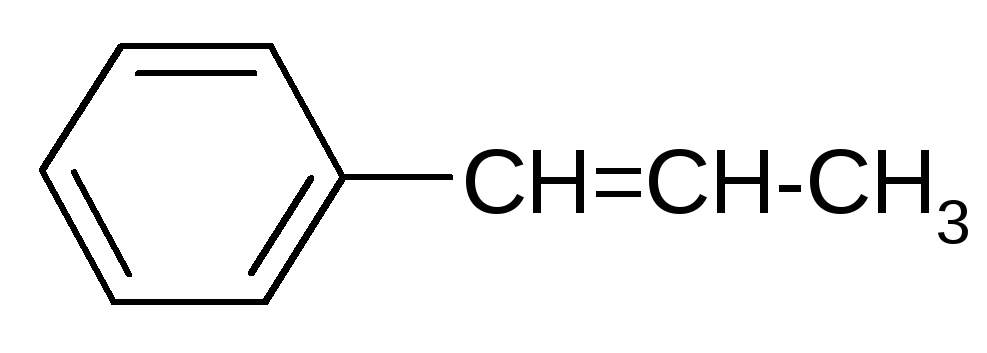
|
Br2 / hν |
|
18 |
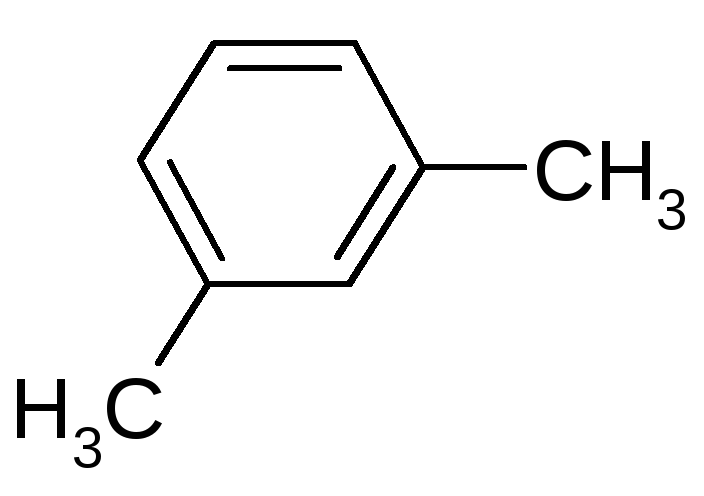
|
Br2 / н.у. |
|
19 |
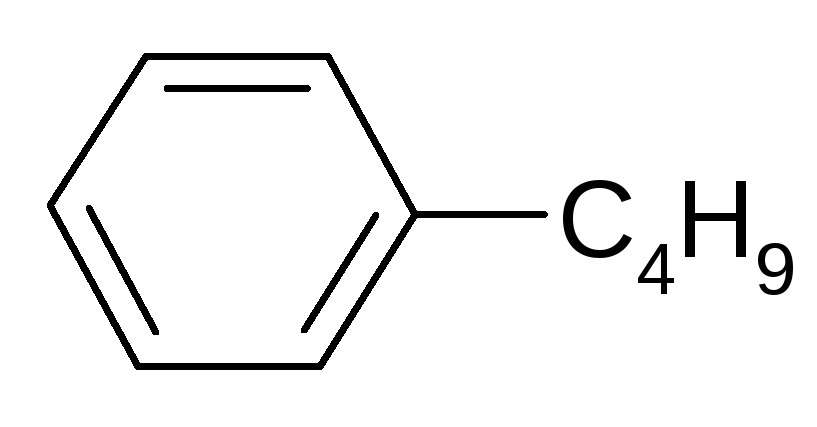
|
KMnO4 / H2SO4 |
|
20 |
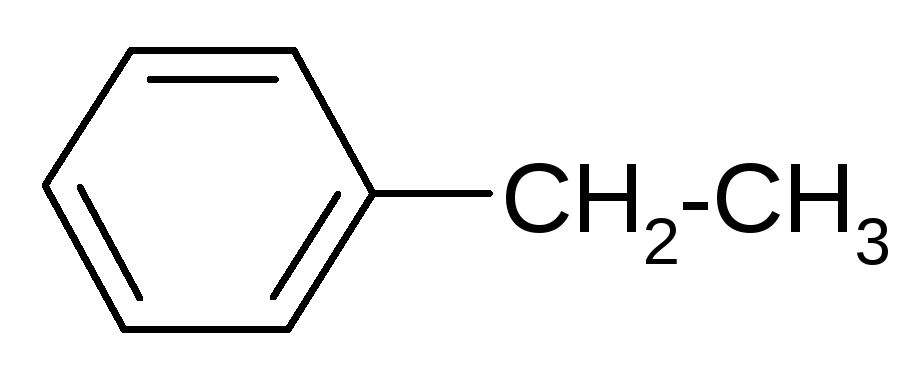
|
Cl2 / AlCl3 |
|
21 |
|
NaOH |
|
22 |
|
O2 |
|
23 |
HCHO |
[Ag(NH3)2]OH |
|
24 |
CH3-CH2-CH3 |
Cl2 / hν |
|
25 |
CH3-CH2-OH |
СH3COOH/ H+ |
|
Продолжение таблицы 15 |
||
|
1 |
2 |
3 |
|
26 |
|
СН3I / AlCl3 |
|
27 |
|
H2SO4/HNO3 |
|
28 |
|
Cl2 / hν |
|
29 |
HC≡C-CH3 |
H2O / H+,Hg2+ |
|
30 |
H2C=CH-CH=CH2 |
2Br2 / н.у. |
|
31 |
HC≡CH |
[Ag(NH3)2]OH |
|
32 |
|
Br2 / н.у. |
|
33 |
CH3-CH2-CH(C2H5)-COOH |
C3H7OH/H+ |
|
34 |
|
[Ag(NH3)2]OH |
|
35 |
|
Br2 / FeCl3 |