
Вопросы_20_2013
.pdf
Общие
1. Концентрация карбоната кальция в его насыщенном растворе составляет _____
моль/дм3 (ПРСаСО3= 4,9∙10–9) |
|
1. 4,9∙10–9 |
3. 9,8∙10–9 |
2. 3,5∙10–5 |
4. 7,0∙10–5 |
2. Концентрация сульфата бария в его насыщенном растворе составляет____
моль/дм3.
1. |
3. |
2. |
4. |
3. Наименьшей растворимостью (моль/л) обладает карбонат двухвалентного металла, значение произведения которого равно
1.3,8∙10-9 |
3.4,0∙10-10 |
2.1,8∙10-11 |
4.7,5∙10-14 |
4. Формула вещества, 0,01 М раствор которого характеризуется наибольшим
значением рН, имеет вид |
|
1.Fe(OH)2 |
3.NaHCO3 |
2.NaOH |
4.Na2SO4 |
5. Формула вещества, 0,1 М раствор которого характеризуется наименьшим значением рН, имеет вид
|
1. H2СO3 |
3. НCl |
|
2. H2S |
4. Nа2НРO4 |
6. Для 0,1 моль/дм3 раствора HCOOH рН составляет |
||
1. |
2,88 |
3. 1,38 |
2. |
2,38 |
4. 1,0 |
7. |
Значение рН 0,001 М раствора азотной кислоты ( = 1), равно…… |
|
1.1 |
|
3.0 |
|
2.2 |
|
4.3 |
|
8. Для поддержания рН > 9 применяется буферная смесь: |
|||
1. |
CH3COOH + CH3COONa |
3. |
HCOOH + HCOONa |
2. |
NH4OH + NH4Cl |
4. |
C6H5OH + C6H5OO NH4 |
9. При разбавлении ацетатного буферного раствора значение величины рН…….
1.увеличится в 2 раза
2.уменьшится в 2 раза
3.уменьшится на 2
4.не изменяется
10. Аммонийный буферный раствор (укажите формулу) предназначен для поддержания:
1. рН=0 |
3. рН<7 |
2. рН>7 |
4. рН=7 |
|
Посуда и приготовление растворов |
1.Укажите ошибку при подготовке бюретки к работе
1.Закрепили в штативе
2.Ополоснули анализируемым раствором
3.«Носик» бюретки заполнили титрантом
4.Объем титранта установили на нулевой отметке
2. Укажите ошибки при работе с пипеткой (несколько ответов):
|
1. |
Отмыли от жира |
|
|
2. |
Ополоснули титрантом |
|
|
3. |
Выдули оставшуюся в ней каплю жидкости |
|
|
4. |
По окончании работы промыли и поставили в штатив |
|
3. Для отбора пробы анализируемого раствора используют |
|||
1. |
Бюретку |
|
3. Капельную пипетку |
2. |
Пипетку Мора |
4. Мензурку |
|
4. Точную мерную посуду применяют для … (несколько ответов):
1.приготовления рабочих растворов
2.приготовления стандартных растворов
3.отбора пробы исследуемого раствора
4.добавления растворов индикаторов
5.измерения объема растворов титрантов
5.Посуда, которая ополаскивается перед титрованием титруемым раствором
1. |
мерная колба. |
4. мерная пипетка. |
2. |
колба для титрования. |
5. мерный цилиндр. |
3. |
бюретка. |
6. химический стакан |
6. Укажите вещества по точной навеске которых можно приготовить стандартный раствор (несколько вариантов):
1. CH3COOH |
3. HCl |
|
|
|
5. K2Cr2O7 |
|
2. NaOH |
4. H |
C |
O ·2H |
2 |
O |
6. MgSO4 |
|
2 |
2 |
4 |
|
|
|
7. Вещества по точной навеске которых можно приготовить стандартный раствор:
1. CH3COOH |
4. H2C2O4·2H2O |
2. NaOH |
5. K2Cr2O7 |
3. HCl |
6. MgSO4 |
8.Укажите весы и мерную посуду для приготовления стандартного раствора.
1.Технические весы, мерный цилиндр.
2.Аналитические весы, мерный цилиндр.
3.Аналитические весы, мерная колба.
4.Технические весы, мерная колба.
9. Химическая посуда для разбавления 0,2000 моль/дм3 раствора Н2С2O4
1. |
мерный цилиндр |
2. |
мерная пипетка |
3. |
коническая колба |
4. |
бюретка |
5. |
мерная колба |
6. |
химический стакан |
10. Способ приготовления раствора гидроксида натрия: Необходимый объем концентрированного раствора
1.отмерить мерным цилиндром, поместить в мерную колбу и довести раствор до метки дистиллированной водой.
2.мерной пробиркой перенести в мерный цилиндр и добавить дистиллированную воду до требуемого объема.
3.пипеткой перенести в мерную колбу и довести объем раствора до метки дистиллированной водой.
4.пипеткой перенести в мерный цилиндр и добавить дистиллированную воду до требуемого объема.
11. Титр это концентрация, показывающая сколько…
1.…миллиграммов вещества, содержащееся в 1 дм3 раствора.
1.... граммов вещества, содержащееся в 1 дм3 раствора.
2.…граммов вещества, содержащееся в 1 см3 раствора.
3.…граммов вещества, содержащееся в 100 г раствора.
12.Масса нитрата натрия, необходимая для приготовления 400 см3 раствора с молярной концентрацией вещества 0,5 моль/дм3, составляет ____г (с точностью до целого значения)
1. 15 |
3. 68 |
2. 34 |
4. 17 |
13. |
Рассчитайте титр (г/см3) раствора безводной щавелевой кислоты с молярной |
|
концентрацией эквивалента 0,0100 моль/дм3. |
||
|
1. 4,5·10–2. |
3. 9,0·10–3. |
|
2. 4,5·10–4. |
4. 9,0·10–4. |
14. |
Массовая доля сульфата меди в растворе, полученном при растворении 50 г |
|
СuSO4 в 200 г воды, составляет ____% (с точностью до целого значения) |
||
|
1. 20 |
3. 10 |
|
2. 15 |
4. 25 |
15. Масса медного купороса CuSO4∙5H2O , необходимая для приготовления 500 г раствора с массовой долей сульфата меди 16% равна….
1.150
2.50
3.125
4.160
16. Укажите вместимость (см3) мерной колбы для приготовления из фиксанала.
раствора I2 |
с молярной концентрацией эквивалента 0,05 моль/дм3. |
||
1. |
200. |
3. |
50. |
2. 2000. 4. 1000.
17. Навеску гидроксида калия массой 28 г растворили и разбавили водой до объема 250 мл. Молярная концентрация эквивалентов КОН в полученном растворе составляет ________ моль/л. (с точностью до целого значения)
1. |
2 |
3. |
3 |
2. |
1 |
4. |
4 |
18. Масса медного купороса, необходимая для приготовления 2 л 0,1 М раствора сульфата меди (II), составляет ________ г.
1. 32 |
3. 25 |
2. 50 |
4. 16 |
19. Какой объем воды (см3) необходимо добавить к 20 см3 0,1 моль/дм3 раствора
уксусной кислоты, чтобы получить |
0,05 моль/дм3 раствор? |
|
17. 10. |
19. 15. |
|
18. 20. |
20. 40. |
|
20. Рассчитайте навеску (m, г) NaCl, необходимую для приготовления 500 см3 0,1 моль/дм3 раствора.
21. Рассчитайте титр раствора щавелевой кислоты с молярной концентрацией эквивалента 0,05 моль/дм3.
22. Масса гидроксида калия, содержащего в 10 л его раствора, значение рН которого равно 11, составляет __________ г ( = 1).
1.0,56 |
3.0,112 |
2.0,28 |
4.0,56 |
23. Масса азотной кислоты, содержащаяся в 5 л ее раствора, значение рН которого равно 3, составляет __________ г ( = 1).
1.0,126 |
3.0,063 |
2.0,315 |
4.0,56 |
24. Масса кристаллогидрата (Na2CO3 ∙10Н2О), необходимая для приготовления 500 г раствора карбоната натрия с массовой долей растворенного вещества
10,6%, составляет _________ г.
1.286
2.106
3.143
4.212
25. Раствор гидроксида бария массой 200 г и массовой долей растворенного вещества 17,1 % разбавили водой до объема 400 мл. Молярная концентрация эквивалентов Ва(ОН)2 в полученном растворе составляет ________ моль/л.
1.2
2.0,1
3.0,5
4.1
Титрование (общие)
1. Точка эквивалентности – это такой момент в процессе титрования, когда:
1.Индикатор поменял окраску;
2.Титрант и титруемое вещество прореагировали между собой в эквивалентных количествах;
3.Вещества прореагировали между собой в равных количествах;
4.Число моль – эквивалентов титранта и титруемого вещества обратно пропорционально;
2.Кривые титрования строятся для:
1.определения концентрации титранта;
2.определения объема титранта;
3.выбора индикатора;
3. установления области скачка;
3. Укажите соответствие между титриметрическим методом анализа и координатами кривой титрования
1. |
Осадительное титрование |
5. |
рН - Vтитранта |
2. |
Комплексонометрия |
6. |
Е - Vтитранта |
3. |
Кислотно-основное |
7. |
рМе - Vтитранта |
|
титрование |
8. |
рCl - Vтитранта |
4. |
Редоксиметрия |
|
|
4. Укажите соответствие между титриметрическим методом анализа и реакцией,
находящейся в его основе: |
|
|
|
1. |
Кислотно-основной |
5. |
Ме2++Cl-= МеCl↓ |
2. |
Редоксиметрический |
6. |
Red1+Ox2=Ox1+ Red2 |
3. |
Комплексонометрический |
7. |
Ме2++Na2H2Y=Na2МеY+2H+ |
4. |
Осадительный |
8. |
H++OH =H2О |
5. Соответствие метода, индикатора и изменения цвета титруемого раствора при фиксировании точки эквивалентности:
1. |
Алкалиметрия |
|
1. |
Эриохромовый черный Т |
|
1. |
Желтый – красный |
2. |
Комплексонометрия |
|
2. |
Метиловый оранжевый |
|
2. |
Бесцветный – розовый |
3. |
Перманганатометрия |
|
3. |
Безиндикаторное титрование |
|
3. |
Белый – кирпично-красный |
4. |
Метод Мора |
|
4. |
Крахмал |
|
4. |
Бесцветный – розовый |
5. |
Ацидиметрия |
|
5. |
Фенолфталеин |
|
5.Винно-красный – синий |
|
6. Соответствие метода, |
титранта |
и |
стандартного вещества: |
||||||
1. |
Алкалиметрия |
|
|
1. HCl |
|
|
|
1. |
K2Cr2O7 |
2. |
Комплексонометрия |
|
|
2. NaOH |
|
|
|
2. |
K2CrO4 |
3. |
Иодометрия |
|
|
3. AgNO3 |
|
|
|
3. |
Na2B4O7 |
4. Метод Мора |
|
4. Na2S2O3 |
|
4. H2C2O4 |
5.Ацидиметрия |
|
5. Na2H2Y |
|
5. NaCl |
Кислотно-основное титрование
1. В основе кислотно-основного титрования находится реакция:
1.H++OH =H2O
2.Ag++Cl-= AgCl↓
3.J2+2S2O32-=S4O62-+2J- 4.Ca2++Na2H2Y= Na2CaY+2Н+
2. В процессе кислотно-основного титрования в растворе изменяется (несколько ответов):
1. |
pH |
3. |
рК; |
5. |
рТ; |
2. |
Е; |
4. |
pМе; |
6. |
СН+; |
3. Титрант в кислотно-основном методе титрования (несколько вариантов):
1.Сильное основание
2.Сильная кислота
3.Слабая кислота
4.Сильный восстановитель
5.Комплексон ΙΙΙ
4. Титрант метода кислотно-основного титрования |
|
||
1. |
Сильный восстановитель |
4. |
Слабый окислитель |
2. |
Сильное основание |
5. |
Комплексон III |
3. |
Слабое основание |
6. |
Иод |
5. Методом кислотно-основного титрования в растворе можно определить
1. NaCl |
|
3. Na2C2O4 |
|
|
2. KNO3 |
|
4. K2SO4 |
|
|
6. Ацидиметрически можно оттитровать: |
|
|
||
1. NaOH, . NH4ОН |
3. |
НCl |
5. |
Н2С2О4, FeSO4 |
2. NH4Cl, NaCl |
4. |
СН3СООNa, NaCl |
6. |
CaCl2, MgCl2 |
7. Задача протолитометрии, решаемая в присутствии индикатора, константа ионизации которого Кi = 1·10–5
1. |
NH4OH + НСl. |
3. |
NaОН + Н2SO4. |
2. |
НСl + КOH. |
4. |
NaOH + НСООН. |
8. Задача, решаемая в протолитометрии в присутствии индикатора с Кi=10–4
1.H2C2O4+ NaOH
2.NH4OH +HCl
3.HCOOH + NaOH
4.NH4OH + CH3COOH
9. Фиксирование точки эквивалентности при титровании раствора гидроксида калия раствором серной кислоты в присутствии метилового оранжевого производят при достижении титруемым раствором …… цвета.
1.розового
2.оранжевого
3.красного
4.желтого
10. Формула соли, в водном растворе которой индикатор фенолфталеин приобретает малиновую окраску, имеет вид
1.К2НРО4 |
|
3KNO3 |
|
2К2SO4 |
|
4FeSO4 |
|
11. Укажите систему, для |
которой точка эквивалентности находится |
||
в кислой среде. |
|
|
|
1. |
НСl + NaOH. |
2. |
КОН + Н2SO4. |
3. |
NH4OH + НСl. |
4. |
NaOH + СН3СООН. |
12. При титровании раствора молочной кислоты раствором NaOH используют
индикатор: |
|
|
|
1. |
Фенолфталеин |
3. |
Эриохромовый черный |
2. |
Метиловый оранжевый |
4. |
Дифениламин |
Ответ обоснуйте.
13. Выберите титрант и индикатор для определения в растворе CH3COOH:
1.HCl и метиловый оранжевый
2.KOH и метиловый оранжевый
3.Na2B4O7 и фенолфталеин
4.KOH и фенолфталеин
14. При определении концентрации щелочи в растворе методом кислотноосновного титрования в качестве индикатора используется …
1.мурексид |
3.эриохромовый черный |
2.фенолфталеин |
4.дифениламин |
15. В чем состоит действие ауксохромных групп?
1.Сообщают окраску.
2.Стабилизируют окраску.
3.Усиливают окраску.
4.Ослабляют окраску.
16. Фиксирование точки эквивалентности при титровании раствора гидроксида калия раствором серной кислоты в присутствии метилового оранжевого производят при достижении титруемым раствором …… цвета.
1. |
розового |
3. |
красного |
2. |
оранжевого |
4. |
желтого |
17. Величина pH в точке эквивалентности больше 7 при титровании…
1.Сильной кислоты сильным основанием
2.Слабой кислоты сильным основанием
3.Сильного основания сильной кислотой
4.Слабого основания сильной кислотой
18.Объем раствора гидроксида натрия с молярной концентрацией эквивалентов 0,1 моль/л, необходимый для нейтрализации 15 мл раствора серной кислоты с молярной концентрацией эквивалентов 0,2 моль/л, равен ________ мл.
1. |
45 |
3. |
20 |
2. |
30 |
4. |
15 |
19. Объем 0,1 моль/дм3 раствора HNO3, необходимый для нейтрализации раствора гидроксида бария, содержащего 0,171 г Ва(ОН)2, равен ____ см3 (ответ с точностью до целого значения)
20. При кислотно-основном титровании 100 мл минеральной воды, содержащей гидрокарбонаты кальция и магния, раствором соляной кислоты с молярной концентрацией эквивалента 0,05 моль/дм3 затрачено 13,90 см3 титранта. Рассчитать массу гидрокарбонат-ионов, содержащуюся в 1 л этого раствора.
21. Рассчитать значение рН в точке эквивалентности при титровании раствором гидроксида натрия раствор уксусной кислоты и выбрать наиболее эффективный индикатор (ответ обосновать).
1.Метиловый оранжевый (∆pH = 3,1–4,4)
2.Метиловый красный (∆pH = 4,4–6,2)
3.Бромтимоловый синий (∆pH = 6,0–7,6)
4.Фенолфталеин (∆pH = 8,2–9,8)
5.Тимолфталеин (∆pH = 9,3–10,5)
22.Рассчитайте массу двуводной щавелевой кислоты в 500 см3 раствора, если на титрование 10,0 см3 этого раствора затрачено 10,5 см3 0,1 моль/дм3 раствора
NaOH:
23. Объем раствора серной кислоты с молярной концентрацией эквивалентов 0,05 моль/л, необходимый для нейтрализации 15 мл раствора гидроксида натрия с молярной концентрацией эквивалентов 0,1 моль/л, равен ______ мл (с точностью до точного значения).
24. На титрование 15 см3 раствора гидроксида натрия затрачено 13,5 см3 раствора соляной кислоты с концентрацией эквивалента 0,1 моль/дм3. Рассчитать массу гидрокисда натрия в 1 дм3 этого раствора (ответ записать с точностью до десятых долей).
25. Для нейтрализации 25 мл раствора гидроксида калия с молярной концентрацией эквивалентов 0,2 моль/л требуется ________ мл раствора серной кислоты с молярной концентрацией эквивалентов 0,1 моль/л.
1.50 |
3.12,5 |
2.100 |
4.25 |
26. Объем раствора гидроксида натрия с молярной концентрацией эквивалентов 0,1 моль/л, необходимый для нейтрализации 15 мл раствора серной кислоты с молярной концентрацией эквивалентов 0,2 моль/л, равен ________ мл.
1.45 |
3.20 |
2.30 |
4.15 |
27. Объем 0,1 М раствора HNO3, необходимый для нейтрализации раствора гидроксида калия, содержащего 0,084 г КОН, равен ________ мл.
1.84 |
3.15 |
2.42 |
4.150 |
28. На титрование 25 см3 раствора гидроксида калия затрачено 20 см3 раствора азотной кислоты с молярной концентрацией 0,1 моль/ дм3. Масса щелочи ( г ) в 500 см3 этого раствора равна
1. |
1,12 |
3. 2,24 |
2. |
5,6 |
4. 4,48 |
29. На титрование 20 см3 раствора NaOH израсходовано 25 см3 раствора HCl c молярной концентрацией 0.08 моль/дм3 . Масса щелочи в 200 см3 этого раствора
равна _____г. |
|
1. 2,4 |
3. 3,2 |
2. 0,8 |
4. 1,6 |
30. Рассчитать объем раствора серной кислоты с концентрацией эквивалента 0,2 моль/дм3, затраченный на титрование 20 см3 раствора гидроксида калия с концентрацией 0,15 моль/дм3 (с точностью до точного значения).
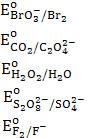
Окислительно-восстановительное титрование
1. 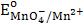 = 1,51 В. Восстановить
= 1,51 В. Восстановить  - в кислой среде (ответ поясните)
- в кислой среде (ответ поясните)
может… |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
1. |
KBrO3; |
|
|
|
|
|
|
|
|
|
|
= 1,52 В |
|
|
|
|
|
|
||||||||
2. Na2C2O4; |
|
|
|
|
|
|
|
|
|
= 0,49 B |
|
|
|
|
|
|
||||||||||
3. H2O2; |
|
|
|
|
|
|
|
|
|
|
|
= 0,77 B |
|
|
|
|
|
|
||||||||
4. Na2S4O8; |
|
|
|
|
|
|
|
|
|
= 2,0 B |
|
|
|
|
|
|
||||||||||
5. |
F ; |
|
|
|
|
|
|
|
|
|
|
|
|
-= 2,87 B |
|
|
|
|
|
|
||||||
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2. Какой ион можно окислить раствором KMnO4 в кислой среде? |
EoMnO / Mn 2 = + |
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
1,51 В. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
1. |
Bi3+; |
|
|
EoBiO |
/ BiO = + 1,80 B. |
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2. NO2–; |
|
Eo |
|
|
|
|
|
|
= + 0,94 B. |
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
NO / NO |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
3 |
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3. SO42–; |
|
Eo |
O2 |
|
|
|
2 |
= + 2,01 B. |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
S |
/ SO |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
2 |
8 |
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
4. |
F–; |
|
|
|
|
EoF |
/ 2F = + 2,87 B. |
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3. Вещество, которое нельзя восстановить действием Na2S2O3. |
|
|||||||||||||||||||||||||
o |
|
2 |
|
|
|
O2 |
= + 0,09 В. |
|
|
|
|
|
|
|
|
|
|
|||||||||
S |
O |
/ 2S |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
4 |
|
6 |
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1. |
CO2; |
|
|
o |
|
|
|
|
|
|
O2 |
= 0,49 B. |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
2CO |
2 |
/ C |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
4 |
|
|
|
|
|
|
|
|
||
|
2. |
I2; |
|
|
|
|
E o |
|
|
|
|
|
= + 0,54 B . |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
I 2 / 2I |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
3. |
FeCl ; |
Eo |
|
|
|
|
|
|
|
= + 0,77 B. |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
3 |
|
|
Fe3 / Fe2 |
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
4. |
KMnO4; |
EoMnO / Mn 2 = + 1,51 B. |
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
4. |
|
В |
|
|
какой |
последовательности |
|
окисляются |
ионы |
перманганатом? |
||||||||||||||||
Eo |
|
|
|
2 |
|
= + 1,51 В. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
MnO |
/ Mn |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
o |
|
|
|
|
|
|
= + 0,15 В, |
|
о |
|
/ Cr 2 |
= – 0,41 В, |
|
|
|
|||||||||||
|
Sn 4 / Sn 2 |
|
|
|
|
|
|
|
|
|
|
Cr3 |
|
|
|
|
|
|
||||||||
Eo |
|
/ Fe2 |
= + 0,77 В. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
Fe3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
1. |
Fe2+, Sn2+, Cr2+. |
|
|
|
|
3. |
Sn2+, |
Cr2+, Fe2+. |
|
|
|
||||||||||||||
|
2. |
Cr2+, Fe2+, Sn2+. |
|
|
|
|
4. |
Cr2+, |
Sn2+, Fe2+. |
|
|
|
||||||||||||||
5. Действием азотной кислоты ( о |
|
|
= + 0,94 В) можно окислить: |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NO / HNO |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
2 |
|
|
|
|
|
|
|
1. Mn2+ ; E о |
|
|
|
|
2 |
= + 1,51 В. |
|
|
3. F–; Eо |
= + 2,87 В. |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
Mn O / Mn |
|
|
|
|
|
|
|
|
F / 2F |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
2. Br–; |
E о |
|
|
|
= + 1,45 В. |
|
|
4. I–; Eо |
/ 2I |
= + 0,54 В. |
|
||||||||||||
|
|
|
|
|
|
|
|
|
BrO / Br |
|
|
|
|
|
|
|
|
|
|
|
I |
|
|
|||
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
6. Методом прямого перманганатометрического титрования в растворе можно определить (несколько ответов)
1.сульфат железа (II)
2.дихромат калия
