
Вопросы_20_2013
.pdf3.щавелевую кислоту
4.уксусную кислоту
7. Способ фиксирования ТЭ в перманганатометрии
1.применение специфического индикатора
2.безиндикаторное титрование
3.применение редокс-индикатора
4.применение фенолфталеина
8. Способ фиксирования ТЭ в перманганатометрии:
1. |
рН-индикатор; |
3. |
безиндикаторный; |
2. |
металлоиндикатор; |
4. |
редокс-индикатор |
9. Найдите стехиометрический коэффициент перед окислителем в реакции
KMnO4 + H2C2O4 + H2SO4 |
→ MnSO4 + CO2 + + K2SO4 + H2O. |
||
1. |
10. |
3. |
2. |
2. |
1. |
4. |
5. |
4. K2SO4
5. H2O
6. K2MnO4
Напишите уравнение реакции, расставьте коэффициенты.
11. Титрант в перманганатометрии: |
|
1.KMnO4; |
4.Na2S2O3; |
2.MnSO4; |
5.Na2S2O3; |
3.Fe SO4; |
6.KBrO3; |
12.Укажите стехиометрический коэффициенты перед окислителем в реакции
FeSO4 + KMnO4 + H2SO4
13.Найдите стехиометрический коэффициент перед восстановителем в реакции
KMnO4 + FeSO4 + H2SO4 |
→ MnSO4 + Fe2 (SO4) 3 + K2SO4 + H2O. |
||
1. |
10. |
3. |
2. |
2. |
1. |
4. |
5. |
14. Найдите стехиометрический коэффициент перед окислителем в реакции
KMnO4 + H2C2O4 + H2SO4 |
→ MnSO4 + CO2 + + K2SO4 + H2O. |
|||
1. |
10. |
3. |
2. |
|
2. |
1. |
4. |
5. |
|
15. Продукты реакции Н2С2O4+KMnO4+H2SO4→ |
|
|||
1. |
СО2 |
|
4. |
K2SO4 |
2. |
MnSO4 |
|
5. |
H2O |
3. |
MnO2 |
|
6. |
K2MnO4 |
Напишите уравнение реакции, расставьте коэффициенты.
16. Скачок на кривой титрования в редоксиметрии при использовании в качестве индикатора эриоглауцина (Е0ind = 1,00 В) составляет
1. |
0,60….....1,00 |
3. |
1,10….....1,31 |
2. |
0,80….....1,40 |
4. |
0,60….....0,90 |
17. В иодометрии титрантами являются растворы…
1.I2
2.KI
3.Na2S2O3
4.KIO3
18. Способ фиксирования ТЭ в иодометрии:
5.рН-индикатор;
6.специфический индикатор крахмал;
7.безиндикаторный;
4. редокс-индикатор
|
Комплексонометрия |
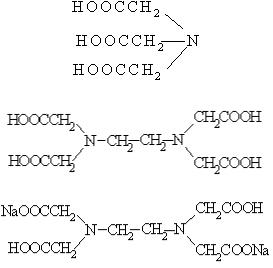
1. Соответствие между формулами комплексонов и их названиями: |
|
1. |
1. Двунатриевая соль |
этилендиаминтетрауксусной кислоты (ЭДТА), комплексон III
2. |
2. Нитрилотриуксусная кислота (НТУ), |
|
комплексон I |
3. |
3. Этилендиаминтетрауксусная кислота |
|
(ЭДТУ), комплексон II |
2. Катионы,определяемые методом комплексонометрии |
|
|
|||
1. |
K+ |
2. |
Mg2+ |
3. |
H+ |
4. |
Ca2+ |
5. |
Na+ |
6. |
NH4+ |
3. Комплексонометрическим методом можно определить в растворе:
1. |
Ca2+, Mg2+ |
3. |
K+, Na+ |
2. |
Ca2+, Na2+ |
4. |
Cu2+, K+ |
Написать уравнение реакции комплексообразования, находящейся в основе метода
4. Закончите уравнение стандартизации раствора комплексона III:
Мg2+ + Н2Y2–…

1. |
МgY2– + 2Н+. |
3. ... |
МgY– + 2Н+. |
2. ... |
МgY– + Н+. |
4. ... |
МgY + 2Н+. |
5. Буферная смесь, применяемая в комплексонометрии, для поддержания pH>9
1.NH4OH+NH4Cl
2.CH3COOH+CH3COONa
3.HCOOH+HCOONa
4.C6H5OOH+C6H5OONH4
6.Точку эквивалентности в комплексонометрии фиксируют,
1.примененяя специфический индикатор
2.безиндикаторным способом
3.применяя фенолфталеин
4.примененяя металлоиндикаторы
7.Металлиндикаторы – это аналитические реагенты, образующие окрашенные комплексы с …
1.титрантом
2.титрируемым ионом металла
3.ионом, входящим в состав буферной смеси
8.Принцип действия металлоиндикатора при титровании заключается в изменении окраски раствора вблизи точки эквивалентности в результате
1.разрушения комплексоната металла
2.образования комплекса металлоиндикатора с ионом титруемого металла
3.разрушения комплекса металлоиндикатора с ионом титруемого металла
4.образования комплексоната металла
9. При прямом комплексонометрическом титровании окраска раствора изменяется, потому что в конечной точке титрования протекает реакция…
1.Меn+ + Ind- = МеIndn-1
2.МеIndn-1 +H2Y2 - = MеYn-4 + HInd + H+
3.Меn+ + H2Y2- = MеYn-4 + 2H+
10.В комплексонометрическом титровании окраска раствора изменяется, потому
что в конечной точке титрования протекает реакция…
1.Меn+ + Ind- = МеIndn-1
2.МеIndn-1 +H2Y2 - = MеYn-4 + HInd + H+
3.Меn+ + H2Y2- = MеYn-4 + 2H+
11.Соли, вызывающие постоянную жесткость воды
1. CaCl2, BaCl2. |
. |
2.Na2SO4, MgSO4.
3.CaCl2, MgSO4.
4.K2CO3, CaCO3.
12. Общая жесткость воды определяется присутствием
1.сульфатов, карбонатов К+ и Fe3+
2.сульфатов, карбонатов, гидрокарбонатов Mg2+ и Ca2+
3.хлоридов, гидрокарбонатов Mg2+ и Zn2+
4.карбонатов, гидрокарбонатов Са2+ и Al3+
13. В аналитических лабораториях общую жесткость воды определяют методом
______________титрования. |
|
1. кислотно-основного |
3. осадительного |
2. окислительно-восстановительного |
4. комплексонометрического |
14. Укажите метод и индикатор для определения жесткости воды:
1.Кислотно-основное титрование, эриохромовый черный Т;
2.Комплексонометрия, эриохромовый черный Т;
3.Йодометрия, крахмал;
4.Аргентометрия, хромат калия;
Напишите уравнение реакции образования комплексоната кальция.
15. Среда, в которой возможно комплексонометрическое определение Са2+ и Mg2+.
1. |
щелочная. |
3. |
кислая. |
2. |
нейтральная. |
4. |
слабокислая. |
16. При определении жесткости воды в колбу для титрования помещают …
1.раствор сульфата магния мерной пипеткой, аммонийный буферный раствор мерным цилиндром, эриохромовый черный Т на кончике шпателя;
2.раствор сульфата магния и аммонийный буферный раствор мерными цилиндрами, эриохромовый черный Т на кончике шпателя;
3.воду и аммонийный буферный раствор мерными пипетками, эриохромовый черный Т на кончике шпателя;
4.воду мерной пипеткой, аммонийный буферный раствор мерным цилиндром, эриохромовый черный Т на кончике шпателя;
17. Фиксирование точки эквивалентности при титровании сточной воды, содержащей ионы кальция, раствором комплексона III в присутствии аммонийного буферного раствора и индикатора эриохромового черного Т производят при достижении титруемым раствором …… цвета.
|
|
1. |
розового |
|
3. |
красного |
|
|
2. |
оранжевого |
4. |
синего |
|
18. Реакция образования комплексоната железа (III) при рН = 2 |
||||||
1. |
Fe 3+ + H2Y 2- |
FeY – + 2 H + |
|
|
||
2. |
Fe3+ + HY3- |
FeY– + H+ |
|
|
||
3. |
Fe3+ |
+ Y4- |
FeY– |
|
|
|
4. |
Fe3+ |
+ H3Y- |
FeY– + 3 H+ |
|
|
|
5. |
Fe 3+ + H4Y |
FeY – + 4 H + |
|
|
||

19. Комплексонатами называют ...
1.металлоиндикаторы
2.титранты в комплексонометрии
3.определяемые вещества в комплексонометрии
4.циклические комплексные соединения комплексонов с металлами
5.буферные растворы в комплексонометрии
20. Укажите правильную формулу комплексоната алюминия:
1 |
|
ООС–Н2С |
|
|
|
СН2 –СООNa |
||||
|
||||||||||
|
|
N–СН2 –СН2– N |
||||||||
2. |
NaООС–Н2С |
Al |
|
|
СН2 –СОО |
|
|
|
|
|
|
|
|||||||||
|
|
|
|
СН2 –СОО |
|
|
||||
|
|
|
|
|
|
|
||||
ООС–Н2С |
|
|
|
|
||||||
|
|
N–СН2 –СН2– N |
|
|
||||||
|
NaООС–Н2С |
|
Al |
|
СН2 –СОО |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
||
3. |
|
NaООС–Н2С |
|
|
|
СН2 –СООAl |
||||
|
|
|
N–СН2 –СН2– N |
|||||||
|
|
AlООС–Н2С |
|
|
|
СН2 –СООAl. |
||||
4. |
|
НООС–Н2С |
|
|
|
СН2 –СООAl |
||||
|
|
|
|
N–СН2 –СН2– N |
||||||
|
|
NaООС– Н2С |
|
|
|
СН2 –СООН . |
||||
21. Укажите правильную формулу комплексоната магния:
1. |
|
ООС–Н2С |
|
|
СН2 –СООNa |
||||
|
|||||||||
|
|
N–СН2 –СН2– N |
|||||||
|
NaООС–Н2С |
Мg |
|
СН2 –СОО |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
2. |
|
ООС–Н2С |
|
СН2 –СОО |
|||||
|
|
|
|
|
|||||
|
|
|
|
||||||
|
|
N–СН2 –СН2– N |
|
|
|||||
|
NaООС–Н2С |
Мg |
|
СН2 –СОО |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
||
3. |
|
NaООС–Н2С |
|
|
СН2 –СООMg |
||||
|
|
|
N–СН2 –СН2– N |
||||||
|
|
MgООС–Н2С |
|
|
СН2 –СООNa. |
||||
4. |
|
НООС–Н2С |
|
|
СН2 –СООMg |
||||
|
|
|
N–СН2 –СН2– N |
||||||
|
|
NaООС– Н2С |
|
|
СН2 –СООН . |
||||
22. Уравнение образования комплекса Ме2+ с комплексоном III:
Ме2+ + Н2Y2– |
… |
||
1. |
... |
МеY2– + 2Н+. |
|
2. ... |
|
МеY + 2Н+. |
|
3. ... |
|
МеY– + Н+. |
|
4. |
… |
|
МеY2–+ Н+. |
23. На титрование 10,0 см3 минеральной воды затрачено 10,50 см3 0,020 моль/дм3
раствора комплексона |
III. Рассчитайте жесткость анализируемой |
воды |
||
(ммоль/дм3). |
|
|
|
|
1. |
21,0 |
3. |
10,5 |
|
2. |
42,0 |
4. |
5,25 |
|
Осадительное титрование
1. Титрант и индикатор при определении хлорид-ионов в растворе методом Мора
1. AgNO3, Fe(III) |
3. AgNO3, K2CrO4 |
2. I2, крахмал |
4. KSCN, Fe(III) |
Ответ пояснить уравнениями реакций. |
|
2. Индикатор метода Мора |
|
1. К2Cr2O7 |
3. K2CrO4 |
2. AgNO3 |
4. FeNH4(SO4)212H2O |
3. Укажите титрант, стандартное вещество и индикатор при определении иодидиона в растворе методом Мора
1.Na2S2O3, K2CrO4, крахмал
2.AgNO3, Na2S2O3, дифениламин
3.K2CrO4, H2C2O4, эозин
4.AgNO3, NaCl, K2CrO4
4. Титрант и индикатор метода Фольгарда |
|
||||
1. AgNO3, K2CrO4 |
3 NH4SCN, K2CrO4 |
||||
2. NH4SCN, NH4Fe(SO4)2 |
4. Na2S2O3, крахмал |
||||
5. Титрант и индикатор метода Фольгарда |
|
||||
1. Н |
Y2– и К |
Cr O |
3. KSCN и K |
CrO4 |
|
2 |
2 |
2 |
7 |
2 |
|
2. AgNO3 и крахмал |
4. КSCN и FeNH4(SO4)212H2O |
||||
6. Фиксирование точки эквивалентности при титровании сточной воды, содержащей бромид калия, раствором нитрата серебра в присутствии хромата калия в качестве индикатора производят при достижении титруемым раствором …… цвета.
1. достижении титруемым раствором красного цвета; 2. переходе цвета титруемой взвеси из белого в красный; 3. выпадении белого осадка; 4. достижении титруемым красного цвета.
7. Фиксирование точки эквивалентности при титровании сточной воды, содержащей бромид натрия, раствором нитрата серебра в присутствии хромата калия в качестве индикатора производят при...
1. достижении титруемым раствором красного цвета;
2. переходе цвета титруемой взвеси из белого в красный;
3.выпадении белого осадка;
4.достижении титруемым раствором синего цвета.
8.Объем 0,1 моль/дм3 раствора NaOH, необходимый для осаждения меди в виде гидроксида из 50 см3 0,05 моль/дм3 раствора сульфата меди (II), равен ____ см3 (ответ с точностью до целого значения)
9. При добавлении избытка раствора серной кислоты к 20 мл 0,1 М раствора ВаCl2 образуется осадок массой ________ мг.
1.0,233
2.0,208
3.0,416
4.0,466
10.Объем 0,1 М раствора NаOН, необходимый для осаждения железа в виде гидроксида из 20 мл 0,05 М раствора нитрата железа (III), равен ________ мл (с точностью до точного значения).
11.При добавлении избытка раствора серной кислоты к 20 мл 0,1 М раствора
ВаCl2 образуется осадок массой ________ мг.
1.0,233
2.0,208
3.0,416
4.0,466
12.Объем раствора 0,1 М хлорида бария, необходимый для осаждения сульфатионов из 200 мл 0,025 М раствора серной кислоты, равен ______ мл (с точностью до точного значения).
13.Объем 0,1 моль/дм3 NaOH, необходимый для осаждения меди в виде гидроксида из 50 см3 раствора сульфата меди (II) с концентрацией 0,05 моль/дм3, равен ____
см3 (ответ с точностью до целого значения).
14. |
При добавлении избытка разбавленного раствора карбоната натрия к 50 см3 |
|
0,1 |
моль/дм3 |
раствора CaCl2 образуется осадок массой ____ г |
|
1.0,5 |
3.0,75 |
|
2.0,25 |
4.1,0 |
15. Объем раствора 0,1 М хлорида бария, необходимый для осаждения сульфатионов из 200 мл 0,025 М раствора серной кислоты, равен ______ мл (с точностью до точного значения).
Введите ответ:
16. Объем раствора 0,1 М хлорида бария, необходимый для осаждения сульфатионов из 200 мл 0,025 М раствора серной кислоты, равен ______ мл (с точностью до точного значения).
17. При сливании 300 мл 0,1 М раствора СаCl2 и 150 мл 0,25 М раствора Na2СО3 образуется осадок массой _________ г.
Введите ответ c точностью до целого значения.
