
- •Вопрос 1 Предмет и задачи биологической химии. Объекты биохимического исследования. Место биохимии среди других биологических дисциплин. Основные разделы и направления в биохимии.
- •Вопрос 4 Простые и сложные белки. Строение, характеристика отдельных групп, биологическая роль
- •Вопрос 5 Нуклеопротеины, химическое строение днк, рнк, биологическая роль
- •Вопрос 6 Связи, формирующие первичную и вторичную структуры днк и рнк. Виды рнк
- •Виды рнк
- •Вопрос 7 История открытия и изучения витаминов. Классификация витаминов и функции витаминов
- •Вопрос 8. Алиментарные и вторичные авитаминозы и гиповитаминозы. Причины (экзо-, эндогенные). Гипервитаминозы
- •Вопрос 9 Витамин с, химическое строение, явления недостаточности, биологическая роль. Участие витамина «с» в синтезе коллагена. Реакция гидроксилирования пролина и лизина
- •Вопрос 10 Витамин рр, строение и биологическая роль. Над-зависимые дегидрогеназы.
- •Вопрос 11 Витамин в1, строение, участие в обмене веществ. Тиаминдифосфат ( тдф), проявление авитаминоза. Суточная
- •Вопрос 12 Витамин в2, строение, роль (фад, фмн), суточная потребность, признаки авитаминоза
- •Вопрос 13 Витамин в6: пиридоксин, пиридоксаль, пиридоксамин. Строение и биологическая роль. Явления недостаточности. Суточная потребность.
- •Вопрос 14 Витамин «а», химическое строение, суточная потребность. Авитаминоз, гипервитаминоз, проявления. Провитамины.
- •Вопрос 16 Ферменты. Биологическая роль. Классификация и номенклатура ферментов
- •Вопрос 17 Механизм действия ферментов. Образование фермент-субстратных комплексов. Общие представления об активном центре ферментов, их химической структуре.
- •Вопрос 18. Сходство и отличие ферментов и неорганических катализаторов. Зависимость скорости ферментативных реакций от температуры, рН. Виды специфичности.
- •Вопрос 19 Активаторы и ингибиторы ферментов. Механизм их действия. Обратимое и необратимое, конкурентное и неконкурентное ингибирование. Использование принципа конкурентного ингибирования в медицине.
- •Вопрос 20 Гормоны. Классификация и биологическая роль.
- •Вопрос 21 Основные системы регуляции метаболизма; иерархия регуляторных систем. Строение и биологическое действие гормонов гипоталамуса и гипофиза. ***
Вопрос 5 Нуклеопротеины, химическое строение днк, рнк, биологическая роль
Нуклеопротеины. Схема гидролиза нуклеопротеинов.
Нуклеопротеины - сложные белки, которые в качестве простетической группы имеют ДНК или РНК.
Схему гидролиза нуклеопротеинов можно представить следующим образом:
Нуклеопротеины

 Белок
ДНК, РНК
Белок
ДНК, РНК
 (гистоны)
(гистоны)
полипептиды полинуклеотиды


а
 минокислоты
мононуклеотиды
минокислоты
мононуклеотиды
нуклеозид Н3РО4

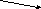 пуриновые
и пентоза
пуриновые
и пентоза
пиримидиновые (рибоза или
основания дезоксирибоза)
Нуклеиновые кислоты, биологическая роль.
Нуклеиновые кислоты (ДНК и РНК) относятся к сложным высокомолекулярным соединениям, состоят из небольшого числа индивидуальных химических компонентов более простого строения. С нуклеопротеинами и, соответственно, нуклеиновыми кислотами непосредственно связаны, кроме того, такие биологические процессы, как митоз, мейоз, эмбриональный и злокачественный рост и др. Нуклеиновые кислоты выполняют ряд важных биологических функ-ций, не свойственных другим полимерным веществам. В частности, они обеспечивают хранение и передачу наследст-венной информации и принимают непосредственное участие в механизмах реализации этой информации путем программирования синтеза всех клеточных белков. Структурные компоненты нуклеиновых кислот выполняют, кроме того, функции кофакторов (коэнзим А и др.), аллостерических эффекторов, входят в состав коферментов (никотин-амидадениндинуклеотид, флавинадениндинуклеотид и др.), принимая тем самым непосредственное участие в обмене веществ, а также в аккумулировании (накоплении), переносе и трасформации энергии. Они являются предшествен-никами вторичных посредников (мессенджеров) – циклических мононуклеотидов (цАМФ и цГМФ), выполняющих
важную функцию в передаче внутриклеточных сигналов.
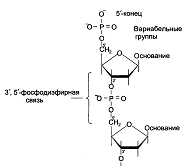
Химическое строение нуклеотидов.
Структурными единицами нуклеиновых кислот являются мономерные молекулы – мононуклеотиды. Следовательно, нуклеиновые кислоты представляют собой полинуклеотиды. Это продукты полимеризации мононуклеотидов, число и последовательность расположения которых в цепях ДНК и РНК определяются в строгом соответствии с программой,
заложенной в молекуле матрицы. Каждый нуклеотид содержит 3 химически различных компонента: гетероциклическое азотистое основание, моносахарид (пентозу) и остаток фосфорной кислоты. В состав нуклеиновых кислот входят азотистые основания двух типов: пуриновые – аденин (А), гуанин (G) и пиримидиновые – цитозин (С), тимин (Т) и урацил (U). В этой «триаде» мононуклеотида углевод занимает
среднее положение. В молекулы ДНК входят A, T, G, C, в РНК- A, C, G, U.
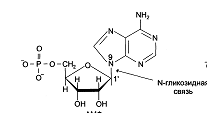
Номенклатура нуклеотидов.

Методы, применяемые при изучении строения нуклеопротеинов.
При изучении химического состава и строения нуклеиновых кислот перед исследователем всегда стоит задача выделения их из биологических объектов.
Для выделения нуклеиновых кислот из комплексов с белками необходимо прежде всего разрушить сильные многочисленные электростатические связи - между "+" заряженной молекулой белков и "-" заряженных молекулами нуклеиновых кислот . Для этого гомогенизированный материал обрабатывают 10% NaCl с последующим осаждением нуклеиновых кислот этанолом. В настоящее время для выделения нуклеиновых кислот в нативном состоянии пользуются фенольным методом, основанным на обработке нейтрально - забуференного раствора. Затем смесь подвергают центрифугированию, при этом денатурированный белок попадает в фенольную фазу, а нуклеиновые кислоты остаются в водной среде, из которой их осаждают на холоду добавлением 2-3-х объёмов этанола. Этим методом удается получить достаточно очищенные препараты нуклеиновых кислот (НК).
В настоящее время применяют ряд усовершенствованных методов разделения НК на фракции из суммарного препарата, полученного описанным выше методом. В их числе хроматография на геле фосфата кальция, ионообменная хроматография (в качестве адсорбентов применяют ДЭАЭ - целлюлозу, ДЭАЭ - сефадекс и др.), ультрацентрифугирование, хроматография по сродству на белковых носителях, метод распределения в двухфазных полимерных системах по Альбертсону, а также ферментативные чисто химические методы гидролиза.
