
- •Введение
- •Краткие исторические и физические сведения. Установки для сжижения газов.
- •Поршневой детандер
- •Центростремительный реактивный турбодетандер
- •Сжижение газа методами Линде и Клода.
- •Метод Клода
- •Производство.
- •Особенности углеводородов
- •Получение сжиженных нефтяных газов из природного газа.
- •Получение сжиженных нефтяных газов из нефти.
- •Хранение жидких газов
- •Применение. Применение в быту
- •Обобщение применения.
- •Значение сжижения газов для научных исследований
Обобщение применения.
Сжижение газов имеет техническое и научное значение. Сжижение воздуха используется в технике для разделения воздуха на составные части. Метод основан на том, что различные газы, из которых воздух состоит, кипят при различных температурах. Наиболее низкие температуры кипения имеют гелий, неон, азот, аргон. У кислорода температура кипения несколько выше, чем у аргона. Поэтому сначала испаряется гелий, неон, азот, а затем аргон, кислород.
Сжиженные газы находят широкое применение в технике. Азот идет для получения аммиака и азотных солей, употребляемых в сельском хозяйстве для удобрения почвы. Аргон, неон и другие инертные газы используются для наполнения электрических ламп накаливания, а также газосветных ламп. Наибольшее применение имеет кислород. В смеси с ацетиленом или водородом он дает пламя очень высокой температуры, применяемое для резки и сварки металлов. Вдувание кислорода (кислородное дутье) ускоряет металлургические процессы. Доставляемый из аптек в подушках кислород облегчает страдания больных. Особенно важным является применение жидкого кислорода в качестве окислителя для двигателей космических ракет. Двигатели ракеты-носителя, поднявшей в космос первого космонавта Ю. А. Гагарина, работали на жидком кислороде.
Жидкий водород используется как топливо в космических ракетах. Например, для заправки американской ракеты «Сатурн-5» требуется 90 т жидкого водорода. Газы, применяемые в промышленности, медицине и т. п., легче перевозить, когда они находятся в сжиженном состоянии, так как при этом в том же объеме заключается большее количество вещества. Так доставляют в стальных баллонах жидкую углекислоту на заводы газированных вод.
Жидкий аммиак нашел широкое применение в холодильниках — огромных складах, где хранятся скоропортящиеся продукты. Охлаждение, возникающее при испарении сжиженных газов, используют в рефрижераторах при перевозке скоропортящихся продуктов.
Значение сжижения газов для научных исследований
Превращение всех газов в жидкое состояние лишний раз подтвердило единство в строении веществ. Оно показало, что состояние вещества зависит от его температуры и давления, а не определено раз и навсегда для данного тела.
С другой стороны, достигнутые при сжижении газов низкие температуры широко раздвинули границы научных исследований и позволили обнаружить изменение многих свойств веществ при сверхнизких температурах. Упругие тела, сделанные из каучука, становятся при этих температурах хрупкими, как стекло. Кусок резины после охлаждения в жидком воздухе легко ломается, а резиновый мячик при ударе разбивается вдребезги. Ртуть и цинк при низких температурах делаются ковкими, а свинец — пластический металл — упругим, как сталь. Колокольчик, сделанный из свинца, звенит. Очень многие вещества (спирт, яичная скорлупа и др.) после освещения их белым светом создают собственное излучение различного цвета (преимущественно зелено-желтого).
При низких температурах интенсивность теплового движения резко уменьшается, поэтому оказывается возможным наблюдение целого ряда явлений, скрытых при более высоких температурах тепловым движением молекул.
При температурах, близких к абсолютному нулю, сильно изменяются электрические свойства некоторых металлов и сплавов: их сопротивление электрическому току становится равным нулю. Это явление, называемое сверхпроводимостью, открыто Г. Камерлинг-Оннесом в 1911 г. При температуре 2,2 К в жидком гелии исчезает вязкость, т. е. он приобретает свойство сверхтекучести. Сверхтекучесть открыл П. Л. Капица в 1938 г.
Вклад учёных в изучение газов очень велик и мал с предстоящими открытиями.
Лицей №1
Творческая работа
по физике
на тему:
«Сжижение газов»

Выполнил
Ученик 10 класса А
Зорин Юрий
Руководитель
Кожакина Г. М.
г. Тула, 2007
Задачи.
Два одинаковых баллона, содержащие газ при температуре T=0оС, соединены узкой горизонтальной трубкой диаметром d=5 мм, посередине которой находиться капелька ртути. Она делит весь сосуд на две части объёмом по V=200 см3 . На какое расстояние x переместиться капелька, если один баллон нагреть на t=2o C, а другой на столько же охладить? Изменением объёмов сосудов пренебречь.
Решение:
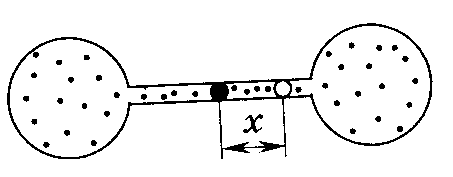
Обозначим через V, р и Т начальные: объем, давление и температуру воздуха в каждой из половин сосуда и соответственно через V1 р1 Т1 и V2, р2, Т2 — состояния воздуха в них после нагревания первого баллона на дельта Т и такого же охлаждения второго баллона. Уравнения состояния для газов в обоих баллонах:
![]()
Получаем, что
![]()
![]()
Но капелька ртути будет перемещаться до тех пор, пока р1 не станет равным р2, тогда из равенства следует, что
![]()
Обозначив через х — смещение капельки ртути, через S — площадь сечения трубки, можно записать:
V1=V +Sx
V2 =V-Sx
Тогда
(V +Sх)/(V - Sх) = (Т + t)/(T - t),
откуда найдем
x=Vt/ST
S=пd2/4
х = 4Vt/(пd2T).
x=7.45
Ответ: х=7,45
Баллон для газовой плиты объёмом V=5 л содержит м=500 г пропана (С3Н8) под давлением р=2 Мпа. Температура t= 20 град С. Что можно сказать об агрегатном состоянии пропана в баллоне?
=m/V=100кг/м3
PV=mRT/M ;
M=mRT/PV=0.121кг/моль
M(C3H8)=44*0.01кг/моль
Сравнив с агрегатным состоянием придём к выводу, что там жидкость.


